-
某同学在实验报告中有以下实验数据记录,其中合理的是
A. 用托盘天平称取11.72g食盐
B. 用100mL的量筒量取25.00mL盐酸
C. 用pH试纸测得某稀醋酸溶液的pH为3.5
D. 用0.2000mol•L-1HC1溶液滴定20.00mL未知浓度NaOH,用去22.40 mL HC1溶液
难度: 中等查看答案及解析
-
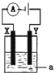
实验室中用电解水的方法制取氢气和氧气,为了增强溶液的导电性最好加入下列电解质中的
A.NaCl B.Na2SO4 C.CuCl2 D.AgNO3
难度: 中等查看答案及解析
-
石墨和金刚石都是碳元素的单质,已知C(石墨,s)=C(金刚石,s) △H>0,下列说法正确的是
A. 石墨不如金刚石稳定
B. 等质量的石墨与金刚石完全燃烧,二者放出的热量相等
C. 等质量的石墨与金刚石完全燃烧,金刚石放出的能量少
D. 金刚石不如石墨稳定
难度: 简单查看答案及解析
-
下列关于反应能量的说法正确的是
A. Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s)△H=-216kJ•mol-1,则反应物总能量大于生成物总能量
B. 吸热反应中由于反应物总能量小于生成物总能量,因而没有价值
C. 101kPa时,2H2(g)+O2(g)=2H2O(l)△H=-571.6k•mol-1,则H2的燃烧热为571.6k•mol-1
D. 已知H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ•mol-1,则含1 mol NaOH的溶液与含0.5molH2SO4的浓硫酸混合后放出57.3kJ的热量
难度: 简单查看答案及解析
-
反应A(g)+3B(g)=2C(g)+2D(g)在不同情况下测得的反应速率如下所示,其中反应速率最快的是
A. v(D)=0.4 mol/(L·s) B. v(C)=0.5 mol/(L·s)
C. v(B)=0.6 mol/(L·s) D. v(A)=0.15 mol/(L·s)
难度: 简单查看答案及解析
-
下列说法中正确的是
A. 凡是放热反应都足自发的,吸热反应都处非自发的
B. 自发反应一定是熵增大,非自发反应一定是熵减小或不变
C. 熵增加且放热的反应一定是自发反应
D. 非自发反应在任何条件下都不能实观
难度: 简单查看答案及解析
-
一定温度下,在一定体积的密闭容器中,可逆反应2NO(g)+Br2(g)
2NOBr(g)体系中,Br2(g)随时间变化的实验数据如下表所示:
时间/min
5
10
15
20
25
30
n(Br2)/mol
0.080
0.075
0.072
0.070
0.070
0.070
根据表中的数据,下列时间中表示该反应达到平衡状态的是
A. 5min B. 10min C. 15min D. 20min
难度: 简单查看答案及解析
-
在容积不变的密闭容器中存在如下反应:2A(g)+B(g)
3C(g)+D(s)△H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
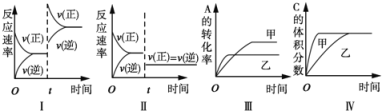
A. 图I表示增加反应物浓度对该平衡的影响
B. 图II表示减小压强对该平衡的影响
C. 图Ⅲ表示温度对该平衡的影响,温度:乙>甲
D. 图IV表示催化剂对该平衡的影响,催化效率:甲>乙
难度: 简单查看答案及解析
-
恒温恒容条件下,反应2AB(g)
A2(g)+B2(g)达到平衡状态的标志是
A. 单位时间内生成n mol A2,同时消耗2n mol AB
B. 容器内,3种气体AB、A2、B2共存
C. 容器中各组分的体积分数不随时间变化
D. AB的消耗速率等于A2的消耗速率
难度: 简单查看答案及解析
-
对于某平衡体系,下列措施一定会使平衡移动的是
A.升高温度 B.使用催化剂
C.改变体系压强 D.改变各组分浓度
难度: 中等查看答案及解析
-
如图所示原电池装置中,电解质溶液为硫酸,下列有关叙述错误的是
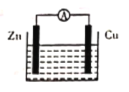
A. 锌做负极发生氧化反应
B. 供电时的总反应为Zn+2H+=Zn2++H2↑
C. 该装置可实现化学能转化为电能
D. 正极产生1 mol H2,消耗锌的质量为32.5 g
难度: 简单查看答案及解析
-
下列关于电解精炼铜的说法中不正确的是
A. 电解质溶液中要含有Cu2+
B. 粗铜作阳极,精铜作阴极
C. 电解时,阳极发生氧化反应,阴极发生还原反应
D. 粗铜中所含Zn、Fe、Ni等杂质电解后以单质形式沉枳于阳极泥中
难度: 简单查看答案及解析
-
钢铁发生析氢腐蚀时,正极上发生的电极反应是
A. 2H++2e-=H2↑ B. Fe2++2e-=Fe
C. 2H2O+O2+4e-=4OH- D. Fe3++e-=Fe2+
难度: 简单查看答案及解析
-
常温下,由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol•L-1,c(SO42-)=0.8mol•L-1,则c(K+)约为
A. 0.4 mol•L-1 B. 0.3 mol•L-1
C. 0.2 mol•L-1 D. 0.15 mol•L-1
难度: 简单查看答案及解析
-
醋酸溶液中存在电离平衡 CH3COOH
CH3COO- + H+,下列叙述不正确的是
A. 升高温度,平衡正向移动,醋酸的电离常数Ka增大
B. 0.10 mol/L的CH3COOH 溶液加水稀释,溶液中c(OH-)增大
C. CH3COOH溶液加少量的CH3COONa固体,平衡逆向移动
D. 室温下,欲使0.1 mol/L醋酸溶液的pH、电离度α都减小,可加入少量水
难度: 简单查看答案及解析
-
HA为一元弱酸,在0.1 mol/L的NaA溶液中,离子浓度关系正确的是
A. c(Na+)>c(A-)>c(H+)>c(OH-)
B. c(Na+)>c(OH-)>c(A-)>c(H+)
C. c(Na+)+c(OH-)=c(A-)+c(H+)
D. c(Na+)+c(H+)=c(A-)+c(OH-)
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 在温度不变时,水溶液中c(H+)和c(OH-)不能同时增大
B. pH=14的溶液是碱性最强的溶液
C. 中性溶液中必然有c(H+)=c(OH-)=1×10-7mol/L
D. 酸或碱溶液稀释时,溶液的pH均减小
难度: 中等查看答案及解析
-
向5 mL NaCl溶液中滴入一滴AgN03溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变成黑色,根据上述变化过程,分析此三种沉淀物的溶解度关系为
A. AgCl=AgI=Ag2S B. AgCl<AgI<Ag2S
C. AgI>AgCl>Ag2S D. AgCl>AgI>Ag2S
难度: 简单查看答案及解析
-
能使水的电离平衡右移,且其水溶液显碱性的离子是
A. H+ B. OH- C. Al3+ D. HCO3-
难度: 简单查看答案及解析
-
25℃时,某溶液中由水电离出的c(OH-)=1×10-13mol/L,该溶液中一定不能大量共存的离子组是
A. NH4+、Fe3+、SO42-、Cl- B. CO32-、PO43-、K+、Na+
C. Na+、SO42-、NO3-、Cl- D. HCO3-、Na+、HSO3-、K+
难度: 简单查看答案及解析
-
下列事实不能用电化学原理解释的是
A. 铝片不需要特殊的保护方法
B. 炒过菜的铁锅未清洗易生锈
C. 轮船水线以下的船壳上镶有一定数量的锌
D. 生铁比熟铁(几乎是纯铁)容易生锈
难度: 简单查看答案及解析
-
常温下,体积相同、pH相同的HCl溶液和CH3COOH溶液,与NaOH溶液中和时两者消耗NaOH的物质的量
A. 相同 B. 中和HCl的多
C. 中和CH3COOH的多 D. 无法比较
难度: 简单查看答案及解析