-
(1)常温时CuSO4的水溶液呈____(填“酸”“中”或“碱”)性,原因是(用离子方程式表示_________。
(2)在实验室配制FeCl3溶液时,常将FeCl3固体先溶于较浓的______(填物成名称)中,然后用蒸馏水稀释到所需的浓度,以_________(填“促进”或“抑制”)其水解。
(3)把A1C13溶液蒸干、灼烧,最后得到的主要固体产物是____(写化学式)。
高二化学填空题简单题查看答案及解析
-
回答下列问题:
(1)CuSO4的水溶液呈______(填“酸”“中”或“碱”)性,原因是(用离子方程式表示)___________;实验室在配制CuSO4溶液时,常先将CuSO4固体溶于较浓的硫酸中,然后用蒸馏水稀释到所需的浓度,以_____ (填“促进”或“抑制”)其水解。
(2)泡沫灭火器的灭火原理是(用离子方程式表示)________________________。
(3)已知在25℃:AgCl(s)
Ag+(aq)+Cl-(aq) Ksp=1.8×10-10,Ag2S(s)
2Ag+(aq)+S2-(aq) Ksp=6.3×10-50,向浓度均为0.001 mol/L的NaCl和Na2S的混合溶液中,逐滴加入AgNO3溶液,最先产生的沉淀是________(填“AgCl”或“Ag2S”)。
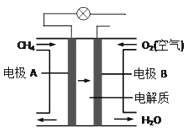
(4)燃料电池能量转化率高,具有广阔的发展前景。天然气燃料电池中,在负极发生反应的物质是 _____(填化学式);如果该电池中的电解质溶液是KOH溶液,电极B电极上发生的电极反应式是:_____________。
高二化学综合题中等难度题查看答案及解析
-
回答下列问题:
(1)CuSO4的水溶液呈______(填“酸”“中”或“碱”)性,原因是(用离子方程式表示)___________;实验室在配制CuSO4溶液时,常先将CuSO4固体溶于较浓的硫酸中,然后用蒸馏水稀释到所需的浓度,以_____ (填“促进”或“抑制”)其水解。
(2)泡沫灭火器的灭火原理是(用离子方程式表示)________________________。
(3)已知在25℃:AgCl(s)
Ag+(aq)+Cl-(aq) Ksp=1.8×10-10,Ag2S(s)
2Ag+(aq)+S2-(aq) Ksp=6.3×10-50,向浓度均为0.001 mol/L的NaCl和Na2S的混合溶液中,逐滴加入AgNO3溶液,最先产生的沉淀是________(填“AgCl”或“Ag2S”)。
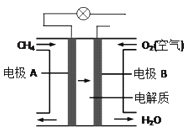
(4)燃料电池能量转化率高,具有广阔的发展前景。天然气燃料电池中,在负极发生反应的物质是 _____(填化学式);如果该电池中的电解质溶液是KOH溶液,电极B电极上发生的电极反应式是:_____________。
高二化学综合题中等难度题查看答案及解析
-
(5分)完成下列化学用语的书写:
(1)用离子方程式表示碳酸钠溶液显碱性的原因:__________ _________。
(2)实验室配制的CuSO4溶液,常常出现浑浊的原因是
(写离子方程式),可采取在配制时加入少量 防止出现浑浊。
(3)泡沫灭火器中盛放的灭火剂包括Al2(SO4)3溶液(约1 mol/L)、NaHCO3溶液(约1 mol/L)及起泡剂。使用时发生反应的离子方程式是_____ _______________________ ____
(4)已知断裂1 mol H2(g)中的H—H键需要吸收436kJ的能量,断裂1 mol O2(g)中的共价键需要吸收498kJ的能量,生成H2O(g)中的1mol H—O键能放出463kJ的能量。试写出O2(g)与H2(g)反应生成H2O(g)的热化学方程式: 。
高二化学填空题中等难度题查看答案及解析
-
溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)Na2CO3溶液显碱性的原因,用离子反应方程式表示_____________________________;CuSO4溶液呈酸性的原因,用离子反应方程式表示:___________________________。
(2)25 ℃时,pH为9的CH3COONa溶液中c(OH-)=________。
(3)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH
)=c(Cl-),则溶液显________(填“酸”“碱”或“中”)性。用含a的代数式表示NH3·H2O的电离常数Kb=___________。
高二化学解答题中等难度题查看答案及解析
-
现有0.1mol/L的纯碱溶液,回答下列问题:
(1)常温下,甲同学用pH试纸检验该溶液,发现其pH>7,你认为原因是什么? (用离子方程式表示)
(2)常温下,乙同学向该溶液中滴入几滴酚酞溶液,发现该溶液遇到酚酞呈红色.对该现象的分析,你认为能得到的结论是:该溶液呈 性.
对为什么遇到酚酞该溶液呈现出红色的原因问题,同学们展开了讨论,乙同学认为,是在配制标准碳酸钠溶液时混入了NaOH所致,而丙同学则认为,是碳酸钠溶液水解所致.
请你设计一个简单的实验方案,来评判上述观点.(要求必须写出操作、现象和结论) .
高二化学填空题中等难度题查看答案及解析
-
(8分)(1)FeCl3的水溶液呈 (“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): 。
(2)实验室在配制 FeCl3的溶液时,常将FeCl3固体先溶于 中,然后再用蒸馏水稀释到所需的浓度。
(3)把FeCl3溶液蒸干,灼烧,最后得到的主要产物是 。
(4)普通泡沫灭火器内的玻璃筒里盛硫酸铝溶液,铁筒中盛碳酸氢钠溶液,其化学反应的原理是(用离子方程式解释) 。碳酸氢钠溶液中的电荷守恒式为 ,溶液中离子浓度由大到小的顺序为 。
高二化学填空题中等难度题查看答案及解析
-
(12分)Ⅰ.(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 ________(填“促进”、“抑制”)其水解。
(2)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。
Ⅱ. 已知水在25 ℃(A)和T ℃(B)时,其电离平衡曲线如图所示:

(1)25 ℃时,将pH=3 的H2SO4溶液与pH=10的NaOH溶液混合,若所得混合溶液的pH=7,则H2SO4溶液与NaOH溶液的体积比为 。
(2)T ℃时,若10体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强Ⅰ碱的pH2之间应满足的关系是 。
(3)曲线B对应温度下,pH=3的HCl溶液和pH=9的某碱溶液等体积混合后,混合溶液的pH>7。请分析其原因: 。
高二化学填空题困难题查看答案及解析
-
(1)Cu(NO3)2的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ;实验室在配制 AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈 性,原因是(用离子方程式表示): 。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)在配制氯化铁溶液时,为了防止发生水解,可以加入少量的 。
高二化学填空题中等难度题查看答案及解析
-
(16分,每空2分)(1)FeCl3的水溶液呈(填 “酸”、“中”、“碱”)性,常温时的pH ________7(填“>”、“=”、“<”),原因是(用离子方程式表示):
;实验室在配制FeCl3的溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,以________(填“促进”、“抑制”)其水解。
(2)醋酸电离方程式: ,
氯化铝在水中电离方程式:_____________________________________________ 。
把氯化铝溶液蒸干,灼烧,最后得到的主要固体产物是________ 。
(3)热的纯碱溶液清洗油污效果比冷的好,这是因为。
高二化学填空题简单题查看答案及解析