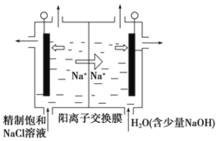
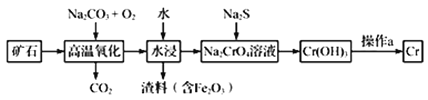
-
升高温度,下列数据不一定增大的是
A. 化学反应速率v B. 水的离子积常数KW
C. 化学平衡常数K D. 醋酸的电离平衡常数Ka
难度: 中等查看答案及解析
-
化学与社会、生产、生活密切相关,下列说法错误的是
A. “煮豆燃豆萁,豆在釜中泣”,句中涉及的能量变化主要是化学能转化为热能和光能
B. 泡沫灭火器可用于一般的起火,也适用于电器起火
C. 加入Na2S可除去工业废水中Cu2+和Hg2+等离子
D. 草木灰不能与铵态氮肥混合施用
难度: 中等查看答案及解析
-
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中正确的是
A. 汽车用的铅蓄电池充电时阳极反应:PbSO4+2H2O-2e-== PbO2+4H++SO42﹣
B. 利用Na2CO3溶液可除油污:CO32- + 2H2O
H2CO3 + 2OH-
C. BaSO4的水溶液导电性极弱:BaSO4
Ba2++SO42﹣
D. 用醋酸除去暖瓶中的水垢:2H++CaCO3== Ca2++ CO2↑+ H2O
难度: 中等查看答案及解析
-
下列依据热化学方程式得出的结论正确的是
A. 已知2SO2(g)+O2(g)
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B. 已知2C(s)+2O2(g) == 2CO2(g) ΔH1, 2C(s)+O2(g)==2CO(g) ΔH2,则ΔH1<ΔH2
C. 已知H+(aq)+OH-(aq) == H2O(l) ΔH=-57.3kJ·mol-1,则任何酸碱中和反应的热效应数值均为57.3kJ
D. 已知C(石墨,s) == C(金刚石,s) ΔH>0,则金刚石比石墨稳定
难度: 中等查看答案及解析
-
稀氨水中存在着下列平衡:NH3·H2O
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
①NH4Cl固体;②硫酸;③NaOH固体;④水;⑤加热;⑥加入少量MgSO4固体。
A. ①②③⑤ B. ③⑥ C. ③ D. ③⑤
难度: 中等查看答案及解析
-
室温下,下列比值为2∶1的是
A. pH=2 与pH=1的硝酸中c(H+)之比
B. 等浓度的(NH4)2SO4(aq)与NH4Cl(aq)中c(NH4+)之比为2:1
C. 0.2mol/L 与0.lmol/L 醋酸中c(H+)之比
D. pH=7的硫酸铵与氨水混合溶液中c(NH4+)与c(SO42-)之比
难度: 中等查看答案及解析
-
下列叙述中,不能用平衡移动原理解释的是
A. 用排饱和食盐水的方法收集氯气
B. SO2催化氧化制SO3的过程中使用过量的氧气,以提高二氧化硫的转化率
C. 溴水中有下列平衡Br2+H2O
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
D. 锌与稀硫酸反应,加入少量硫酸铜反应速率加快
难度: 中等查看答案及解析
-
下列条件下,对应离子一定能大量共存的是
A. 中性溶液中:Mg2+ 、Fe3+ 、SO32- 、Cl-
B. 使甲基橙变红的溶液中:NH4+ 、Al3+、SO42﹣、Mg2+
C. 25℃时,水电离出的c(H+)=1×10-13mol/L:K+ 、Ba2+ 、NO3-、S2-
D. c(H+)/c(OH-) = 1×1012的溶液中:Fe2+、NO3-、HCO3-、Na+
难度: 中等查看答案及解析
-
下列有关生活生产中的叙述合理的是
A. 铜的精炼工业和电镀铜工业,均可采用CuSO4溶液做电解质溶液
B. 明矾和漂白粉分别用于自来水的净化和杀菌消毒,两者的作用原理相同
C. 水库的钢闸门与电源负极相连以防止其生锈,该法即牺牲阳极的阴极保护法
D. 工业上合成氨采用500℃左右的温度,其原因是适当加快NH3 的合成速率,催化剂在500℃左右时其活性最好,且能提高H2的转化率
难度: 困难查看答案及解析
-
NA是阿伏加德罗常数的值,下列说法正确的是
A. 0.1mol FeCl3完全水解形成Fe(OH)3胶体的胶粒数为0.1NA
B. 1 mol N2 与 3 mol H2 充分反应,产物的分子数为 2NA
C. 钢铁发生吸氧腐蚀时,0.56g Fe反应转移电子数为0.03NA
D. 1L 0.1mol·L-1的NaHCO3溶液中HCO3- 和CO32-离子数之和小于0.1NA
难度: 困难查看答案及解析
-
为达到预期的实验目的,下列操作中正确的是
A. 用玻璃棒蘸取待测液滴在润湿的pH试纸上,测得其pH为12
B. 制FeCl3溶液时,将FeCl3固体溶于盐酸中,然后再用水稀释到所需的浓度
C. 中和热测定的实验中使用的玻璃仪器只有2种
D. 在滴定时,左手操作锥形瓶,右手操作滴定管开关
难度: 中等查看答案及解析
-
合成氨化学方程式 N2(g)+3H2(g)
2NH3(g) △H=−92.4 kJ/mol。将l mol N2(g)、3 mol H2(g)充入2 L的密闭容器中,在500℃下反应,10 min 时达到平衡,NH3的体积分数为
,下列说法中正确的是

A. 若达到平衡时,测得体系放出9.24 kJ热量,则H2反应速率变化曲线如图甲所示
B. 反应过程中,混合气体平均相对分子质最M,混合气体密度d,混合气体压强p,三者关系如图乙所示
C. 图丙容器I和II达到平衡时,NH3的体积分数
,则容器I放出热量与容器II吸收热量之和为92.4 kJ
D. 若起始加入物料为1 mol N2,3 mol H2,在不同条件下达到平衡时,NH3的体积分数变化如图丁所示
难度: 中等查看答案及解析
-
下列说法正确的是
A. 在其他外界条件不变的情况下,增大压强能增大活化分子的百分数
B. NH4Cl(s)=NH3(g)+HCl(g)室温下不能自发进行,说明该反应的△H <0
C. 加入合适的催化剂能降低反应活化能,从而改变反应的焓变
D. 常温下,KSP[Al(OH)3]=1×10-33。欲使溶液中c(Al3+)≤ 1×10-6 mol/L,需调节溶液的pH≥5
难度: 中等查看答案及解析
-
氮氧化物具有不同程度的毒性,利用构成电池方法既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,发生反应 6NO2+ 8NH3= 7N2+12H2O,装置如图所示。下列关于该电池的说法正确的是
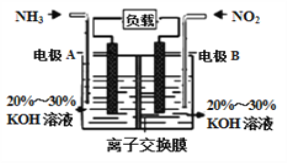
A. 为使电池持续放电,离子交换膜需选用阴离子交换膜
B. 电子从右侧电极经过负载后流向左侧电极
C. 电极A极反应式为2NH3 - 6e-=N2 +6H+
D. 当有4.48LNO2被处理时,转移电子物质的量为 0.8mol
难度: 中等查看答案及解析
-
根据下列实验操作和现象所得到的结论正确的是
选项
结论
操作
A
CO32-水解是吸热反应
在0.1 mol/LNa2CO3溶液中,滴加2滴酚酞显浅红色,微热,红色加深
B
Ksp(BaSO4)>Ksp(BaCO3)
常温下,用饱和Na2CO3溶液可将BaSO4全部转化为BaCO3
C
酸性A比B强
等体积、pH=3的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多
D
金属性:M>N
由M、N与稀硫酸构成的原电池中,M上产生大量气泡
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值。如某溶液中某溶质的浓度为1×10-3mol·L-1,则该溶液中该溶质的pC=-lg(1×10-3) = 3。下图为25℃时H2CO3溶液的pC-pH图(若离子浓度小于10-5 mol·L-1,可认为该离子不存在)。下列说法错误的是
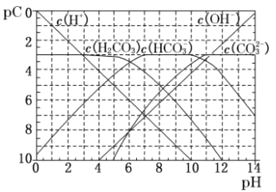
A. 向Na2CO3溶液中滴加盐酸至pH等于11时,溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-)+c(Cl-)
B. 25℃时,H2CO3的一级电离平衡常数Ka1= 10-6
C. 25℃时,CO2饱和溶液的浓度是0.05 mol·L-1,其中1/5的CO2转变为H2CO3,若此时溶液的pH 约为5,据此可得该温度下CO2饱和溶液中H2CO3的电离度约为1%
D. 25℃时,0.1 mol·L-1,的Na2CO3和0.1 mol·L-1的NaHCO3混合溶液中离子浓度的大小为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
难度: 中等查看答案及解析