-
下列物质的用途,主要利用了该物质化学性质的是( )
A.干冰用于人工降雨 B.氮气用作充氮包装
C.铜用作制导线 D.石墨用作制铅笔芯
难度: 简单查看答案及解析
-
下列实验操作正确的是( )
A.
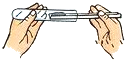 用纸槽取固体粉末 B.
用纸槽取固体粉末 B.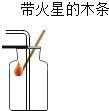 验满氧气
验满氧气C.
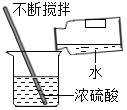 稀释浓硫酸 D.
稀释浓硫酸 D.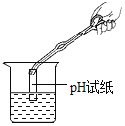 测溶液pH
测溶液pH难度: 简单查看答案及解析
-
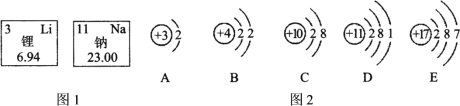
下列有关原子的说法不正确的是( )
A.原子中质子数一定等于电子数 B.原子中一定含有质子、中子和电子
C.原子的质量主要集中在原子核上 D.金属原子最外层的电子一般少于4个
难度: 简单查看答案及解析
-
下列客观事实对应的微观解释正确的是( )
A.炎热的夏天,自行车轮胎易爆胎——温度升高,分子体积变大
B.分离液态空气制氧气——分子可以再分
C.CO2和CO化学性质不同——分子构成不同
D.金刚石和石墨物理性质差异较大——碳原子结构不同
难度: 简单查看答案及解析
-
燃料及其燃烧被广泛应用于生活和生产中。下列有关燃料和燃烧的说法正确的是( )
A.燃料完全燃烧时,一定会生成二氧化碳
B.石油通过炼制可以得到汽油、柴油
C.物质与氧气发生反应时都会伴随发光、放热现象
D.化学反应中只有燃烧能放出热量
难度: 中等查看答案及解析
-
在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前后各物质的质量如下表所示。下列说法不正确的是( )
物质
甲
乙
丙
丁
反应前物质的质量/g
4
10
3
4
反应后物质的质量/g
6
4
x
8
A.乙一定是化合物 B.丙可能是该反应的催化剂
C.反应中的乙和丁质量变化之比为3:2 D.丁的相对分子质量一定是甲的2倍
难度: 中等查看答案及解析
-
下图为某化学反应的微观示意图。下列说法正确的是( )
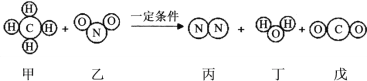
A.1个乙分子中有3个原子核 B.该反应中属于有机物的有2种
C.甲中碳、氢元素的质量比为l:4 D.反应后生成丙和丁的分子个数比为1:1
难度: 中等查看答案及解析
-
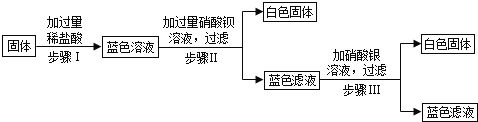
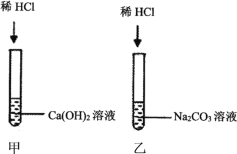
学习了酸、碱、盐的性质后,同学们设计了下面实验方案,其中不正确的是( )
A.浓硫酸干燥氢气和氧气 B.澄清的石灰水检验二氧化碳气体
C.少量稀盐酸检验熟石灰是否变质 D.石灰石、纯碱和水为原料制取烧碱
难度: 困难查看答案及解析
-
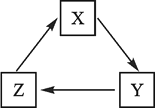
下列各组物质间通过一步反应就能实现如图转化的是
X
Y
Z
A
Fe
FeCl2
Fe2O3
B
Ca(OH)2
NaOH
NaCl
C
AgNO3
Ba(NO3)2
BaSO4
D
H2O
O2
CO2
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列各组物质的溶液,不另加试剂就不能将它们区别开来的一组是( )
A.Fe2(SO4)3、NaOH、H2SO4、Ba(OH)2
B.K2CO3、Na2SO4、KNO3、BaCl2
C.Ca(NO3)2、Na2CO3、NaCl、HNO3
D.K2CO3、H2SO4、HNO3、BaCl2
难度: 困难查看答案及解析