-
从海水中提取的溴占世界产溴量的1/3。已知溴水呈橙色,将SO2气体通入溴水时,可以观察到溴水褪色。则下列有关叙述中正确的是( )
A.SO2使溴水褪色,显示了SO2的漂白性
B.SO2是形成酸雨的唯一原因
C.从溴水中提取单质溴,可以用乙醇进行萃取
D.SO2使溴水褪色,显示了SO2的还原性
难度: 简单查看答案及解析
-
某些化学试剂可用于净水。水处理中使用的一种无机高分子混凝剂的化学式可表示为[Al2(OH)nClm·yH2O]X,式中m等于( )
A.6-n B.3-n C.6+n D.3+n
难度: 简单查看答案及解析
-
下列冶炼金属的对应关系中错误的是( )
金属冶炼
冶炼方法
A
火烧孔雀石
焦炭法
B
湿法炼铜
水煤气法
C
铝热法炼铬
活泼金属置换法
D
光卤石炼镁
电解法
难度: 简单查看答案及解析
-
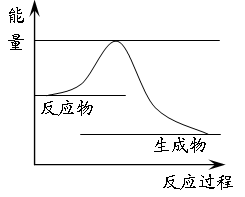
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是( )

A.该反应为放热反应 B.催化剂能降低反应的活化能
C.催化剂能改变反应的焓变 D.逆反应的活化能大于正反应的活化能
难度: 简单查看答案及解析
-
已知氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1 mol氢气中的化学键消耗的能量为Q1KJ,破坏1 mol氯气中的化学键消耗的能量为Q2KJ,形成1 mol氯化氢中的化学键释放的能量为Q3KJ,则下列关系式中一定正确的是( )
A.Q1+Q2<2Q3 B.Q1+Q2>2Q3 C.Q1+Q2<Q3 D.Q1+Q2=Q3
难度: 简单查看答案及解析
-
一种“即食即热型快餐”适合外出旅行时使用。其内层是用铝箔包裹的、并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是( )
A.浓硫酸与水 B.熟石灰与水 C.生石灰与水 D.氯化钠与水
难度: 简单查看答案及解析
-
下列化学反应的热量变化可用:H+(aq) + OH-(aq) = H2O(l),△H= —57.2kJ/mol表示的是( )
A.含有1molH2SO4的浓硫酸与含有1molNaOH的稀溶液混合
B.0.1 mol/L 的醋酸溶液与 1mol/L的NaOH溶液等体积混合
C.1mol/L的盐酸10mL与1mol/L的NaOH15mL混合
D.1mol/L的盐酸10mL与1mol/L的氨水15mL混合
难度: 简单查看答案及解析
-
下列说法或表示方法中正确的是( )
A.等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多
B.氢气的燃烧热为285.8kJ ·
,则氢气燃烧的热化学方程式为
2H2(g)+O2(g)=2H2O(l);△H=-285.8 kJ·
C.Ba(OH)2 · 8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l);△H<0
D.某酸溶液可以与石灰石反应放出CO2,则该酸不一定为强酸。
难度: 简单查看答案及解析
-
现有下列四个小实验,简要实验步骤及现象如下
①在紫色的KMnO4酸性稀溶液中,逐滴滴入过氧化氢溶液,溶液温度变化不大,但褪色速率越来越快
②将化学荧光棒[外层是塑料管放草酸二苯酯(还原剂)及发光颜料,内玻璃管中放入4%过氧化氢溶液]弯曲,内管断裂,液体混合,发出五颜六色的光。
③两根外形相同的铁棒和锡棒紧靠,放入稀硫酸中,发现一根棒的表面有气泡产生
④正在烧煤球的煤炉中,滴上几滴水,立刻串出火苗
下列分析正确的是( )
A.实验①中,反应生成的Mn2+可能是该反应的催化剂
B.实验②中,该反应是太阳能转变为光能
C.实验③中,有气泡产生的棒是铁棒
D.实验④中,加入的水是反应的催化剂,且该反应能自发进行
难度: 简单查看答案及解析
-
在298K、100kPa时,已知: 2H2O(g)=O2(g)+2H2(g) △H1
Cl2(g)+H2(g)=2HCl(g) △H2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) △H3
则△H3与△H1和△H2间的关系正确的是( )
A.△H3=△H1+2△H2 B.△H3=△H1+△H2
C.△H3=△H1-△H2 D.△H3=△H1-△H2
难度: 简单查看答案及解析
-
相同温度下,两个恒压且压强相同的密闭容器中发生可逆反应
实验测得反应在起始及达到平衡时的有关数据如下表所示:
容器编号
起始时各物质物质的量/mol
达平衡时体系能量变化
X2
Y2
XY3
①
0.1
0.3
0
4.63 kJ
②
0.8
2.4
0.4
Q(Q>O)kJ
下列叙述正确的是( )
A.反应的平衡常数:①>②
B.达平衡时,两个容器中XY3的物质的量浓度均为
C.若容器①体积为0.20L.则达平衡时放出的热量大于4.63kJ
D.达到平衡时,容器①、②中各物质的百分含量相同
难度: 简单查看答案及解析
-
用蒸馏水稀释
的醋酸至
,稀释过程中温度维持25℃不变,下列各项中始终保持增大趋势的是 ( )
A.c(H+)
c(OH— ) B.c(H+) C.
D.
难度: 简单查看答案及解析
-
用
溶液完全中和pH=3的下列溶液各100mL需NaOH溶液体积最大的是( )
A.硫酸氢钠 B.硫酸 C.氢氟酸 D.氯酸
难度: 简单查看答案及解析
-
(6分)将V1 ml 1.0 mol/L HCl溶液和V2 ml未知浓度的NaOH溶液混合均匀后测量并记录溶液的温度,实验结果如图所示(实验中始终保持V1+V2==50 ml)。下列叙述中不正确的是

A.当V1==30 ml时,盐酸和NaOH溶液恰好完全反应
B.NaOH溶液的浓度约为1.5 mol/L
C.做该实验时环境温度为22℃
D.该实验表明化学能可以转化为热能
难度: 简单查看答案及解析