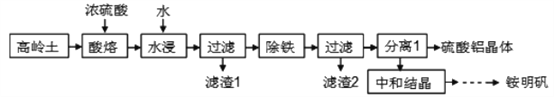
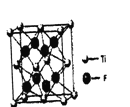
-
短周期主族元素X、Y、Z、W的原子序数依次增大,X的原子半径比Y的小,Y原子最外层电子数是其内层电子总数的3倍,W原子的核电荷数等于X、Z原子的核电荷数之和,X和Z同主族。下列说法正确的是
A. 原子半径:r(W)>r(Z)>r(Y)
B. Z的最高价氧化物对应水化物的碱性比W的强
C. 化合物X2Y2和Z2Y2所含化学键类型完全相同
D. 工业上常用电解熔融W的氧化物制备W的单质
难度: 简单查看答案及解析
-
下列有关物质的性质与用途具有对应关系的是
A. NH3极易溶于水,可用于工业制冷剂
B. 木炭具有还原性,可用于冰箱和居室除臭剂
C. Al2O3是两性氧化物,可用于制造高温材料
D. Na、K合金熔点低且导热,可用于快中子反应堆的导热剂
难度: 简单查看答案及解析
-
根据下列实验操作和现象所得到的结论正确的是
选项
实验操作和现象
结论
A
取少量淀粉水解液于试管中,加入过量氢氧化钠溶液和新制Cu(OH)2悬浊液,加热至沸腾,出现砖红色沉淀。
淀粉己完全水解
B
向浓度均为0.1 mol·L-1的Na2CO3和Na2S的混合溶液中,滴入少量AgNO3溶液,先产生黑色沉淀(Ag2S)。
Ksp(Ag2S)<Ksp(Ag2CO3)
C
向溶液X中先滴加稀硝酸,再滴加BaCl2溶液,出现白色沉淀。
溶液X中一定含有SO42-
D
溴乙烷与NaOH乙醇溶液共热产生的气体通入KMnO4酸性溶液中,溶液褪色。
产生的气体为乙烯
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
在探究Ba2ClO(OH)3·H2O性质的实验中,取该物质溶解后,分别和下列溶液充分混合搅拌,反应后溶液中主要存在的一组离子正确的是
A. 加入过量浓盐酸:H+、Ba2+、Cl-、ClO-
B. 加入过量NaHCO3稀溶液:Na+、HCO3-、CO32-、ClO-
C. 加入过量Fe(NO3)2溶液:Ba2+、NO3-、Fe2+、ClO-
D. 加入过量Na2SO4溶液:Ba2+、ClO-、Na+、SO42-
难度: 中等查看答案及解析
-
下列关于元素及其化合物的说法中正确的是
A. Fe为活泼金属,常温下可与浓硝酸、稀硝酸、浓硫酸剧烈反应
B. Na久置于空气中,可以和空气中的有关物质发生反应,最终生成NaHCO3
C. 铝具有良好的导电性,钢抗拉强度大,钢芯铝绞线可用作远距离高压输电线材料
D. 铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀
难度: 中等查看答案及解析
-
下列有关化学用语表示正确的是
A. 中子数为20的氯原子:
Cl B. 硫离子的结构示意图:
C. N2H4的电子式:
D. 丙烯的结构简式:CH2CHCH3
难度: 简单查看答案及解析
-
下列指定反应的离子方程式正确的是
A. 向Al2(SO4)3溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓
B. 向Fe(OH)3胶体中加入氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O
C. 将NaClO溶液与亚硫酸钠溶液混合:ClO-+SO32-=SO42-+Cl-
D. 用石墨作电极电解氯化镁溶液:2Cl-+2H2O
H2↑+Cl2↑+2OH-
难度: 简单查看答案及解析
-
下列装置用于实验室制备氨气并配制银氨溶液,不能达到实验目的的是
A.
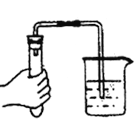 检查气密性 B.
检查气密性 B.  制备氨气 C.
制备氨气 C. 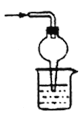 吸收氨尾气 D.
吸收氨尾气 D. 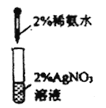 配制银氨溶液
配制银氨溶液难度: 中等查看答案及解析
-
在给定的条件下,下列选项所示的物质间转化均能一步实现的是
A. SiO2
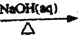 Na2SiO3
Na2SiO3H2SiO3
B. S
SO2
BaSO3
C. NH3
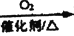 NO2
NO2 HNO3
D. MgCl2·6H2O
MgCl2
Mg
难度: 中等查看答案及解析
-
轴烯是一类独特的星形环烃。三元轴烯(
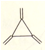 )与苯
)与苯A. 均为芳香烃 B. 互为同素异形体
C. 互为同系物 D. 互为同分异构体
难度: 中等查看答案及解析
-
1.52g 铜镁合金完全溶解于50mL 密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )。
A. 该合金中铜与镁的物质的量之比是2:1
B. 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
难度: 简单查看答案及解析
-
4-AFMF是一种探测物质的荧光素,其结构简式如下图。下列有关该物质的说法正确的是
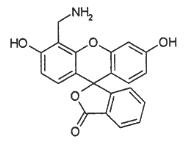
A. 分子中三个苯环处于同一平面
B. 1 mol 4-AFMF 最多可与2molNaOH 反应
C. 在酸性条件下水解,水解产物只有1种
D. 能与溴水、FeCl3溶液及稀硫酸发生反应
难度: 简单查看答案及解析
-
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20 mLpH=14的溶液(不考虑水解),然后用1mol/L的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是
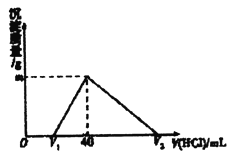
A. 原合金质量为0.92 g B. 产生氢气的体积为1120mL(标准状况下)
C. 图中m的值为1.56 D. 图中V2的值为60
难度: 困难查看答案及解析
-
298K时,在20.0mL0.10mol·L-1氯水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。己知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是
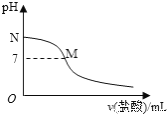
A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. N点处的溶液中pH<12
难度: 困难查看答案及解析
-
在①、②、③容积不等的恒容密闭容器中,均充入0.lmolCO和0.2molH2,在催化剂的作用下发生反应:CO(g)+2H2(g)
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:
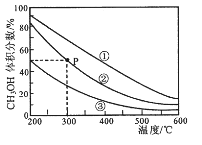
下列说法正确的是
A. 该反应的正反应为放热反应
B. 三个容器容积:①>②>③
C. 在P点,CO转化率为75%
D. 在P点,向容器②中再充入CO、H2 及 CH3OH 各 0.025mol,此时 v(CO)正<v (CO)逆
难度: 困难查看答案及解析