-
下列物质能够反应,且没有明显现象的是( )
A. Na2CO3溶液加入澄清石灰水中
B. Fe2O3加入NaOH溶液中
C. 稀HCl滴入Ba(OH)2溶液中
D. CO2通入澄清石灰水中
难度: 简单查看答案及解析
-
金属钛有银白色金属光泽,密度为4.5gcm-3,熔点为1725℃,具有良好的延展性和耐腐蚀性。下列物品不能用钛制作的是( )
A. 保险丝
B. 医疗器械
C. 潜艇外壳
D. 眼镜架
难度: 中等查看答案及解析
-
联合国卫生组织经过考察和研究,认为我国使用的铁锅是有益于人类健康的理想炊具,并向全世界推广,其主要原因是( )
A. 可有效减少缺铁性贫血
B. 熔点较高
C. 价格便宜,不易生锈
D. 传热慢,保温性能好
难度: 简单查看答案及解析
-
下列关于化肥的说法中,正确的是( )
A. (NH4)2SO4属于复合肥料
B. 从外观即可把NH4NO3与KCl区别开
C. 农作物所必需的营养元素只有氮、磷和钾三种
D. NH4Cl与熟石灰混合有刺激性气味气体放出
难度: 简单查看答案及解析
-
人们对事物的认识常需经历一个不断修正和完善的过程,如对酸的认识就是如此。下列各项是不同时期对酸的认识,其中与我们现在所学酸的定义最相近的是
A. 有酸味的物质 B. 只有氢才是酸不可缺少的元素
C. 一切酸中都含有氧 D. 与碱作用时失去原有性质的物质
难度: 中等查看答案及解析
-
科技文献中经常出现下列词汇,其中与相关物质的颜色并无联系的是( )
A. 赤色海潮
B. 绿色食品
C. 白色污染
D. 棕色烟气
难度: 简单查看答案及解析
-
金属活动性顺序在科学研究中有重要应用。已知锌、铁、铜三种金属与其盐溶液之间能发生如下反应:Zn+FeSO4===ZnSO4+Fe;Fe+CuSO4===FeSO4+Cu。则三种金属的活动性顺序从强到弱的排列是
A. Zn>Fe>Cu
B. Cu>Fe>Zn
C. Fe>Cu>Zn
D. Cu>Zn>Fe
难度: 简单查看答案及解析
-
近年来,经过我国科学家的努力,制造出了国产芯片“龙芯一号”和“龙芯二号”,芯片的核心部件是以高纯度的单质硅为原材料制造的。用化学方法制得高纯度硅的反应原理是
,该反应属于( )
A. 化学反应
B. 分解反应
C. 复分解反应
D. 置换反应
难度: 简单查看答案及解析
-
向100g质量分数为3.65%的盐酸中逐滴加入4%的氢氧化钠溶液,同时测定有关数据,下列图像正确的是(横坐标为每次加入氢氧化钠溶液的量)( )
A.
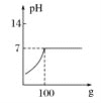
B.

C.

D.

难度: 困难查看答案及解析
-
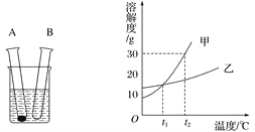
甲物质的溶液可用作化肥、电镀液等。甲的溶解度曲线如图所示,下列说法正确的是
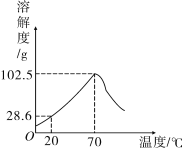
A.甲的溶解度是102.5g
B.甲的溶解度随温度的升高而增大
C.20℃时,100 g甲的饱和溶液中溶质质量为28.6 g
D.将70℃甲的饱和溶液升高温度或降低温度,都有晶体析出
难度: 中等查看答案及解析
-
金属防锈既可以节约资源,又能美化环境.下列钢铁制品经过如下处理后,防锈效果最差的是( )
A.经常在表面涂油的大型钢制机械
B.涂上防锈漆后的“辽宁”号航母舰体外壳
C.擦洗干净后长期存放在室外的大型铁制农机具
D.经过“烤蓝”,在表面形成致密氧化膜的钢制枪管
难度: 简单查看答案及解析
-
化学源自生活,又服务于生活,化学知识可以用于解决许多生活问题。下列做法中不符合化学原理的是
A. 用食醋除去热水瓶的薄层水垢
B. 用米汤检验食用碘盐中的碘酸钾
C. 人体被蜂、蚁等叮咬而射入蚁酸后,可用肥皂水消除相关症状
D. 用灼烧并闻气味的方法区别纯棉织物和纯毛织物
难度: 中等查看答案及解析
-
a、b、c 三种物质的溶解度曲线如下图所示。取等质量
℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至
℃。下列说法不正确的是
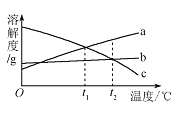
A. 原饱和溶液中,溶质的质量分数 a>b="c"
B. 恢复至 t2℃时,析出溶质的质量 a>b=c
C. 恢复至t2℃时,三种溶液一定都是饱和溶液
D. 若继续降温至 t1℃,三种溶液一定都是饱和溶液
难度: 困难查看答案及解析
-
下列金属单质能与稀硫酸发生置换反应的是
A. 铁
B. 金
C. 铜
D. 银
难度: 简单查看答案及解析
-
小强家的仓库里存有少量无标签但密封良好的化肥。为了确定该化肥的成分,他取少量化肥与熟石灰粉末混合、研磨,闻到刺激性气味。由此判断该化肥可能为
A. 氯化铵
B. 碳酸钾
C. 硫酸钾
D. 硝酸钠
难度: 简单查看答案及解析
-
下图是氢氧化钙的溶解度曲线。在冬天气温为5 ℃时配制的氢氧化钙饱和溶液,在夏天气温为38 ℃时(水的蒸发忽略不计),不可能出现的情况是
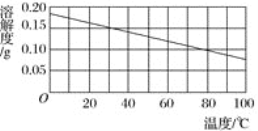
A. 溶液变浑浊
B. 溶液变为不饱和
C. 溶液质量变小
D. 溶质质量分数变小
难度: 中等查看答案及解析
-
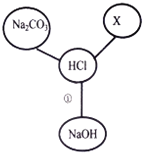
下列各组变化中,每一转化在一定条件下均能一步实现的是( )


A. ①③
B. ①③④
C. ②③④
D. ①②③④
难度: 中等查看答案及解析
-
地壳中含量最多的金属元素与非金属元素组成的化合物的化学式为( )
A. SiO2
B. FeO
C. Fe3O4
D. Al2O3
难度: 简单查看答案及解析