-
“电子垃圾”中含有金属铜和少量贵金属金、银等,直接废弃将严重污染环境且造成金属资源浪费。社会实践小组为回收这些金属,设计了以下操作步骤:
①分拆、灼烧:把废弃电子产品分拆后灼烧,将部分金属转化为氧化物;
②酸洗:用硝酸溶解灼烧得到的混合物,过滤,收集残渣中的金;
③回收:利用合适的金属提炼出滤液中的铜和银。
为达到分别提炼金属铜、银的目的,下列方案合理的是
A. 用金属铁同时提炼出铜和银
B. 先用金属铜提炼出银,再用金属铁提炼出铜
C. 用金属铁提炼出金属铜
D. 用金属铜提炼出金属银
难度: 简单查看答案及解析
-
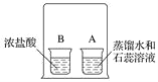
下列各组常见的固体物质中,用水不能区分的是( )
A.NaOH和NH4NO3
B.CuSO4和Na2SO4
C.Na2CO3和CaCO3
D.NaCl和KCl
难度: 困难查看答案及解析
-
下列说法中正确的是
A.食用“地沟油”对人体有害
B.煤、石油、天然气都属于可再生能源
C.为保障食品安全,杜绝使用任何食品添加剂
D.为提高农作物产量,应大量施用化肥
难度: 中等查看答案及解析
-
下列与化学有关的知识内容完全正确的一组是( )
A
①食品包装填充氮气——防止变质、变形
②食品包装放入生石灰——防止受潮
③鉴别硝酸铵和硫酸铵——加熟石灰研磨,闻气味
B
①H2、CH4都是可燃气体——点燃前须检验纯度
②吃水果、蔬菜——可以补充维生素
③墙内开花墙外香——分子不断运动
C
①硬水和软水——加肥皂水可以区分
②有腐蚀性的药液溅入眼睛内——要立即用水冲洗,切不可用手揉搓。
③ClO2中氯元素的化合价——1价
D
①少用塑料购物袋——有利于减少“白色污染”
②随时用水冲洗铁制品——防止铁生锈
③水污染——对人类没有影响
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
有关溶液的说法正确的是( )
A. 具有均一性、稳定性的液体一定是溶液
B. 配制溶液时,搅拌可以增大固体溶质的溶解度
C. 饱和溶液的浓度一定比不饱和溶液的浓度大
D. 配制氢氧化钠溶液时,必须将氢氧化钠固体放在玻璃器皿中称量
难度: 简单查看答案及解析
-
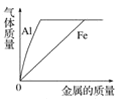
下列曲线正确的是( )
A. 向等体积、等浓度的稀盐酸中加金属

B. 向稀硝酸中加水

C. 双氧水分解

D. 向等体积、等浓度的稀盐酸中加金属
难度: 简单查看答案及解析
-
某种新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属丝,当玻璃被击碎时,产生电信号,与金属丝相连的警报系统就会立即报警,这是利用了金属的( )
A. 延展性
B. 导电性
C. 导热性
D. 可燃性
难度: 简单查看答案及解析
-
生活中的下列物品,主要材料属于合成材料的是
A. 全棉毛巾 B. 塑料袋 C. 不锈钢盆 D. 青花瓷瓶
难度: 简单查看答案及解析
-
厨房中下列用品所使用的主要材料属于有机合成材料的是( )
A.菜刀 B.瓷碗 C.塑料盆 D.木制面板
难度: 简单查看答案及解析
-
下列各组固体物质,只用水和组内物质就可相互鉴别的一组是
A. FeCl3、Na2SO4、NaOH、AgNO3
B. CaCO3、Na2CO3、K2CO3、BaCl2
C. NaOH、KNO3、CuSO4、NaNO3
D. BaCl2、CuSO4、MgCl2、NaCl
难度: 中等查看答案及解析
-
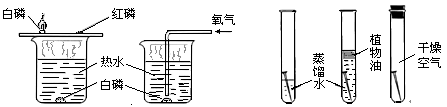
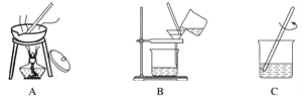
控制变量法是实验探究的重要方法,下图是两个常见实验,说法不正确的是( )

A. 甲中①③对比,可探究铁生锈是否与水有关
B. 甲中①②对比,可探究铁生锈是否与氧气有关
C. 乙中水中白磷不燃烧是因为没有接触氧气
D. 乙中红磷不燃烧是因为红磷没有可燃性
难度: 简单查看答案及解析
-
下图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )

A.20℃时,100g甲溶液中含甲物质的质量小于25g
B.20℃时,等质量甲、乙饱和溶液中含溶质的质量相等
C.30℃时,甲物质的溶解度大于乙物质的溶解度
D.50℃时,将甲、乙两种物质的饱和溶液分别降温至20℃,析出晶体的质量甲大于乙
难度: 困难查看答案及解析
-
生活中废弃的铝制易拉罐、破铁锅、废铜线等可归为一类加以回收,它们属于
A. 化合物
B. 金属或合金
C. 氧化物
D. 非金属
难度: 中等查看答案及解析
-
“吃去健康,吃出营养“是人们普遍的饮食追求,下列说法不正确的是
A.过多摄入微量元素不利于健康 B.糖类是人体能量的重要来源
C.每天都要摄入一定量的蛋白质 D.油脂会使人发胖,故禁食油脂
难度: 简单查看答案及解析
-
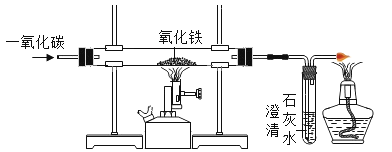
下列化学观点正确的是( )
A. 气球吹爆是化学变化
B. KClO3中氯元素的化合价为+1
C. 一氧化碳与氧化铁反应属于置换反应
D. 磁铁矿主要成分是Fe3O4
难度: 简单查看答案及解析
-
在某无色溶液中能大量共存的是
A. K+、Cu2+、NO3-、SO42-
B. Na+、H+、CO32-、NO3-
C. Ba2+、NH4+、OH-、SO42-
D. Ba2+、K+、NO3-、OH-
难度: 中等查看答案及解析
-
据悉,英国海军建造了一种反水雷的“塑料战舰”,舰身材料是一种强化塑料。则该塑料
A. 属于天然高分子材料 B. 一定是导电塑料
C. 具有热塑性 D. 是一种具有特殊功能的合成材料
难度: 中等查看答案及解析
-
室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如右下图所示。下列有关说法不正确的是
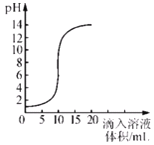
A. 该图像表示的是将氢氧化钠溶液滴入盐酸中
B. 氢氧化钠溶液和盐酸恰好完全反应时。溶液的pH等于7
C. 当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D. 滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
难度: 困难查看答案及解析
-
为创建“国家环保模范城市”,今年某市将原来的垃圾桶撤换成分类型垃圾收集箱。下图是国家颁布的“城市生活垃圾分类标志”。废旧电池投入的垃圾收集箱上应贴有的标志是( )
A.

B.

C.

D.

难度: 中等查看答案及解析
-
下列说法中正确的是
A. 在测定空气中氧气含量的实验里,红磷可以用木炭代替
B. 合金的熔点要比组成它的纯金属的熔点低
C. 电解水生成氢气和氧气,说明水是由氢气和氧气组成的
D. 一氧化碳还原氧化铜时,先加热氧化铜粉末至红热,后通入一氧化碳气体
难度: 简单查看答案及解析