-
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A. 1mol/L的NaCl溶液中含有的离子总数为2NA
B. 1 mol Na2O2与CO2完全反应时转移电子数为2NA
C. 标准状况下,22.4LH2O含有的 H—O键数为2NA
D. 18g 18O2中含有的中子数为10NA
难度: 中等查看答案及解析
-
在下列条件的水溶液中可以大量共存的粒子组是( )
A. 使酚酞变红的溶液中:Na+、HCO3-、Cl-、NO3-
B. 含大量H+的溶液中:Na+、K+、NO3-、AlO2-
C. 无色溶液中:SO42-、Cl-、Al3+、NH4+
D. 含大量Fe3+的溶液:Na+、Mg2+、NO3-、I-
难度: 中等查看答案及解析
-
已知短周期元素的四种离子 A2+、 B+、 C3-、 D-具有相同的电子层结构,则下列叙述中正确的是 ( )
A. 原子序数: D>C>B>A B. 离子半径: C3->D->A2+>B+
C. 原子半径: B>A>C>D D. 氧化性: A2+>B+,还原性: C3-<D-
难度: 中等查看答案及解析
-
化学与生活密切相关,下列说法正确的是( )
A. 光伏电池板的主要成分是二氧化硅
B. 导致酸雨的主要物质有SO2、NO2和CO2等
C. 食品包装袋中的铁粉包是为了防止食品氧化而变质
D. 包装食品的保鲜膜最好选用PVC(聚氯乙烯)材质的保鲜膜
难度: 简单查看答案及解析
-
下列有关化学用语表达不正确的是( )
A. 甲烷的结构式:CH4 B. 质子数为 53,中子数为 78 的碘原子:
C. Na 的原子结构示意图:
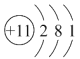 D. 钙离子的电子式: Ca2+
D. 钙离子的电子式: Ca2+难度: 简单查看答案及解析
-
下列物质分类正确的是( )
A. SiO2、NO2均为酸性氧化物 B. 稀豆浆、淀粉溶液均为胶体
C. 烧碱、乙醇均为电解质 D. 水玻璃、冰醋酸均为混合物
难度: 简单查看答案及解析
-
下列有关物质性质的应用正确的是
A.氯化铝是一种电解质,可用于电解法制铝
B.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸
C.生石灰能与水反应,可用来干燥氯气
D.液氨汽化时要吸收大量的热,可用作制冷剂
难度: 中等查看答案及解析
-
有关基本营养物质说法正确的是( )
A. 淀粉和纤维素互为同分异构体 B. 鸡蛋白滴加浓硝酸变黄色
C. 糖类、油脂、蛋白质都能发生水解反应 D. 木材、稻草、蚕丝主要成分都是纤维素
难度: 简单查看答案及解析
-
下列有关物质变化的说法不正确的是( )
A. 石油的分馏和裂化都是化学变化 B. 硝化反应和酯化反应都属于取代反应
C. 煤的液化和气化都是化学变化 D. 乙烯与溴水反应和苯与H2反应都属于加成反应
难度: 简单查看答案及解析
-
已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )
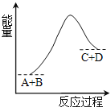
A. 反应物的总能量高于生成物的总能量
B. 该反应为放热反应
C. 该反应在常温下也有可能进行
D. 若此反应过程中有电子转移,可设计成原电池
难度: 简单查看答案及解析
-
下列表示对应化学反应的离子方程式不正确的是( )
A. 向Al2(SO4)3溶液中加入过量氨水:Al3++ 3NH3·H2O=Al(OH)3↓+ 3NH4+
B. Cl2与H2O反应:Cl2+H2O=2H++ClO-+Cl-
C. 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O
D. 碳酸氢钙溶液中加入足量烧碱溶液:Ca2+ +2HCO3-+2OH-=CaCO3 ↓+CO32- +2H2O
难度: 简单查看答案及解析
-
在2A(g)+B(g)=3C(g)+4D(g)中,表示该反应速率最快的是( )
A. v(A)=0.5mol•L﹣1.mim﹣1
B. v(B)=0.3mol•L﹣1.mim﹣1
C. v(C)=0.8mol•L﹣1.mim﹣1
D. v(D)=1.0mol•L﹣1.mim﹣1
难度: 中等查看答案及解析
-
五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同主族,B和D同主族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的气态化合物在水中呈碱性,C和E形成化合物CE。下列说法不正确的是( )
A. B离子的半径大于C离子的半径
B. 将C的单质放入CuSO4溶液中会有蓝色沉淀产生
C. E的最高价氧化物对应水化物的化学式为HEO4
D. 稳定性BA3>DA3>AE
难度: 简单查看答案及解析
-
下图是铅蓄电池构造示意图,下列说法不正确的是( )

A. 铅蓄电池是二次电池,充电时电能转化为化学能
B. 电池工作时,电子由Pb板通过导线流向PbO2板
C. 电池工作时,负极反应为:Pb-2e-+SO42-=PbSO4
D. 电池工作时,H+移向Pb板
难度: 简单查看答案及解析
-
下列说法中,错误的是( )
A. 化学反应必然伴随发生能量变化
B. 石灰石生成生石灰伴随的能量变化主要是化学能转化为热能
C. 化学变化中的能量变化主要是由化学键变化引起的
D. 化学反应中能量变化的大小与反应物的状态有关
难度: 简单查看答案及解析
-
下列有关实验操作和现象、结论都正确的是( )
选项
实验操作和现象
实验结论
A
向某盐溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝
该溶液中一定含有NH4+
B
向某溶液中加入盐酸酸化的氯化钡溶液,产生白色沉淀
该溶液中一定含有SO42-
C
将盐酸滴入碳酸钠溶液中,产生气泡
非金属性:Cl>C
D
常温下,将大小、形状相同的锌和铝分别加入到等体积98%的浓硫酸中,观察到前者反应速率快
锌比铝活泼
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。某课外兴趣小组对X进行如下实验探究:

下列说法正确的是( )
A. 12.8g固体可能为Fe2O3 B. 混合物X的成分为Al2O3、Fe2O3、Cu、SiO2
C. Fe2O3、Cu的物质的量之比为1:1 D. m>24.8
难度: 中等查看答案及解析
-
关于下列图像的说法不正确的是( )
选项
横轴x
纵轴y
图像
A
烷烃分子中的碳原子数
碳的质量分数,y的最小值等于75%
B
温度
食物腐败变质速度
C
碱金属元素原子序数
碱金属单质熔沸点
D
卤素原子序数
卤素阴离子(X-)半径
A. A B. B C. C D. D
难度: 简单查看答案及解析