-
推理是化学学习中常用的思维方法,下面推理中正确的是 ( )
A. 酸中都有氢元素,所以含有氢元素的化合物一定是酸
B. 碱性溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性
C. 酸与碱反应有盐和水生成,因此有盐和水生成的反应一定是中和反应
D. 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
难度: 中等查看答案及解析
-
下列说法中,正确的是( )
A. 任何原子都是由质子、中子、电子构成的
B. 原子是由不带电的粒子构成的
C. 相对原子质量就是原子的质量
D. 原子是不停地运动着的
难度: 中等查看答案及解析
-
下列客观事实的微观解释正确的是( )
选项
客观事实
微观解释
A
红墨水在热水中扩散比在冷水中快
水分子间有空隙
B
H2O在通电条件下产生H2
H2O分子中有H2
C
橡皮容易被压形变
分子间存在斥力
D
NaCl溶液能导电
溶液中存在自由移动的Na+、Cl﹣
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
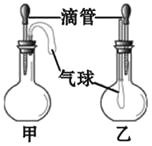
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是( )
甲
乙
A.
稀硫酸和铜片
水和硝酸铵固体
B.
水和氢氧化钠固体
AgNO3溶液和稀盐酸
C.
双氧水和MnO2
NaOH溶液和CO2
D.
Na2CO3溶液和稀硫酸
水和浓硫酸
A. A B. B C. C D. D
难度: 中等查看答案及解析