-
配制100 mL 0.1 mol·L-1Na2CO3溶液,下列操作正确的是( )
A. 称取1.06 g无水碳酸钠,加入100 mL容量瓶中,加水溶解、定容
B. 称取1.06 g无水碳酸钠,加入100 mL蒸馏水,搅拌、溶解
C. 转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中
D. 定容后,塞好瓶塞,反复倒转,摇匀
难度: 中等查看答案及解析
-
用NA表示阿伏伽德罗常数的值,下列叙述正确的是
A. 标准状况下,33.6 L HF中含有氟原子的数目为1.5NA
B. 常温常压下16 g O3和O2混合物中氧原子数为NA
C. pH=1的H3PO4溶液中,含有0.1NA个H+
D. 0.1 mol H2O2分子中含极性共价键数目为0.3 NA
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A. 硅晶体中,有NA个Si就有2NA个Si-Si键
B. 常温常压下,等物质的量浓度的Na2CO3与Na2S溶液中Na+数目相等
C. 惰性电极电解食盐水,若线路中通过2NA个电子的电量时,则阳极产生气体22.4 L
D. 1molNa2O2与足量CO2充分反应,转移的电子数为2 NA
难度: 困难查看答案及解析
-
下列实验中,①pH试纸的使用,②过滤,③蒸发,④配制一定物质的量浓度溶液,均用到的仪器是
A. 蒸发皿 B. 玻璃棒 C. 试管 D. 分液漏斗
难度: 简单查看答案及解析
-
在溶液的配制过程中会引起浓度偏高的是
①用1 g 98%的浓硫酸加4 g水配制成19.6%的硫酸 ②配制一定物质的量浓度的硫酸溶液时,定容后,塞好塞子倒转摇匀后,发现液面低于刻度线 ③10%的硫酸和90%的硫酸等体积混合配制50%的硫酸溶液 ④向80 mL水中加入18.4 mol·L-1硫酸20 mL,配制3.68 mol·L-1的硫酸溶液 ⑤质量分数为5x%和x%的两种氨水等体积混合配制成3x%的氨水
A. ①③⑤ B. ②④⑤ C. ③④ D. ④⑤
难度: 中等查看答案及解析
-
下列除去杂质的操作中不正确的是( )
A. CuO中混有Al2O3:加入过量烧碱溶液充分反应后过滤
B. FeCl2溶液中混有CuCl2:加入过量铁粉充分反应后过滤
C. Na2CO3固体中混有少量NaHCO3:加入过量NaOH溶液,反应后加热蒸干
D. 氯气中混有少量氯化氢气体:将混合气体通过盛饱和食盐水的洗气瓶
难度: 中等查看答案及解析
-
C和CuO在一定温度下反应,产物有Cu、Cu2O、CO、CO2。若将2.00 g C跟16.0 g CuO混合,隔绝空气加热,将生成的气体全部通过足量的澄清石灰水,反应一段时间后共收集到1.12 L气体(标准状况),生成沉淀的质量为5.00 g。下列说法错误的是
A. 反应后的固体混合物中还含有碳
B. 反应后的固体混合物中氧化物的物质的量为0.05 mol
C. 反应后的固体混合物中Cu的质量为12.8 g
D. 反应后的固体混合物总质量为14.4 g
难度: 中等查看答案及解析
-
下列各图所示装置的气密性检查中,一定漏气的是 ( )
A.
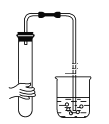 B.
B. 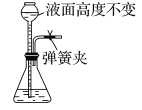 C.
C. 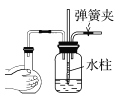 D.
D. 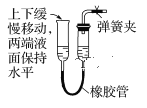
难度: 中等查看答案及解析
-
下列实验操作不能达到目的是( )
A. 除去MgCl2酸性溶液中的Fe3+:加热搅拌,加入MgCO3,过滤,加适量的盐酸
B. 制备Fe(OH)3胶体:向饱和FeCl3溶液中滴加少量NaOH溶液
C. 检验Fe2(SO4)3溶液中是否含有FeSO4:滴加少许酸性高锰酸钾溶液,并振荡
D. 使盛有少量氢氧化镁沉淀的试管中的沉淀溶【解析】
加入一定量的氯化铵溶液难度: 中等查看答案及解析
-
如图是某学校购买的硫酸试剂标签上的部分内容。据此下列说法正确的是

A. 该硫酸的物质的量浓度为1.84mol·L−1
B. 1mol Zn与足量的该硫酸反应产生2g H2
C. 配制200mL4.6mol·L−1的稀硫酸需取该硫酸50mL
D. 该硫酸与等体积的水混合所得溶液的物质的量浓度等于9.2mol·L−1
难度: 中等查看答案及解析
-
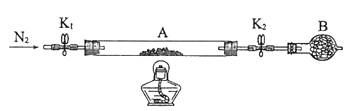
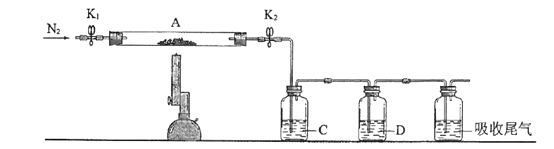
下图所示实验装置用于测定气体摩尔体积,相关叙述正确的是
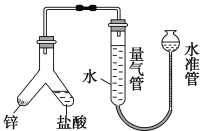
A. 用CCl4代替水,测得氢气的体积更准确
B. 量气管压入漏斗的水过多而溢出,会导致测定失败
C. 必须待体系温度降低到0 ℃时才可进行读数
D. 上提水准管,量气管液面高度不断改变,说明装置漏气
难度: 中等查看答案及解析
-
某温度下,物质X2SO4的饱和溶液密度为ρg·mL-1,c(X+)= c mol·L-1,溶质的质量分数为a%,溶质的摩尔质量为Mg·mol-1,溶解度为S g,下列表达式正确的是
A. c=
B.
C.
D.
难度: 中等查看答案及解析
-
塑化剂是一种对人体有害的物质。增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得:
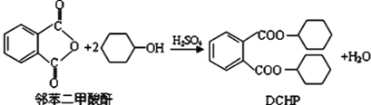
下列说法正确的是
A. DCHP的分子式为C20H24O4
B. 环己醇分子的核磁共振氢谱有4个吸收峰
C. DCHP能发生加成反应和取代反应,不能发生酯化反应
D. 1mol DCHP可与4mol NaOH完全反应
难度: 中等查看答案及解析
-
《Chem.sci.》报道麻生明院士团队合成非天然活性化合物
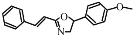 (b)的新方法。下列说法不正确的是
(b)的新方法。下列说法不正确的是A. b的分子式为C18H17NO2 B. b的一氯代物有9种
C. b可发生取代反应 D. b可使酸性高锰酸钾溶液褪色
难度: 中等查看答案及解析
-
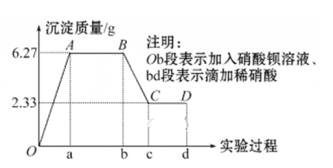
某溶液由Na+、Cu2+、Ba2+、Fe3+、AlO
、CO
、SO
、Cl中的若干种离子组成,取适量该溶液进行如下实验:下列说法正确的是
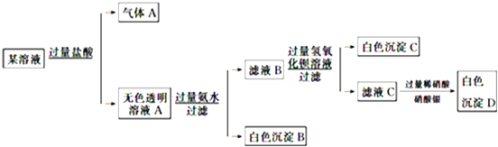
A. 原溶液中一定只存在
、
、
、Cl-四种离子
B. 气体A的化学式是CO2,其电子式为O::C::O
C. 原溶液中一定不存在的离子是Cu2+、Ba2+、Fe3+
D. 生成沉淀B的离子方程式为:Al3++3OH===Al(OH)3↓
难度: 中等查看答案及解析
 ]是一种医药中间体,它的一种合成路线如下:
]是一种医药中间体,它的一种合成路线如下:
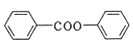 )的合成路线(其它试剂任选)___________。
)的合成路线(其它试剂任选)___________。