-
地壳中含量最多的金属元素,非金属元素和空气中含量最多的元素组成的化合物是
A. Al(NO3)3 B. CaCO3 C. Al2(SO4)3 D. Fe(NO3)3
难度: 中等查看答案及解析
-
化学在生产、生活中应用广泛。下列过程属于化学变化的是( )
A. 海水晒盐 B. 石油分馏 C. 煤制煤气 D. 干冰制冷
难度: 简单查看答案及解析
-
黄河鲤鱼是豫菜常用食材,下列和鱼肉中富含的主要营养素相同的是( )
A. 奶油蛋糕 B. 玉米窝头 C. 凉拌黄瓜 D. 卤水豆腐
难度: 简单查看答案及解析
-
分类法是化学研究的重要方法.以下分类不正确的是( )
A. 合金:生铁、青铜、硬铝
B. 氧化物:水、二氧化锰、五氧化二磷
C. 碱:纯碱,生石灰水,苛性钠
D. 合成材料:塑料,合成橡胶,合成纤维
难度: 简单查看答案及解析
-
构成下列物质的微粒与构成干冰的微粒种类相同的是( )
A. 铜 B. 氨气 C. 金刚石 D. 氯化钠
难度: 简单查看答案及解析
-
下列有关水的说法正确的是( )
A. 澄清洁净的矿泉水是纯水
B. 填埋垃圾不会导致水体污染
C. 将硬水过滤可以得到软水
D. 肥皂水可以区别硬水和软水
难度: 简单查看答案及解析
-
下列实验操作不正确的是( )
A. 闻气味
 B. 倾倒液体
B. 倾倒液体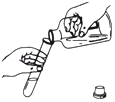
C. 测溶液的pH
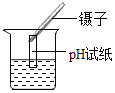 D. 稀释浓硫酸
D. 稀释浓硫酸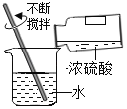
难度: 简单查看答案及解析
-
硒有防癌、抗癌作用。如图为硒的原子结构示意图,下列说法不正确的是( )
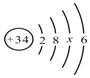
A. 图中x的值为18 B. 硒原子的核电荷数为34
C. 硒元素位于第四周期 D. 硒是人体必需常量元素
难度: 简单查看答案及解析
-
下列是对初中化学中“三”的总结,不完全正确的一组是( )
A. 构成物质的三种微粒:原子、分子、离子
B. 灭火的三种方法:隔绝氧气、降低着火点、清除或隔离可燃物
C. 常见的三种防锈措施:保持洁净和干燥、表面覆盖保护层、改变金属内部结构
D. 清除污垢常涉及三种原理:乳化(如洗涤剂)、溶解(如干洗剂)、化学反应(如酸液除锈)
难度: 简单查看答案及解析
-
下列变化过程不属于金属冶炼的是( )
A. 电解氧化铝
B. 铁在氧气中燃烧
C. 焦炭与氧化铜在高温下反应
D. 高温下一氧化碳与氧化铁反应
难度: 简单查看答案及解析
-
下列离子组合能在pH=12的溶液中大量共存的是( )
A. K+、Cu2+、SO42﹣、Cl﹣ B. K+、Na+、NO3﹣、Cl﹣
C. CO32﹣、H+、Na+、Cl﹣ D. Ba2+、Cl﹣、Na+、SO42﹣
难度: 困难查看答案及解析
-
一定条件下,a,b,c,d四种物质在密闭容器中发生反应,测得反应前后各物质的质量如下表所示,下列有关说法中不正确的是( )
物质
a
b
c
d
反应前的质量/g
30
20
10
15
反应后的质量/g
x
y
0
10
A. 参加反应的c与d的质量比为2:1
B. x+y=65
C. 当y≤20时,该反应一定是化合反应
D. x的取值范围:0≤x≤30
难度: 简单查看答案及解析
-
取镁、碳酸镁组成的固体混合物20.4g,放入325g稀硫酸中,恰好完全反应,得到5.4g气体和溶质质量分数为20%的溶液,则原固体混合物中镁元素的质量为( )
A. 4.8g B. 9.6g C. 13.6g D. 16.8g
难度: 中等查看答案及解析