-
化学与能源、环境、生产、生活关系密切,下列说法中不正确的是
A.环保快餐饭盒的材料可用“玉米塑料”(主要成分为聚乳酸)制成
B.缺铁性贫血在我国居民中普遍存在,可在酱油中添加三价铁盐予以改善
C.松花蛋是一种常见食物,但食用时有氨的气味,可以蘸些食醋除去
D.世博停车场安装催化光解设施,可将汽车尾气中CO和NOx转化为无毒气体
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.标准状况下,18 g 2H2O中所含的中子总数为10NA
B.标准状况下,11.2 L O2反应转移的电子数一定为2NA
C. 常温下, 1.0L 0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA
D.室温下,16g甲烷含有共价键数为2NA
难度: 中等查看答案及解析
-
X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是
A.由mXa+与nYb-,得m+a=n-b
B.X2-的还原性一定大于Y-
C.X,Y一定不是同周期的金属元素
D.若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY
难度: 中等查看答案及解析
-
下列叙述不正确的是
A.天然气和沼气的主要成分都是甲烷
B.葡萄糖和蔗糖都含有C、H、O三种元素,但不是同分异构体
C.纤维素乙酸酯、油脂和蛋白质在一定条件下都能水解
D.乙醇和乙酸能发生酯化反应,只要一种反应物过量酯化反应就能进行彻底
难度: 中等查看答案及解析
-
下列叙述正确的是
A.Na2O2、Cl2、NO2均能与水发生氧化还原反应
B.在加热的条件下稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
C.Cu、Fe、C分别在氧气中燃烧都只能生成一种氧化物
D. NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
难度: 中等查看答案及解析
-
现有等体积的Ba(OH)2、NaOH和NH3·H2O三种溶液,将它们分别与V1 L、V2 L、V3 L等浓度的盐酸混合,下列说法中正确的是
A.若混合前三溶液pH相等,将它们同等倍数稀释后,NaOH溶液pH最大
B.若混合前三溶液pH相等,酸碱恰好完全反应,则V1>V2>V3
C.若混合前三溶液物质的量浓度相等,酸碱恰好完全反应,则V1>V2>V3
D.若混合前三溶液物质的量浓度相等,混合后溶液呈中性,则V1>V2>V3
难度: 中等查看答案及解析
-
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mLpH=14的溶液,然后用1mol·L-1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是
A.原合金质量为0.92g
B.产生氢气的体积为896mL(标准状况下)
C.图中m的值为1.56
D.图中V2为60
难度: 中等查看答案及解析
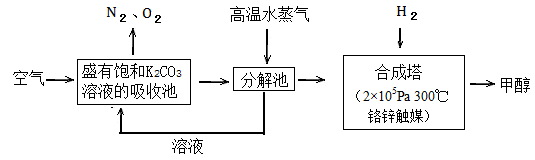
 (1)B的同素异形体的名称为_________________;F的化学式为__________________________。
(1)B的同素异形体的名称为_________________;F的化学式为__________________________。