-
下列物品主要由合金制成的是
A.塑料水杯 B.单车轮胎 C.羊毛衣服 D.青铜雕像
难度: 中等查看答案及解析
-
随着世界人口的增长, 人类对农产品的需求量增大,化肥对农作物的增产已成为最有力的措施。现有一包化肥,可能是碳酸氢铵、硫酸铵、磷矿粉、氯化钾中的一种,取少量样品,观察到外观为白色固体,加水后能全部溶解;另取少量样品与熟石灰混合研磨,没有刺激性气体放出,这包化肥是( )
A.碳酸氢铵 B.氯化钾 C.硫酸铵 D.磷矿粉
难度: 中等查看答案及解析
-
在高速发展的信息时代,我们要学会获取和辨别信息,下列信息中正确的是
A. 为了提高粮食产量,应大量使用农药、化肥
B. 用甲醛水溶液浸泡海鲜产品来延长食品保质期
C. 锌元素有“智力之花”美称,补锌口服液喝得越多越好
D. 塑料薄膜可用于大棚蔬菜,同时也会造成“白色污染”
难度: 中等查看答案及解析
-
检验碳酸盐的正确方法是( )
A. 滴加盐酸,产生使木条火焰熄灭的气体
B. 滴加BaCl2溶液产生白色沉淀
C. 加热,产生使澄清石灰水变浑浊的气体
D. 滴加稀盐酸产生使澄清石灰水变浑浊的气体
难度: 中等查看答案及解析
-
下列物质露置于空气中,一段时间后,质量增加的是
A. 大理石
B. 双氧水
C. 浓盐酸
D. 烧碱
难度: 简单查看答案及解析
-
利用化学知识对下列说法进行判断,其中正确的是( )
A. 咀嚼米饭时会出现甜味,这一过程属于物理变化
B. 绿色植物合成葡萄糖的过程中将太阳能转化为化学能
C. 要提高澄清石灰水的溶质质量分数,可以升高该溶液的温度
D. 向鸡蛋清中加入饱和硫酸铵溶液出现白色沉淀,鸡蛋清中蛋白质失去了原有的生理功能
难度: 中等查看答案及解析
-
今年5月1日开始,醉酒驾驶机动车辆交被依法追究刑事责任。每100mL血液中酒精含量达到80mg时,即属于醉酒(血液的pH约为7.4),关于醉酒血液的说法正确的是( )
A. 该血液中的酒精的质量分数为80%
B. 该血液中酒精的溶解度是80
C. 该血液是酒精的饱和溶液
D. 该血液显碱性
难度: 中等查看答案及解析
-
向某盐酸中逐滴加入氢氧化钠溶液,所得溶液的pH与加入氢氧化钠溶液的质量关系曲线图合理的是( )
A.

B.
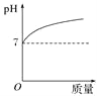
C.

D.

难度: 中等查看答案及解析
-
实验室配制50 g溶质质量分数为6%的NaCl溶液的操作步骤有计算、称量、量取、溶解。该实验过程中不需要用到的仪器是
A.
玻璃棒
B.
烧杯
C.
漏斗
D.
量筒
难度: 简单查看答案及解析
-
下列物质为纯净物的是( )
A. 黄铁矿
B. 菱铁矿
C. 不锈钢
D. 含氧质量分数为30%的氧化铁
难度: 简单查看答案及解析
-
以下是初中化学的一些基本实验,其中不能达到相应的实验目的的是( )
A. 测定空气中O2的含量
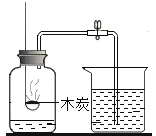
B. 稀释浓硫酸
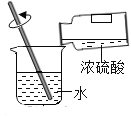
C. 铁丝在空气中的变化
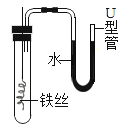
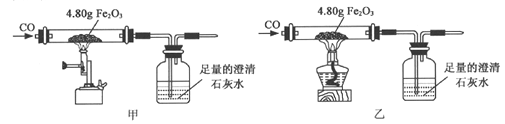
D. 一氧化碳还原氧化铁
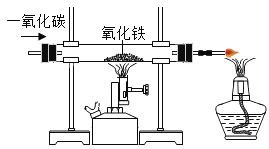
难度: 简单查看答案及解析
-
科技文献中经常出现下列词汇,其中与相关物质的颜色并无联系的是( )
A. 赤色海潮
B. 绿色食品
C. 白色污染
D. 棕色烟气
难度: 简单查看答案及解析
-
下列化学方程式中属于复分解反应的是( )
A. C+O2
CO2 B. 2H2O
2H2↑+O2↑
C. 3CO+Fe2O3
2Fe+3CO2 D. HCl+AgNO3=AgCl↓+HNO3
难度: 中等查看答案及解析
-
2015年4月10日,南京工业大学科研团队,在有机合成材料中成功观察到“长余辉”现象.并研制出纯有机的“夜明珠”.下列物品所用主要材料属于有机合成材料的是
A.不锈钢汤勺 B.塑料玩具 C.羊毛围巾 D.纯棉T桖
难度: 中等查看答案及解析
-
(2分)下列生活用品所使用的主要材料属于有机合成材料的是( )




A.纯棉毛巾 B.塑料保鲜膜 C.真丝围巾 D.不锈钢锅
难度: 中等查看答案及解析
-
某同学想用pH试纸测定一些物质的pH,下列做法能达到实验目的的是( )
A. 用湿润的pH试纸测定稀硫酸的pH
B. 用干燥的pH试纸测定二氧化碳气体的pH
C. 用干燥的pH试纸测定浓硫酸的pH
D. 用干燥的pH试纸测定氢氧化钠稀溶液的pH
难度: 中等查看答案及解析
-
小瑾同学用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁。下列关系错误的是( )
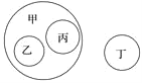
甲
乙
丙
丁
A
碱
烧碱
氢氧化钾
纯碱
B
合成材料
塑料
合成纤维
合成橡胶
C
溶液
糖水
生理盐水
泥浆
D
化石燃料
石油
煤
酒精
A. A
B. B
C. C
D. D
难度: 中等查看答案及解析
-
某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和酸碱指示剂进行实验的过程见下图。下图所加试剂①②③分别是( )

A. 稀NaOH溶液、石蕊溶液、稀盐酸
B. 稀盐酸、石蕊溶液、稀NaOH溶液
C. 稀NaOH溶液、酚酞溶液、稀盐酸
D. 稀盐酸、酚酞溶液、稀NaOH溶液
难度: 中等查看答案及解析
-
质量相等的金属镁和铝分别加入质量相等、溶质质量分数相等的两份稀硫酸中,反应完毕后,金属均有剩余。则反应两种溶液质量关系是( )
A. 相等
B. 镁反应后的溶液质量大
C. 铝反应后的气体质量大
D. 无法比较
难度: 简单查看答案及解析
-
“浸土选种”是现代农业生产常用的科学方法,取武当山特区某村土壤浸出的溶液,加入无色酚酞溶液后显红色。下表为四种农作物适宜生长的pH范围,你认为该村土壤比较适宜种植的农作物是( )
农作物
水稻
茶树
玉米
马铃薯
pH
6.0~7.0
6.0~7.0
7.0~8.1
4.8~5.5
A. 玉米
B. 茶树
C. 水稻
D. 马铃薯
难度: 中等查看答案及解析