-
金属镍有广泛的用途。粗镍中含少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是
A. 阳极发生还原反应,其电极反应式:Ni2++2e-===Ni
B. 电解过程中,阳极质量的减少与阴极质量的增加相等
C. 电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D. 电解后,电解槽底部的阳极泥中只有Cu和Pt
难度: 中等查看答案及解析
-
将AsO43-+2I-+2H+
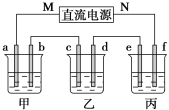
AsO33-+I2+H2O设计成图所示的电化学装置,其中C1、C2均为碳棒。甲、乙两组同学分别进行下述操作:
甲组:向B烧杯中逐滴加入浓盐酸
乙组:向B烧杯中逐置滴加入40%NaOH溶液,下列描述中,正确的是

A. 甲组操作过程中,C2做负极
B. 乙组操作过程中,C1上发生的电极反应为: 2I—-2e—=I2
C. 两次操作过程中,微安表(G)指针的偏转方向相反
D. 甲组操作时该装置为原电池,乙组操作时该装置为电解池
难度: 中等查看答案及解析
-
某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池反应为:Li+LiMn2O4==Li2Mn2O4。下列说法正确的是
A. 放电时,LiMn2O4发生氧化反应,电池内部Li+向正极移动
B. 放电时,正极反应为:Li++LiMn2O4+e-==Li2Mn2O4
C. 羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D. 充电时,锂的碳材料为阳极且反应为:Li++e-==Li
难度: 中等查看答案及解析
-
将铁粉和硫粉混合后加热,待反应一发生即停止加热,反应仍可持续进行,直至反应完全生成新物质硫化亚铁。这现象说明了
A. 该反应是吸热反应
B. 该反应是放热反应
C. 铁粉和硫粉在常温下可以发生反应
D. 硫化亚铁的总能量高于铁粉和硫粉的总能量
难度: 简单查看答案及解析
-
已知1molSiO2含有4mol Si—O。有关键能数据如表,晶体硅在氧气中燃烧的热化学方程式:Si(s)+O2(g)=SiO2(s);ΔH=-989.2kJ·mol-1,则表中x的值为
化学键
Si—O
O=O
Si—Si
键能/kJ·mol-1
x
498.8
176
A. 460 B. 920 C. 1165.2 D. 423.3
难度: 简单查看答案及解析
-
合成氨工业中氢气可由天然气和水反应制备,其主要反应为:CH4(g)+ 2H2O(g)
CO2(g)+4H2(g) 已知,破坏1mol化学键需要吸收的热量如下表所示:
化学键
C—H
O—H
C=O
H—H
吸收热量(kJ/mol)
414
464
803
436
试通过计算判断,下列有关甲烷转化成氢气过程的能量变化示意图正确的是
A.
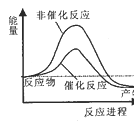 B.
B. 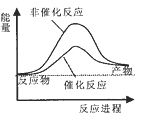 C. C
C. C D.
D. 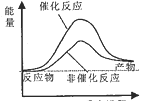
难度: 简单查看答案及解析
-
废电池的污染引起人们的广泛重视,废电池中对环境形成污染的主要物质是
A. 锌 B. 汞 C. 石墨 D. 二氧化锰
难度: 简单查看答案及解析
-
以下现象与电化腐蚀无关的是
A. 黄铜(铜锌合金)制作的铜锣不易产生铜绿
B. 生铁比软铁芯(几乎是纯铁)容易生锈
C. 铁质器件附有铜质配件,在接触处易生铁锈
D. 银质奖牌久置后表面变暗
难度: 简单查看答案及解析
-
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
A. 4Fe(OH)2+2H2O+O2===4Fe(OH)3↓
B. 2Fe+2H2O+O2===2Fe(OH)2↓
C. 2H2O+O2+4e-===4OH-
D. Fe-3e-===Fe3+
难度: 简单查看答案及解析
-
某学生欲完成2HCl+2Ag═2AgCl+H2↑反应,设计了下列四个实验,你认为可行的实验是

A. B. C. D.
难度: 中等查看答案及解析
-
利用电解法可将Fe、Zn、Ag、Au等杂质的粗铜提纯,下列叙述正确的是( )
A.电解时以纯铜作阳极
B.电解时阳极发生还原反应
C.纯铜连接电源负极,电极反应是Cu-2e- =Cu2+
D.电解后,电解槽底部会形成含少量Ag、Au等金属阳极泥
难度: 中等查看答案及解析
-
观察下列几个装置示意图,有关叙述正确的是

A. 装置①中阳极上析出红色固体
B. 装置②的待镀铁制品应与电源正极相连
C. 装置③中外电路电子由a极流向b极
D. 装置④的离子交换膜允许阳离子、阴离子、水分子自由通过
难度: 困难查看答案及解析
-
用惰性电极电解下列溶液,一段时间后,停止电解,向溶液中加入一定质量的另一种物质(括号内),能使溶液完全复原的是
A. CuCl2 (CuO) B. NaOH (NaOH) C. CuSO4 (CuO) D. NaCl (NaOH)
难度: 简单查看答案及解析
-
下列各个装置中能组成原电池的是
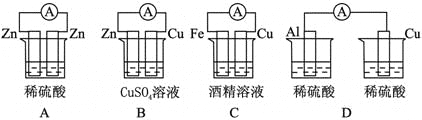
难度: 中等查看答案及解析
-
下图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是 ( )
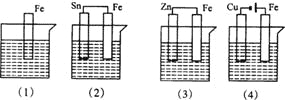
A. (4)>(2)>(1)>(3) B. (2)>(1)>(3)>(4)
C. (4)>(2)>(3)>(1) D. (3)>(2)>(4)>(1)
难度: 中等查看答案及解析
-
下列图示中关于铜电极的连接错误的是

A. A B. B C. C D. D
难度: 中等查看答案及解析
-
将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是

A. KNO3盐桥中的K+移向CuSO4溶液
B. Ag作负极,Cu作正极
C. 工作一段时间后,CuSO4溶液中c(Cu2+)增大
D. 取出盐桥后,电流计的指针依然发生偏转
难度: 中等查看答案及解析
-
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池说法正确的是
A. 电池的总反应是:2C4H10+13O2→8CO2+10H2O B. 在熔融电解质中,O2-由负极移向正极
C. 通入空气的一极是正极,电极反应为:O2 - 4e-==2 O2- D. 通入丁烷的—极是正极,电极反应为:C4H10+26e-+13O2-==4CO2+5H2O
难度: 中等查看答案及解析
-
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为: 2H2+O2=2H2O,下列有关说法错误的是
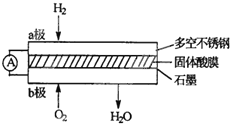
A. 电子通过外电路从a极流向b极
B. b极上的电极反应式为:O2+4H++4e-=2H2O
C. H+由b极通过固体酸电解质传递到a极
D. 每转移0.1 mol电子,标准状况下需消耗1.12 L的H2
难度: 中等查看答案及解析
-
结合如图判断,下列叙述正确的是

A. 图Ⅲ盐桥的原电池工作时,铜电极上发生氧化反应,CuSO4溶液蓝色变深
B. Ⅰ和Ⅱ中负极反应均是Fe﹣2e﹣═Fe2+
C. Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e﹣═4OH﹣
D. Ⅰ和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,Ⅱ有蓝色沉淀
难度: 中等查看答案及解析
-
在标准状况下,用铂电极电解CuSO4溶液,当阴极产生12.8g铜时,阳极放出的气体是
A. 1.12L H2 B. 1.12L O2 C. 2.24L H2 D. 2.24L O2
难度: 简单查看答案及解析
-
下列热化学方程式叙述正确的是(△H的绝对值均正确)
A. C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) △H=-1376.0kJ/mol(燃烧热)
B. NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=57.3kJ/mol(中和热)
C. 2S(s)+3O2(g)=2SO3(g) △H =-269KJ/mol(燃烧热)
D. 2NO2(g)=O2(g) + 2NO(g) △H=+116.2kJ/mol (反应热)
难度: 简单查看答案及解析
-
汽车的启动电源常用铅蓄电池,电池反应如下: PbO2 + Pb + 2H2SO4
2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
A. PbO2放电时是电池的负极,充电时是电池的阳极
B. 负极的电极反应式为:Pb + SO42—– 2e–=PbSO4
C. 放电时,PbO2得电子,被氧化
D. 电池放电时,溶液酸性增强
难度: 简单查看答案及解析
-
化学反应N2+3H2
2NH3的能量变化如图所示,该反应的热化学方程式是
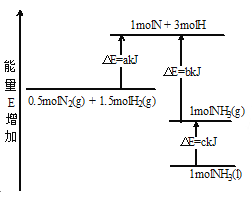
A. N2(g)+3H2(g)
2NH3(l) △H= 2(a﹣b﹣c)kJ/mol
B. N2(g)+3H2(g)
2NH3(g)△H=2(b﹣a)kJ/mol
C. 0.5N2(g)+1.5H2(g)
NH3(l)△H=(b+c﹣a)kJ/mol
D. 0.5N2(g)+1.5H2(g)
NH3(g)△H=(a+b)kJ/mol
难度: 中等查看答案及解析
-
下列依据热化学方程式得出的结论正确的是
A. 已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ· mol-1说明2 mol H2(g)和1 mol O2(g)的能量总和小于2 mol H2O(g)的能量
B. 已知C(s,石墨)===C(s,金刚石) ΔH>0,则金刚石比石墨稳定
C. 已知NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,则含20 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量
D. 已知2C(s)+2O2(g)===2CO2(g) ΔH1 2C(s)+O2(g)===2CO(g) ΔH2,则ΔH1>ΔH2
难度: 中等查看答案及解析
-
在1 200 ℃时,天然气脱硫工艺中会发生下列反应
H2S(g)+
O2(g)=SO2(g)+H2O(g) ΔH1
2H2S(g)+SO2(g)=
S2(g)+2H2O(g) ΔH2
H2S(g)+
O2(g)=S(g)+H2O(g) ΔH3
2S(g)=S2(g) ΔH4
则ΔH4的正确表达式为( )
A. ΔH4=
(ΔH1+ΔH2-3ΔH3) B. ΔH4=
(3ΔH3-ΔH1-ΔH2)
C. ΔH4=
(ΔH1+ΔH2-3ΔH3) D. ΔH4=
(ΔH1-ΔH2-3ΔH3)
难度: 中等查看答案及解析
-
某混合溶液中只含有两种溶质NaCl和H2SO4,且n(NaCl)︰n(H2SO4)=3︰1。若以石墨电极电解该溶液,下列推断中不正确的是
A. 阴极产物为H2
B. 阳极先析出Cl2,后析出O2
C. 电解液的pH不断增大,最终大于7
D. 整个电解的过程实质是电解水
难度: 中等查看答案及解析
-
如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是
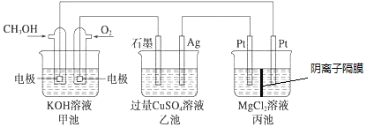
A. 甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B. 甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+
C. 反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使溶液恢复原浓度
D. 甲池中消耗4.48L(标准状况下)O2,此时丙池中理论上最多产生23.2 g固体
难度: 中等查看答案及解析
-
如图是Zn和Cu形成的原电池,下列描述合理的是
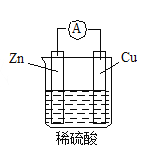
①Cu为阳极,Zn为阴极 ②Cu极上有气泡产生
③SO42-向Cu极移动 ④若有0.5 mol电子流经导线,则可产生0.25 mol气体
⑤电子的流向是:Cu→导线→Zn ⑥正极反应式:Cu+2e-=Cu2+
A. ①②③ B. ②④ C. ④⑤⑥ D. ③④⑤
难度: 简单查看答案及解析
-
用情性电极电解一定浓度的CuSO4溶液,通电—段时间后,向所得的溶液中加入19.6g Cu(OH)2后恰好恢复到电解前的浓度和pH。则下列说法正确的是
A. 电解过程中阴极没有气体生成 B. 电解过程中转移的电子的物质的量为0.6mol
C. 原CuSO4溶液的浓度为0.1 mol·L-1 D. 电解过程中阴、阳极共收集到气体体枳为8.96L(标准状况)
难度: 中等查看答案及解析