-
沃尔沃公司的斯蒂芬•沃尔曼发明了一种“三效催化转换器”,这种转换器可将汽车尾气中的有毒气体转化为无污染的气体,如图是其中一个反应过程的微观示意图,从图中可获得的信息是( )
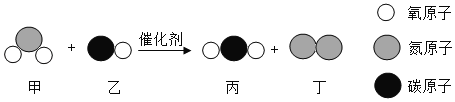
A. 有毒气体指的是N2
B. 无污染的气体是CO
C. 甲和丁中同种元素的化合价相等
D. 乙和丙中所含原子种类相同
难度: 简单查看答案及解析
-
玻璃导气管是科学实验中用途广泛的一个仪器,有关它的使用正确的是(省略夹持和加热装置)( )
A.
 排水法集气 B.
排水法集气 B. 向上排空气法集气
C.
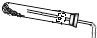 用高锰酸钾制氧气 D.
用高锰酸钾制氧气 D. 检验二氧化碳
难度: 简单查看答案及解析
-
1911年物理学家卢瑟福用束带正电的、质量比电子大得多的α粒子轰击金箔来探究原子的内部结构,根据实验现象提出原子的核式结构。该实验说明( )
A. 绝大多数α粒子穿过金箔方向不变,说明原子所带正电是均匀分布的
B. 极少数α粒子发生大角度的偏转,说明任何实验都存在一些偶然现象
C. 原子全部正电荷和几乎全部质量都集中在体积较小的原子核里
D. 带负电的电子在核外空间里绕着核旋转
难度: 简单查看答案及解析
-
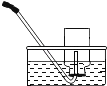
金属钠在氯气中燃烧,生成氯化钠固体,现象如图,则( )

A. 发生剧烈反应产生大量白雾
B. 氯化钠是由钠离子和氯离子构成的
C. 氯原子在反应中失去电子形成带负电荷的氯离子
D. 钠原子和钠离子的差别在于质子数不同
难度: 简单查看答案及解析
-
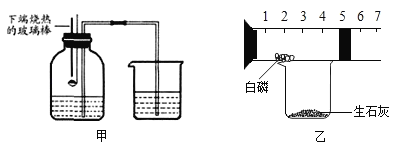
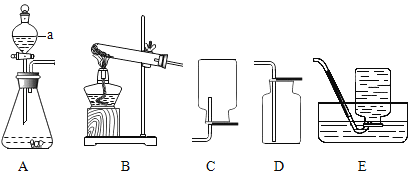
水在不同的实验中所起的作用可能不同,以下解释错误的是( )
A.
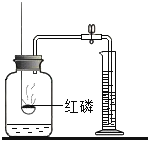 测定空气中氧气含量,通过量筒中水体积的变化得出O2体积
测定空气中氧气含量,通过量筒中水体积的变化得出O2体积B.
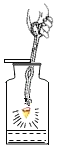 铁丝在氧气中燃烧,集气瓶中的水能冷却溅落融熔物防止瓶炸裂
铁丝在氧气中燃烧,集气瓶中的水能冷却溅落融熔物防止瓶炸裂C.
硫在氧气中燃烧,集气瓶中水主要能吸收放出的热量
D.
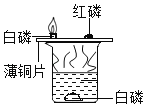 探究燃烧条件,烧杯中的水能加热铜片和隔绝空气
探究燃烧条件,烧杯中的水能加热铜片和隔绝空气难度: 简单查看答案及解析
-
X、Y、Z、W四种物质在一定条件下充分反应后,测得反应前后各物质的质量如下,获得的信息正确的是( )
X
Y
Z
W
反应前质量/g
22
34
2
0
反应后后质量/g
40
待测
2
16
A. 表格中待测量为0
B. 反应中Y和X的质量比是9:17
C. Z在反应中一定是催化剂
D. W在该反应中是反应物
难度: 简单查看答案及解析
-
化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和,
和
各取一个原子相比较,正确的是( )
A. 不同种原子 B. 不是同位素 C. 中子数相同 D. 电子数不同
难度: 简单查看答案及解析