-
用NA表示阿伏加德罗常数,下列有关说法正确的是
A.2.0 g D218O中含有的质子数为NA
B.标准状况下,22.4 L NH3分子含有的杂化轨道数为4 NA
C.78 g Na2O2晶体中所含阴、阳离子个数均为2 NA
D.1 mol Fe完全溶于一定量的硝酸溶液中,转移的电子数一定是3 NA
难度: 中等查看答案及解析
-
小明同学的化学纠错本上有如下内容,其中原因分析及改正有误的是
错误
原因分析及改正
A
FeBr2溶液中通入少量Cl2的离子方程式:
2Br-+Cl2=Br2+2Cl-
还原性强弱:Fe2+>Br-;
改正:2Fe2++Cl2=2Fe3++2Cl-。
B
除去CO2中的HCl气体:通过饱合Na2CO3溶液,分离方法:洗气
“饱合”应为“饱和”,Na2CO3不仅要吸收HCl气体,还要吸收CO2,应改用饱和NaHCO3溶液;分离方法:洗气。
C
用已知浓度的HCl溶液滴定未知浓度的NaOH溶液。指示剂:甲基橙,终点判断:当滴至最后一滴标准液,溶液由黄色变为橙色,即达终点。
指示剂不能用甲基橙,改用酚酞,终点判断:当滴至最后一滴标准液,溶液由红色变为浅红色,即达终点。
D
双原子分子一定是非极性分子
双原子分子有可能为单质或化合物分子;
改正:双原子单质分子一定是非极性分子而双原子化合物分子一定是极性分子。
难度: 困难查看答案及解析
-
化学与环境、材料、信息、生活关系密切,下列说法正确的是
A.“山东疫苗案”涉疫苗未冷藏储运而失效,这与蛋白质变性有关
B.硫、氮、碳的氧化物是形成酸雨的主要物质
C.半导体行业中有一句“行话”:“从沙滩到用户”,说明计算机芯片的主要成分是二氧化硅
D.自来水厂常用明矾作消毒杀菌剂
难度: 中等查看答案及解析
-
下列有关离子方程式书写或离子共存说法正确的是
A.在0.1 mol/L Na2CO3溶液中:Al3+、NH4+、SO42-、NO3-一定能大量共存
B.常温下,
=0.1 mol/L的溶液中,下列离子一定能大量共存:K+、Cl-、Fe2+、NO3-
C.清洗锅炉时先用纯碱溶液浸泡的主要原因:CaSO4(s)+CO32-(aq)
SO42-(aq)+CaCO3(s)
D.向Al2(SO4)3溶液中加入少量Ba(OH)2溶液:Ba2++SO42-+Al3++3OH-=BaSO4↓+Al(OH)3↓
难度: 困难查看答案及解析
-
150℃时,在固定容积的密闭容器中将1 L气态混合烃与9 L氧气(足量)混合点燃,恢复到原温度时容器内压强为原来的108%,则原混合烃组成可能是
A.甲烷与乙烷体积比为1∶4
B.乙烯与丁烷体积比为4∶1
C.丙炔与乙炔物质的量比为4∶1
D.乙烯与丁烯物质的量比为1∶4
难度: 中等查看答案及解析
-
常温下,下列有关稀溶液中离子浓度的说法正确的是
A.同浓度的四种溶液:① NH4Cl ② (NH4)2SO4 ③ NH4HSO4 ④ NH4Al(SO4)2溶液,c(NH4+)浓度的大小关系:②>④>③>①
B.一定浓度的NaHS溶液中:c(Na+)+c(OH-)=c(H+)+c(HS-)+2c(H2S)
C.若0.1 mol/L NH4Cl溶液pH=5,则其中离子浓度最大与最小的差值为(0.1-10-5)mol/L
D.现有四种溶液:① pH=4的H2SO4溶液 ② pH=4的NH4Cl溶液 ③ pH=10的氨水 ④ pH=10的CH3COONa溶液,其中水电离出的氢离子浓度大小关系为:②=④>③>①
难度: 困难查看答案及解析
-
向甲、乙、丙三个容积固定不变的密闭容器中充入一定量的X和Y,一定条件下发生反应 X(g)+aY(g)
2Z(g)。各容器的反应温度、反应物起始量、反应过程中Z的浓度随时间变化分别以下图和下表来表示。下列说法不正确的是
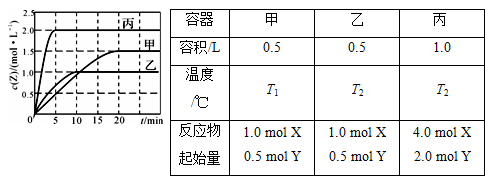
A.该反应温度升高,平衡常数减小
B.20 min内甲容器中反应的平均速率:v(X)=0.0375mol·(L·min)-1
C.10 min时,其他条件不变,向乙容器中再加入2 mol Z,平衡向逆反应方向移动
D.其他条件不变,若缩小乙的体积,Y的转化率增大
难度: 困难查看答案及解析