-
下列关于某些离子的检验及结论,一定正确的是( )
A. 加入稀盐酸产生无色气体,将该气体通入澄清石灰水中变浑浊,则一定有CO32-
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定有SO42-
C. 加入浓烧碱溶液加热,产生的气体能使湿润的红色石蕊试纸变蓝,则一定有NH4+
D. 加入Na2CO3溶液产生白色沉淀,再加盐酸,白色沉淀消失,则一定有Ba2+
难度: 困难查看答案及解析
-
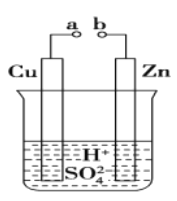
下列有关电池的说法不正确的是( )
A. 手机上用的锂离子电池属于二次电池
B. 锌锰干电池中,锌电极是负极
C. 氢氧燃料电池可把化学能转化为电能
D. 铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
难度: 简单查看答案及解析
-
下列物质中属于电解质的是
①酒精 ②硫酸铜 ③水 ④醋酸 ⑤镁 ⑥氨水
A. ①②④⑤ B. ②③④ C. ②③④⑥ D. 全部
难度: 简单查看答案及解析
-
化学与生产、生活密切相关。下列叙述不正确的是
A. 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体
B. 煤的干馏和石油的分馏均属化学变化
C.
可用于文物年代的鉴定,
与
互为同位素
D. 用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
难度: 中等查看答案及解析
-
下列选项中正确的是( )
A. 钠原子的结构示意图:

B. 过氧化钠的电子式:
C. 碳酸氢钠的电离方程式:NaHCO3= Na++ H+ + CO32-
D. 中子数为12的钠的核素符号为:
难度: 中等查看答案及解析
-
下列实验操作能达到目的是( )
A. 用pH试纸测定次氯酸溶液的pH=3.5
B. 将FeCl3溶液加热蒸干并灼烧获得Fe2O3固体
C. 向明矾溶液中加入一定量NaOH制备Al(OH)3胶体
D. 室温下,测得pH=5的NaHSO4溶液与pH=9的NaHCO3溶液中水的电离程度相等
难度: 简单查看答案及解析
-
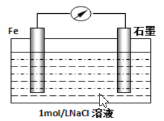
用下列实验装置进行相应实验,能达到实验目的的是( )
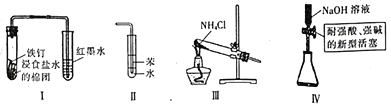
A. Ⅰ用于观察铁的析氢腐蚀 B. Ⅱ用于吸收HCl
C. Ⅲ可用于制取NH3 D. Ⅳ用于量取20.00mLNaOH溶液
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 18 g D2O所含的电子数为10NA
B. 1 mol H2O2中含有极性键的数目为3NA
C. 标准状况下,22.4 L四氯化碳所含分子数为NA
D. 32g O2和O3的混合物中含有的氧原子数为2NA
难度: 中等查看答案及解析
-
下列各组离子一定能大量共存的是( )
A. 在强碱溶液中:Na+、K+、AlO2﹣、CO32﹣
B. 在pH=0的溶液中:K+、Fe2+、Cl﹣、NO3﹣
C. 在含大量Fe3+的溶液中:NH4+、Na+、Cl﹣、SCN﹣
D. 在c(H+)=10﹣13mol/L的溶液中:NH4+、Al3+、SO42﹣、NO3﹣
难度: 中等查看答案及解析
-
同温同压下,体积相同的两个容器中,分别充满由
、
、
三种原子构成的一氧化氮(
)和一氧化碳(
)。下列说法正确的是( )
A. 所含分子数和质量均不相同
B. 含有相同的质子和中子
C. 含有相同的分子数和电子数
D. 含有相同数目的中子、原子和分子
难度: 简单查看答案及解析
-
某无色透明的混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体。现将此混合气体通过品红溶液后,品红溶液褪色,向剩余气体中通入空气,很快变为红棕色。下列对于原混合气体成分的判断中正确的是
A. 肯定没有SO2和NO B. 肯定没有Cl2、O2和NO2
C. 可能有Cl2和O2 D. 肯定只有NO
难度: 中等查看答案及解析
-
下列用来表示物质变化的化学用语中,正确的是( )
A. 氢氧碱性燃料电池的负极反应式:O2+2H2O+4e-
4OH-
B. 粗铜精炼时与电源正极相连的是纯铜,主要电极反应式:Cu-2e-=Cu2+
C. 钢铁发生电化学腐蚀的负极反应式:Fe-3e-
Fe3+
D. 钢闸门应与外接电源的负极相连,起保护作用
难度: 中等查看答案及解析
-
将反应Cu(s)+2Ag+(aq)
Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,下列有关叙述正确的是

A. KNO3盐桥中的K+移向Cu(NO3)2溶液
B. 工作一段时间后,AgNO3溶液中c(Ag+)减小
C. 电子由AgNO3溶液通过盐桥移向Cu(NO3)2溶液
D. Cu作负极,发生还原
难度: 简单查看答案及解析
-
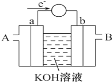
一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通乙烷和氧气,电极反应为C2H6+18OH-=2CO32-+12H2O+14e-;14H2O+7O2+28e-=28OH-,有关推断错误的是( )
A. 通氧气的电极为正极
B. 在电解质溶液中CO32-向正极移动
C. 放电一段时间后,KOH的物质的量浓度将下降
D. 参加反应的氧气和乙烷的物质的量之比为7∶2
难度: 中等查看答案及解析