-
用右图表示的一些物质或概念间的从属或包含关系中不正确的是
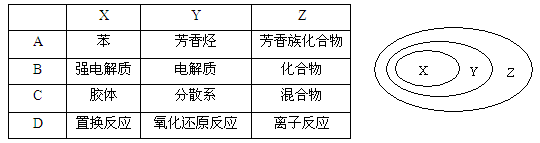
难度: 中等查看答案及解析
-
稀土是工业味精,邓小平说过“中东有石油,我们有稀土”。金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是
A.电解熔融CeO2制Ce,铈在阳极获得
B.铈有四种稳定的核素
Ce、
Ce、
Ce、
Ce,它们互为同素异形体
C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+
D.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑
难度: 中等查看答案及解析
-
下列实验装置设计正确且能达到目的的是
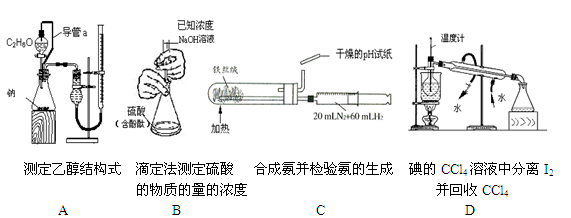
难度: 中等查看答案及解析
-
下列离子方程式中正确的
A.向苯酚钠溶液中通入少量CO2:
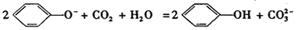
B.向氯化银悬浊液中滴加氨水,溶液逐渐澄清:
2NH3·H2O+AgCl Ag(NH3)2++Cl-+2H2O
C.石墨做电极,电解硫酸铜溶液:Cu2++2H2O Cu + O2↑+ 4H+
D.氯气溶于水:Cl2+H2O Cl-+ ClO-+2H+
难度: 中等查看答案及解析
-
下列操作中正确的是
A.除去乙酸乙酯中的少量乙酸:加入乙醇和浓硫酸将乙酸全部转化为乙酸乙酯
B. 除去C2H5OH中的少量CH3COOH:加足量CaO,蒸馏
C. 用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO
D.将蔗糖在稀硫酸中加热水解后,直接加入银氨溶液检验是否有葡萄糖生成
难度: 中等查看答案及解析
-
在一体积不变的密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g)
2C(g);△H<0。达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
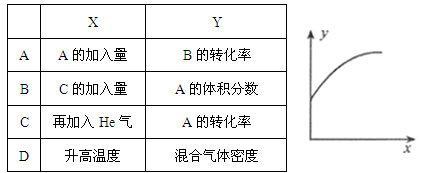
难度: 中等查看答案及解析
-
在某温度时,pH=3的某水溶液中c(OH-)=10-9mol/L,现有该温度下的四份溶液:①pH=2的CH3COOH、②0.01 mol·L-1的HCl、③pH=11的氨水、④pH=11的NaOH溶液,下列说法正确的是
A.①中水的电离程度最小,③中水的电离程度最大
B.将②、③混合,若pH=7,则消耗溶液的体积②=③
C.将四份溶液稀释相同倍数后,溶液的pH:③>④>②>①
D.将①、④混合,若有c(CH3COO-) > c(H+),则混合液一定呈碱性
难度: 中等查看答案及解析
-
某有机化合物A只含碳、氢、氧三种元素,常用作局部麻醉剂和镇痛剂。,其分子模型如右图所示(图中球与球之间的连线代表化学键,如单键、双键等)。下列说法错误的是

A.它的分子式为C10H12O2
B.有机物A是苯酚的同系物
C.1molA与足量的浓溴水反应最多可能消耗2 molBr2
D.有机物A遇FeCl3溶液显紫色,至少有12个原子共平面
难度: 中等查看答案及解析




