-
2018年4月22日是第49个世界地球日。今年地球日活动周主题为“珍惜自然资源呵护美丽国土”。下列有关说法或做法正确的是
A. 推广使用煤、石油、天然气,有利于缓解温室效应
B. 普通锌锰于电池不含环境污染物,可以随意丢弃
C. 在生产、流通和消费等过程中实行“减量化、再利用、资源化”
D. 将高耗能、高污染的企业迁至偏僻的农村地区,提高贫穷地区居民收入
难度: 中等查看答案及解析
-
有机化合物与人类的生活密切相关,下列叙述中正确的是
A. 蚕丝和棉花的主要成分均是纤维素
B. 糯米中的淀粉一经水解就酿成了酒
C. 用加酶洗衣粉洗涤羊毛织品效果更好
D. 乙醇和乙酸都是常用调味品的主要成分
难度: 中等查看答案及解析
-
除去下列物质中的杂质(括号内为杂质),所用试剂和分离方法均正确的是( )
混合物
所用试剂
分离方法
A
甲烷(乙烯)
酸性高锰酸钾
洗气
B
苯(乙酸)
氢氧化钠溶液
分液
C
氯气(HCl)
氢氧化钠溶液
洗气
D
乙醇(水)
金属钠
蒸馏
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下表是部分短周期元素的原子半径及主要化合价,根据下表信息判断正确的是
元素代号
L
M
Q
R
T
原子半径/nm
0.130
0.118
0. 090
0.102
0.073
主要化合价
+2
+3
+2
+6、-2
-2
A. 简单氢化物的沸点:T<R
B. 最高价氧化物对应水化物的碱性:L<Q
C. L2+与R2-的核外电子数相等
D. M与T形成的化合物具有两性
难度: 中等查看答案及解析
-
书法离不开文房四宝(笔、墨、纸、砚),做笔用的狼毫、研墨用的墨条、宣纸和做砚台用的砚石的主要成分依次是
A. 多糖、石墨、蛋白质、无机盐
B. 塑料、石墨、多糖、无机盐
C. 蛋白质、炭黑、多糖、无机盐
D. 蛋白质、煤炭、多糖、有机玻璃
难度: 简单查看答案及解析
-
硒(Se)是人体必需的微量元素,具有抗氧化、增强免疫力等作用。下列说法错误的是
A.
与
互为同位索
B.
与
属于同种原子
C.
与
核外电子排布相同
D.
与
是硒元素的两种不同核素
难度: 中等查看答案及解析
-
现欲用纯净的CaCO3与稀盐酸反应制取CO2,生成CO2的体积与时间的关系如下图所示。下列叙述正确的是
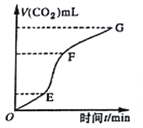
A. OE段化学反应速率最快
B. FG段收集的二氧化碳最多
C. 由图像无法推断出该反应为放热反应
D. 向溶液中加入氯化钠溶液,可以降低该反应的化学反应速率
难度: 中等查看答案及解析
-
科学家发现一种只有四个中子构成的粒子,这种粒子被称为“四中子”,也有人称之为“零号元素”。下列关于“四中子”粒子的说法不正确的是
A. 该粒子不显电性
B. 在周期表中与氢元素在同一周期
C. 该粒子质量比氢原子大
D. 该粒子质量数为4
难度: 简单查看答案及解析
-
下列反应过程中,同时有离子键和共价键的断裂和形成的是
A. 2H2+O2
2H2O B. NH3 +HCl=NH4Cl
C. 2Na2O2+2H2O=4NaOH+O2↑ D. 2Mg+CO2
2MgO+C
难度: 中等查看答案及解析
-
(题文)已知某反应中能量变化如图所示,所得结论错误的是( )

A. 该图像可以表示氯化铵与消石灰反应的能量变化
B. 该反应过程中,一定有其他形式的能量转化成化学能
C. 该反应过程中,形成新化学键释放的总能量小于断裂旧化学键吸收的总能量
D. 因为生成物的总能量高于反应物的总能量,所以该反应一定需要加热才可进行
难度: 中等查看答案及解析
-
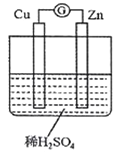
如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M、N、P物质,其中可以成立的是

M
N
P
A
Zn
Cu
稀H2SO4溶液
B
Cu
Fe
稀HCl溶液
C
Ag
Zn
AgNO3溶液
D
Zn
Fe
Fe(NO3)3溶液
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
关于生活中的有机物,下列说法不正确的是( )
A. 葡萄糖可以发生氧化反应、银镜反应和水解反应
B. 工业上利用油脂在碱性条件下的水解反应制取肥皂和甘油
C. 食用植物油的主要成分是高级不饱和脂肪酸甘油酯,是人体的营养物质
D. 皮肤接触浓硝酸变黄是蛋白质的颜色反应
难度: 中等查看答案及解析
-
某元素一种原子的质量数为A,其阴离子Xn-核外有x个电子,mg这种原子的原子核内中子的物质的量为
A.
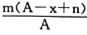 mol B.
mol B. 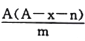 mol
molC.
 mol D.
mol D. 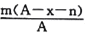 mol
mol难度: 中等查看答案及解析
-
已知:N2O4(g)
2NO2(g) ,将装有N2O4和NO2混合气体的烧瓶浸入热水中,烧瓶内混合气体的颜色逐渐变深。下列结论不能说明该反应已经达到化学平衡状态的是
A. 烧瓶内气体的质量不再变化
B. 烧瓶内气体的颜色不再变化
C. 烧瓶内气体的压强不再变化
D. N2O4的消耗速率与NO2的消耗速率之比为1:2
难度: 简单查看答案及解析
-
X、Y、Z、M均为短周期元素,它们在周期表中的位置如下图。若Y原子的最外层电子数是次外层电子数的3倍。下列说法中正确的是

A. 原子半径:X<Y<Z<M
B. 最简单气态氢化物的热稳定性:Y<Z
C. 最高价氧化物对应水化物的酸性:Z<M
D. X与Y形成的化合物均易溶于水
难度: 中等查看答案及解析
-
甲烷和乙烯的混合气体5 L,完全燃烧消耗相同状况下的O2 12 L,则甲烷和乙烯的体积比为
A. 2:1 B. 1:2 C. 3:2 D. 2:3
难度: 中等查看答案及解析