-
关于油脂的下列叙述中不正确的是[ ]
A.油脂属于酯类 B.油脂没有固定的熔沸点
C.油脂是高级脂肪酸的甘油酯 D.油脂都不能使溴水褪色
难度: 简单查看答案及解析
-
蔗糖3.42g与麦芽糖3.42g混合后并完全水解,若生成m个葡萄糖分子与n 个果糖分子,则m与n的比值是[ ]
A.1:3 B.3:1 C.1:2 D.1:1
难度: 简单查看答案及解析
-
能使蛋白质从溶液中析出,又不使蛋白质变性的方法是[ ]
A.加饱和硫酸钠溶液 B.加福尔马林
C.加75%的酒精 D.加氯化钡溶液
难度: 简单查看答案及解析
-
甘氨酸和丙氨酸在一定条件下发生缩合反应,生成的二肽有[ ]
A.1种 B.2种 C.3种 D.4种
难度: 简单查看答案及解析
-
25 ℃时,合成氨反应的热化学方程式为:
N2(g)+3H2(g)
2NH3(g) △H=-92.4 kJ/mol
在该温度时,取2mol N2和7 mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是[ ]
A.92.4 kJ B.92.4 kJ ~184.8 kJ
C.小于184.8 kJ D.184.8 kJ
难度: 简单查看答案及解析
-
新科技革命三大支柱通常是指[ ]
①能源 ②交通 ③通讯 ④材料 ⑤信息
A.①②③ B.①③⑤ C.②③⑤ D.①④⑤
难度: 简单查看答案及解析
-
硅橡胶
 是由二甲基二氯硅烷
是由二甲基二氯硅烷经两种反应而制得的,这两种反应依次是[ ]
A.取代、缩聚 B.水解、加聚
C.氧化、缩聚 D.消去、加聚
难度: 简单查看答案及解析
-
下列材料中属于功能高分子材料的是[ ]
①高分子膜 ②生物高分子材料 ③隐身材料
④液晶高分子材料 ⑤光敏高分子材料 ⑥智能高分子材料
A.①②⑤ B.②④⑤⑥ C.③④⑤ D.全部
难度: 简单查看答案及解析
-
具有单双键交替长链(如:—CH=CH—CH=CH—CH=CH—…)的高分子有可能成为导电塑料。下列高分子中可能成为导电塑料的是[ ]
A.聚乙烯 B.聚丁二烯
C.聚苯乙烯 D.聚乙炔
难度: 简单查看答案及解析
-
完全燃烧一定质量的无水乙醇,放出的热量为Q,已知为了完全吸收生成的二氧化碳,消耗掉8mol·L-1的氢氧化钠溶液50mL,则相同条件下1 mol无水乙醇燃烧放出的热量不可能是[ ]
A.小于5Q B.5Q C.5Q~10Q D.10Q
难度: 简单查看答案及解析
-
下列对化学反应热现象的说法正确的是[ ]
A.放热反应发生时都不必加热
B.化学反应中一定有能量变化
C.一般地说,吸热反应加热后才能发生
D.化学反应的热效应数值与参加反应的物质的多少无关
难度: 简单查看答案及解析
-
在a g冰醋酸、甲醛、葡萄糖、甲酸甲酯、果糖的混合物中,碳元素的质量分数为[ ]
A.30% B.40%
C.50% D.数据不全,无法计算
难度: 简单查看答案及解析
-
人造象牙主要成分的结构是
,它是通过加聚反应制得的,则合成象牙的单体是[ ]
A.HCHO B.CH3CHO
C.CH3OCH3 D.C2H2和H2O
难度: 简单查看答案及解析
-
下列热化学方程式中的反应热为可燃物的燃烧热的是[ ]
A.H2(g)+1/2O2(g)=H2O(g) △ H =-241.8kJ·mol—1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △ H =-846.3kJ·mol—1
C.C(s)+O2(g)=CO2(g) △ H =-393.5kJ·mol—1
D.C3H8(g)+5O2(g)=3CO(g)+4H2O(l) △ H = -2044.0kJ·mol—1
难度: 简单查看答案及解析
-
已知热化学方程式:2H2(g)+O2(g)=2H2O(g) ΔH1=-483.6kJ/mol, 则对于热化学方程式:2H2O(l)=2H2(g)+O2(g) ΔH2=b,下列说法正确的是[ ]
A.该反应的ΔH2=+483.6kJ/mol B.|ΔH2|<|ΔH1|
C.|ΔH2|>|ΔH1| D.热化学方程式中化学计量数表示分子个数
难度: 简单查看答案及解析
-
有反应2A(g)+B(g)
2C(g) △H =Q,下列叙述正确的是[ ]
A.增大压强,v正增大,v逆减小
B.升高温度,v正减小,v逆增大
C.增大A浓度的瞬间,v正增大,v逆不变
D.增大A浓度瞬间,v正增大而v逆减小
难度: 简单查看答案及解析
-
对于反应M+N→P,如果温度每升高10℃,速率增大为原来的3倍,在10℃时,完成反应10%需81min,则在30℃时完成反应10%需要时间为[ ]
A.27min B.9min C.13.5min D.3min
难度: 简单查看答案及解析
-
在10L密闭容器中,发生如下反应:
4NH3(g)+5O2(g)
4NO(g)+6H2O(g)。半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均反应速率υ(X)(反应物的消耗速率或产物的生成速率)可表示为[ ]
A.υ(NH3)=0.0100mol·L-1·s-1 B.υ(O2)=0.0010mol·L-1·S-1
C.υ(NO)=0.0010mol·L-1·s-1 D.υ(H2O)=0.045mol·L-1·s-1
难度: 简单查看答案及解析
-
甲乙两个容器内都在进行A→B的反应,甲中每分钟减少4molA,乙中每分钟减少2molA,则两容器中的反应速率[ ]
A.甲快 B.乙快 C.相等 D.无法确定
难度: 简单查看答案及解析
-
在恒温、恒容的密闭容器中进行反应A(g)
B(g)+C(g)。若反应物的浓度由2mol/L降到0.8mol/L需20s,那么反应物浓度由0.8mol/L降到0.2mol/L所需反应时间为[ ]
A.10s B.大于10s C.小于10s D.无法判断
难度: 简单查看答案及解析
-
反应N2+O2=2NO,在密闭容器中进行,能加快该反应速率的是[ ]
A.扩大体积使压强增大 B.体积不变充入N2使压强增大
C.体积不变充入He使压强增大 D.压强不变充入N2使体积增大
难度: 简单查看答案及解析
-
淀粉溶液中加入少量稀硫酸,加热使淀粉水解,为测定其水解程度,下列试剂:①氢氧化钠溶液;②银氨溶液;③新制的氢氧化铜悬浊液;④碘水。
其中必须使用的是[ ]
A.④ B.②④ C.①④ D.①③④
难度: 简单查看答案及解析
-
强酸与强碱在稀溶液发生中和反应的热化学方程式为:
H+(aq)+OH-(aq)=H2O(l) △H=-57.3 KJ/mol,向3份同体积0.2 mol/L的NaOH溶液中分别加入适量的①稀醋酸、②浓硫酸、③稀硝酸,恰好完全反应的热效应△H1、△H2、△H3的关系正确的是[ ]
A.△H1>△H2>△H3 B.△H2>△H3>△H1
C.△H2>△H1>△H3 D.△H1>△H3>△H2
难度: 简单查看答案及解析
-
某温度时,2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均速率分别为
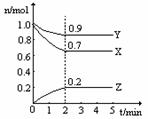
A.3X+Y
2Z; 0.05 mol/(L·min)
B.2X+Y
2Z; 0.1 mol/(L·min)
C.3X+Y
2Z; 0.1 mol/(L·min)
D.X+3Y
2Z; 0.05 mol/(L·min)
难度: 简单查看答案及解析
-
在相同温度和压强下,将32g硫分别在纯氧气中和空气中完全燃烧,令前者放出的热量为Q1,后者放出的热量为Q2,则关于Q1和Q2的相对大小判断正确的是[ ]
A.Q1<Q2 B .Q1>Q2 C.Q1=Q2 D.无法确定
难度: 简单查看答案及解析
-
一定温度下,向一个容积为2L的真空密闭容器中(事先装入催化剂)通入
和
,
后测得密闭容器内的压强是起始时的0.9倍,在此时间内
是[ ]
A.
B.
C.
D.
难度: 简单查看答案及解析
-
常温下,分别将四块形状相同质量为9g的铁块同时投入下列四种溶液中,产生H2速率最快的是[ ]
A.500mL2mol/L的HCl B.200mL2mol/L的H2SO4
C.300mL3mol/L的HCl D.500mL6mol/L的HNO3
难度: 简单查看答案及解析
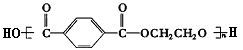 ,它是________和________(填单体的结构简式)通过____________反应而制的,反应的化学方程式为:______________________________________________。
,它是________和________(填单体的结构简式)通过____________反应而制的,反应的化学方程式为:______________________________________________。