-
有机化学在日常生活应用广泛,下列有关说法不正确的是
A.相同条件下,正丁烷、新戊烷、异戊烷的沸点依次增大
B.苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色
C.甲苯和Cl2光照下的反应与乙醇和乙酸的反应属于同一类型的反应
D.有芳香气味的C9H18O2在酸性条件下加热可水解产生相对分子质量相同的两种有机物,则符合此条件的C9H18O2的结构有16种
难度: 中等查看答案及解析
-
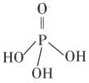
莽草酸的结构简式如图,下列关于莽草酸的说法不正确的是

A.相同条件下等物质的量的莽草酸和正戊醛(C5H10O)完全燃烧时的耗氧量相同
B.分子中含有两种含氧官能团,可发生取代反应
C.1mol莽草酸既可与2mol氢气发生加成反应,也可与4molNaOH发生中和反应
D.可用溴水鉴别莽草酸、乙醇、四氯化碳和苯
难度: 中等查看答案及解析
-
NA为阿伏伽德罗常数的值.下列叙述正确的是
A.常温常压下,46g的NO2和N2O4混合气体含有的分子数为NA
B.1mol Fe粉与1mol水蒸气充分反应转移的电子数为2NA
C.标准状况下,1L乙醇完全燃烧产生
分子的数目为
D.
中含有电子数为
难度: 中等查看答案及解析
-
下列热化学方程式或离子方程式中,正确的是
A.0.01mol·L-1NH4Al(SO4)2溶液与0.02mol·L-1Ba(OH)2溶液等体积混合:
NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
B.一定条件下,将0.5mol N2(g)和1.5molH2(g)置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:
N2(g)+3H2(g)
2NH3(g) △H=-38.6kJ·mol-1
C.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+==AgBr↓
D.CO(g)的燃烧热是283.0 kJ·mol-1,则CO2分解的热化学方程式为:
2CO2(g) =2CO(g)+O2(g) ΔH=+283.0 kJ·mol-1
难度: 中等查看答案及解析
-
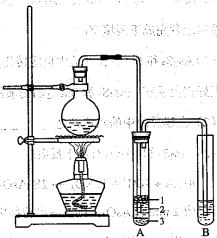
关于如图所示①、②两个装置的评价正确的是

选择
叙 述
评价
A
装置名称:①电解池,②原电池
错误
B
硫酸浓度变化:①增大,②减小
错误
C
电极反应式:①阳极:4OH--4e-====2H2O+O2↑
②正极:Zn-2e-====Zn2+
正确
D
离子移动方向:①H+向阴极移动 ②H+向正极移动
正确
难度: 中等查看答案及解析
-
次氯酸可用于杀菌消毒。已知25°C时:
①HClO(aq)+OH-(aq)= ClO-(aq)+ H2O(l) ΔH=-Q1kJ·mol-1
②H+(aq) +OH-(aq) = H2O(l) ΔH=-57.3kJ·mol-1
下列说法正确的是
A.在25°C时,次氯酸的电离方程式及热效应可表示为:
HClO(aq)=H+(aq)+ClO-(aq) ΔH=-(57.3+Q1)kJ·mol-1
B.将20ml 1mol/L HClO与10ml 1mol/L NaOH混合后的溶液,一定存在:
2C(H+)-2C(OH-)=C(ClO-)-C(HClO)
C.已知酸性H2SO3>HClO>HSO3-, 则向Na2SO3溶液中加入HClO的离子方程式为:SO32-+ HClO= HSO3-+ ClO-
D.已知酸性CH3COOH>HClO,则等浓度CH3COONa和NaClO的混合液中:
C(Na+)> C(ClO-)> C(CH3COO-)> C(OH-)> C(H+)
难度: 中等查看答案及解析
-
有6.85g铅的氧化物,用足量的CO 在高温下将其还原,把生成的全部CO2通入到足量的澄清的石灰水中得到4.00g固体沉淀物,这种铅的氧化物的化学式为
A. PbO B. PbO2
C. Pb3O4 D. Pb3O4和PbO2的混合物
难度: 中等查看答案及解析