-
在下列物质中,化学键类型相同的一组是( )
A.CO2和H2O
B.NaCl和HCl
C.CCl4和KCl
D.MgCl2和SO2难度: 中等查看答案及解析
-
下列除去杂质的方法正确的是( )
物质 杂质 试剂 主要操作 A SiO2 Fe2O3 盐酸 过滤 B CO2 CO O2 点燃 C FeCl2溶液 FeCl3 Cu 分液 D CH3CH2OH H2O Na 蒸馏
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
X、Y、Z都是第三周期元素,核电荷数依次增大,X的氧化物对应水化物强碱,Z的原子半径最小(稀有气体除外).据此判断下列说法不正确的是( )
A.X是第ⅠA元素,Z是第ⅦA元素
B.X、Y、Z三种元素的最高化合价逐渐减小
C.Z的最高价氧化物对应的水化物是强酸
D.X、Z形成的化合物是离子化合物难度: 中等查看答案及解析
-
误食重金属盐而引起的中毒,急救方法是( )
A.服用大量生理盐水
B.服用大量冷开水
C.服用大量的豆浆或牛奶
D.服用大量小苏打溶液难度: 中等查看答案及解析
-
下列实验现象描述正确的是( )
A.氯化氢与氨气相遇,有大量的白雾生成
B.用铂丝蘸取硫酸钠溶液灼烧,火焰呈黄色
C.氯化亚铁溶液与无色的KSCN溶液混合,溶液呈红色
D.SO2通入品红溶液,红色褪去,再加热,红色不再出现难度: 中等查看答案及解析
-
新型镁合金被大量应用于制成笔记本电脑外壳、竞赛自行车框架等,这说明镁合金具有的优异性能是( )
①熔点低 ②硬度大 ③延展性好 ④导电性强 ⑤密度小 ⑥耐腐蚀.
A.①②③
B.②③④
C.①③⑥
D.②⑤⑥难度: 中等查看答案及解析
-
能够将溶液和胶体区分开的方法是( )
A.过滤
B.观察颜色、状态
C.利用丁达尔效应
D.闻气味难度: 中等查看答案及解析
-
对于2NaBr+Cl2═2NaCl+Br2反应,下列说法不正确的是( )
A.该反应既是置换反应,又是氧化还原反应
B.Cl2是氧化剂,发生还原反应
C.若有1.6gBr2生成,反应过程中转移了0.02NA个电子
D.钠元素在反应中价态不变,所以NaBr既不是氧化剂,又不是还原剂难度: 中等查看答案及解析
-
下列化合物中,既有离子键又有共价键的是( )
A.NH4Cl
B.MgO
C.C2H6
D.CO2难度: 中等查看答案及解析
-
下列说法正确的是( )
A.1H、2H、3H互为同素异形体
B.O2、O3互为同位素
C.正丁烷和异丁烷互为同分异构体
D.乙烷、乙烯互为同系物难度: 中等查看答案及解析
-
在下列有关实验的叙述中,正确的是( )
A.用烧杯或烧瓶给液态物质加热时,不用垫石棉网
B.用乙醇和乙酸做原料可以制得乙酸乙酯
C.在用托盘天平称量固体药品时,药品直接放在右盘上
D.如果未知溶液中滴加BaCl2溶液有白色沉淀生成,证明原溶液中一定含有SO42-离子难度: 中等查看答案及解析
-
下列关于146C的叙述,错误的是( )
A.质子数是6
B.电子数为6
C.中子数是6
D.质量数是14难度: 中等查看答案及解析
-
下列物质在一定条件下不能和水反应的是( )
A.NH3
B.Cu
C.乙烯
D.淀粉难度: 中等查看答案及解析
-
下列化学用语书写正确的是( )
A.氯原子的结构示意图:
B.作为相对原子质量测定标准的碳核素:614C
C.氯化镁的电子式:
D.用电子式表示氯化氢分子的形成过程:难度: 中等查看答案及解析
-
在强酸性溶液中能大量共存的无色透明的离子组是( )
A.Al3+、Cu2+、NO3-、Cl-
B.Na+、NO3-、SO42-、CO32-
C.Mg2+、NH4+、SO42-、Cl-
D.Ba2+、K+、OH-、Cl-难度: 中等查看答案及解析
-
从节约原料和防止环境污染因素考虑,用铜制取硝酸铜,方法最佳的是( )
A.CuCu(NO3)2
B.CuCu(NO3)2
C.CuCuCl2
Cu(NO3)2
D.CuCuO
Cu(NO3)2
难度: 中等查看答案及解析
-
分别向盛有淀粉碘溶液的两烧杯中滴加新鲜黄瓜汁和久置黄瓜汁,黄瓜汁中含有的维生素C能使淀粉碘溶液褪色,实验结果见右表.下列说法不正确的是( )
黄瓜汁 新鲜 久置 滴数 12 20
A.维生素C具有还原性,能将碘单质还原为I-离子
B.实验时两烧杯中的淀粉碘溶液的浓度和体积相等
C.新鲜黄瓜汁中比久置黄瓜汁中维生素C含量低
D.维生素C缺乏的病人要多吃新鲜的蔬菜和水果难度: 中等查看答案及解析
-
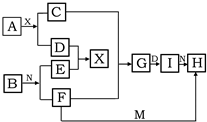
元素X的单质及X与Y形成的化合物能按如图所示的关系发生转化,则X为( )
A.Fe
B.Cu
C.S
D.C难度: 中等查看答案及解析
-
能正确表示下列化学反应的离子方程式是( )
A.碳酸钙与盐酸反应:CaCO3+2H+═Ca2++CO2↑+H2O
B.铜片与浓硝酸反应:Cu+NO3-+4H+═Cu2++NO↑+2H2O
C.二氧化锰与浓盐酸反应:MnO2+4HClMn2++2Cl-+Cl2↑+2H2O
D.硫酸铜与氢氧化钡反应:Ba2++SO42-═BaSO4难度: 中等查看答案及解析
-
下列关于如图所示的原电池的有关说法中,正确的是( )
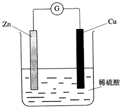
A.Zn是负极,发生还原反应
B.Cu是负极,发生氧化反应
C.锌片上有气体逸出
D.电子由锌片通过导线流向铜片难度: 中等查看答案及解析
-
下列食物属碱性食物的是( )
A.面包
B.葡萄
C.大米
D.鸡蛋难度: 中等查看答案及解析
-
下列关于药物的使用说法正确的是( )
A.虽然药物能治病,但大部份药物有毒副作用
B.青霉素有解热镇痛的作用
C.阿司匹林是最重要的抗生素
D.随着药物的普及,生病了都可以到药店自己买药吃难度: 中等查看答案及解析
-
人体中因缺少或过多会患甲状腺疾病的元素是( )
A.Na
B.Cl
C.F e
D.I难度: 中等查看答案及解析