-
奉贤在新一轮规划中提出要打造东方美谷。下列相关说法错误的是
A. 垃圾分类可有效提高垃圾的资源价值和经济价值
B. 绿色化学要求从源头上消除或减少对环境的污染
C. 推广可降解的一次性餐具,减少白色污染
D. 直接在田间焚烧秸秆,补充土壤中的钾元素
难度: 简单查看答案及解析
-
下列化学用语表示不正确的是
A. 碳原子的结构示意图:
B. CO2分子的电子式:
C. 碳原子核外电子排布的轨道表达式:
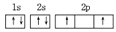
D. CO2分子的比例模型:
难度: 简单查看答案及解析
-
下列物质属于强电解质的是
A. 硫酸钡 B. 盐酸 C. 乙醇 D. 三氧化硫
难度: 简单查看答案及解析
-
下列说法中正确的是
A. 晶体中分子间作用力越大分子越稳定
B. 原子晶体中共价键越强熔点越高
C. 冰融化时水分子中共价键发生断裂
D. 氢氧化钠熔化时离子键、共价键均被破坏
难度: 简单查看答案及解析
-
下列关于化石燃料的加工说法正确的是
A. 石油裂化主要得到乙烯
B. 石油分馏是化学变化,可得到汽油、煤油
C. 煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气
D. 煤制煤气是物理变化,是高效、清洁地利用煤的重要途径
难度: 简单查看答案及解析
-
下列各项实验基本操作中,正确的是
A. 为了加快锌和稀硫酸反应的速率,可以向稀硫酸中加入少量硫酸铜
B. 在做中和滴定实验时清洗滴定管后,直接装液滴定
C. 为了加快过滤速度,用玻璃棒搅拌过滤器中的液体
D. 为了使配制的氯化铁溶液保持澄清,加入盐酸和铁片
难度: 简单查看答案及解析
-
有些物质既能与强酸溶液反应又能与强碱溶液反应,下列物质不具有此类性质的是
A. NaHCO3 B. (NH4)2CO3 C. Al D. AlCl3
难度: 中等查看答案及解析
-
下列涉及化学学科观点的有关说法正确的是
A. 微粒观:二氧化硫是由硫原子和氧原子构成的
B. 转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和
C. 守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g
D. 结构观:金刚石和石墨由于结构中碳原子的排列方式不同,性质存在着较大的差异
难度: 简单查看答案及解析
-
下列各组离子在碱性条件下能大量共存,而在强酸性条件下能发生氧化还原反应的是( )
A. Mg2+、Na+、SO42-、Cl— B. K+、CO32-、Cl—、NO3—
C. Na+、K+、NO3—、SO32— D. NH4+、Na+、SO42-、NO3—
难度: 中等查看答案及解析
-
下列溶液中通入足量SO2,根据其实验现象,所得结论不正确的是
溶液
现象
结论
A
含HCl、BaCl2和FeCl3的溶液
产生白色沉淀
SO2有还原性
B
H2S溶液
产生黄色沉淀
SO2有氧化性
C
酸性KMnO4溶液
紫红色溶液褪色
SO2有漂白性
D
加有酚酞的NaOH溶液
褪色
SO2是酸性氧化物
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
对滴有酚酞试液的下列溶液,操作后颜色变深的是 ( )
A.AlCl3溶液中再溶入AlCl3
B.CH3COONa溶液加热
C.氨水中加入少量NH4Cl固体
D.醋酸溶液加热
难度: 中等查看答案及解析
-
科学家在人工智能的研制过程中依据某化学规律,快捷地寻找到合适的光电效应材料,其依据的化学规律可能是
A. 元素周期律 B. 质量守恒定律 C. 阿伏伽德罗定律 D. 勒沙特列原理
难度: 中等查看答案及解析
-
下列物质溶液间中的反应可用离子方程式OH-+ H+→H2O表达的是:
A. H2SO4和Ba(OH)2 B. NH3·H2O和HCl
C. NaHSO4和KOH D. NaHCO3和NaOH
难度: 中等查看答案及解析
-
化学家格哈德·埃特尔证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下:

下列关于合成氨反应的叙述中不正确的是
A. 该过程表明,在化学反应中存在化学键的断裂与形成
B. 在催化剂的作用下,反应物的化学键变得容易断裂
C. 过程②需吸收能量,过程③则放出能量
D. 常温下该反应难以进行,是因为常温下生成物的化学键难以形成
难度: 中等查看答案及解析
-
电解CuCl2溶液的装置如右图所示,下列分析正确的是

A. b电极的质量不变 B. a电极是该装置的负极
C. a电极上发生氧化反应 D. 电子由b电极经溶液流向a电极
难度: 中等查看答案及解析
-
已知2SO2(g)+O2(g)
2SO3(g)+Q kJ·mol-1(Q>0)。下列说法正确的是
A. 相同条件下,2molSO2(g)和1molO2(g)所具有的能量小于2molSO3(g)所具有的能量
B. 将2molSO2(g)和1molO2(g)充分反应可放出的热量为Q kJ
C. 增大压强或升高温度,该平衡都向逆反应方向移动
D. 若充分反应后放热Q kJ,则此过程中有2molSO2(g)被氧化
难度: 中等查看答案及解析
-
莎普爱思眼药水适用于早期老年性白内障,有效成分之一苄达酸结构如图所示。下列关于苄达酸的叙述正确的是
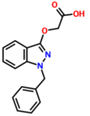
A. 分子式为C16H16N2O3 B. 属于芳香族化合物,且有弱酸性
C. 苯环上的一氯代物有5种 D. 该物质属于酯类
难度: 中等查看答案及解析
-
某溶液含有①NO3-、②HCO3- 、③SO32- 、④CO32- 、⑤SO42-等五种阴离子。向其中加入少量的Na2O2固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化)
A. ① B. ①⑤ C. ①④⑤ D. ①③④⑤
难度: 中等查看答案及解析
-
在下列工业生产中,进行的主要反应是非氧化还原反应的是
①氯碱工业 ②氨碱法制纯碱 ③由焦炭、水、空气等合成氨 ④工业上生产硫酸
A. ④ B. ①③ C. ①②④ D. ②
难度: 中等查看答案及解析
-
一定量的H2和Cl2充分燃烧后,将反应生成的气体通入100mL1.0mol/L的NaOH溶液中,两者恰好完全反应,生成NaClO为0.01mol。则燃烧前H2和Cl2的物质的量之比为
A. 5:4 B. 4:5 C. 4:3 D. 3:4
难度: 中等查看答案及解析
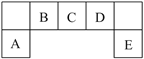

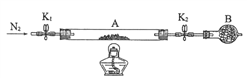
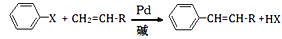 (X为卤原子,R为取代基)
(X为卤原子,R为取代基)