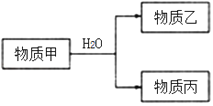
-
下列叙述不正确的是( )
A. NH3的结构式:
B.
的原子核内的中子数与核外电子数之差是32
C. Na2O2与H2O2中所含的化学键类型不完全相同
D. 可以利用在水溶液中是否导电证明氯化铝是离子化合物还是共价化合物
难度: 简单查看答案及解析
-
五种短周期元素X、Y、Z、M、W的原子序数与其常见化合价的关系如图所示,下列关系不正确的是( )
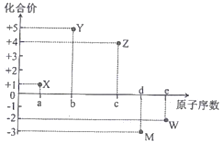
A. 元素X可能为锂
B. 原子半径大小:r(M)>r(w)
C. X2W中各原子均达8电子稳定结构
D. 元素气态氢化物的沸点:YH3>MH3
难度: 中等查看答案及解析
-
下列关于热化学反应的描述中正确的是( )
A. HCl和NaOH反应的中和热△H=-57.3 kJ·mol-1,则1 mol硫酸与足量氢氧化钡溶液反应放热为114.6 kJ
B. H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(1)=2H2(g)+O2(g)反应的△H=+571.6kJ·mol-1
C. 反应物的热效应与是否使用催化剂有关
D. 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g) + 3H2(g) ⇌ 2NH3(g) △H= -38.6 kJ·mol-1
难度: 中等查看答案及解析
-
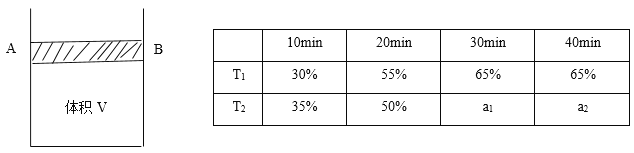
为了探究外界条件对反应aX(g)+bY(g)⇌cZ(g)的影响,以X和Y物质的量比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。以下判断正确的是( )
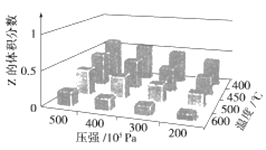
A. ΔH>0,ΔS>0
B. ΔH>0,ΔS<0
C. ΔH<0,ΔS>0
D. ΔH<0,ΔS<0
难度: 困难查看答案及解析
-
下列说法或表示方法中正确的是( )
A. 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B. 由C(金刚石)=C(石墨)ΔH=-1.9 kJ·mol-1可知,金刚石比石墨稳定
C. 在一定条件下,某可逆反应的ΔH=+100 kJ·mol-1,则该反应正反应活化能比逆反应活化能大100 kJ·mol-1
D. 己知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2。则ΔH1>ΔH2
难度: 中等查看答案及解析
-
下列说法正确的是( )
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率;
②电冶铝工业中用电解熔融状态氧化铝,用冰晶石作助熔剂的方法进行冶炼
③电解法精炼铜时,电路中每转移2 mol电子,阳极质量就减少64 g
④镀锌铁镀层破坏后锌仍能减缓铁腐蚀,其原理为牺牲阳极的阴极保护法
⑤第五套人民币的一元硬币材质为铜芯镀银,在电镀过程中,铜芯应做阳极
⑥外加电流的金属保护中,被保护的金属与电源的正极相连,发生氧化反应
A. ①②④ B. ①②③④ C. ①③⑤⑥ D. ③④⑥
难度: 中等查看答案及解析
-
(题文)有关下列四个常用电化学装置的叙述中,正确的是( )
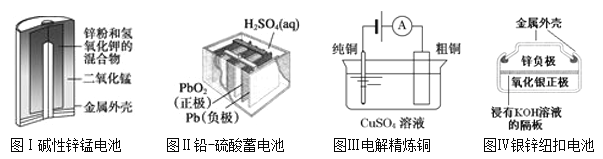
A. 图Ⅰ所示电池中,MnO2的作用是催化剂
B. 图Ⅱ所示电池放电过程中,硫酸浓度不断增大
C. 图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中被还原为Ag
难度: 中等查看答案及解析
-
下列事实或操作不符合平衡移动原理的是( )
A. 开启啤酒有泡沫逸出
B. 向FeCl3溶液中加KSCN,有FeCl3+3KSCN⇌3KCl+Fe(SCN)3(血红色)反应,平衡后向体系中加入KCl固体使体系红色变浅。
C. 装有NO2的烧瓶置于热水中颜色加深
D. 实验室用排饱和食盐水的方法收集氯气
难度: 中等查看答案及解析
-
在一恒温恒容容器中,发生反应:2A(g)+B(s) ⇌ C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个
①容器内B(s)物质的量浓度不变;②混合气体的密度不变;③混合气体的压强不变;④混合气体的平均相对分子质量不变;⑤C(g)的物质的量浓度不变;⑥容器内A、C、D三种气体的浓度之比为2:1:1;⑦某时刻v(A)=2v(C)且不等于零;⑧单位时间内生成n mol D,同时生成2n mol A
A. 3 B. 4 C. 5 D. 6
难度: 中等查看答案及解析
-
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图,已知断裂1 mol N≡N键吸收942kJ热量,生成1 mol N-N键释放167 kJ热量根据以上信息和数据,下列热化学方程式正确的是( )
A. 2N2=N4 △H =-882 kJ·mol-1
B. N2 (g)=0.5N4 (g) △H=+441 kJ
C. N2 (g)=0.5N4 (g) △H=-441 kJ·mol-1
D. 2N2(g)=N4(g) △H=+882 kJ·mol-1
难度: 困难查看答案及解析
-
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨和锂,含Li+导电固体为电解质。下列有关LiFePO4电池说法正确的是( )
A. 放电时电池正极反应为:FePO4+Li++e-=LiFePO4
B. 放电时电池内部Li+向负极移动
C. 充电过程中,电池正极材料的质量增加
D. 可加入硫酸以提高电解质的导电性
难度: 困难查看答案及解析
-
反应N2O4(g)
2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
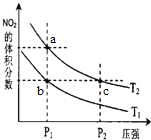
A. a、c两点的反应速率:a>c
B. a、c两点气体的颜色:a深,c浅
C. b、c两点的转化率:b>c
D. 由b点到a点,可以用加热的方法
难度: 困难查看答案及解析
-
某恒定温度下,在一个2L的密闭容器中充入A气体、B气体,测得其浓度为2mol/L和1mol·L-1;且发生如下反应:3A(g)+2B(g)
4C(?)+2D(?)已知“?”代表C、D状态未确定;反应一段时间后达到平衡,测得生成1.6molC,且反应前后压强比为5:4,则下列说法中正确的是( )
①该反应的化学平衡表达式为:K=
②此时B的转化率为35%
③增大该体系压强,平衡向右移动,但化学平衡常数不变.
④增加C的量,A、B转化率不变
A.①② B.②③ C.①④ D.③④
难度: 困难查看答案及解析
-
某同学组装了如图所示的电化学装置,则下列说法正确的是
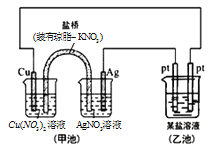
A. 图中甲池为原电池装置,Cu电极发生还原反应
B. 实验过程中,甲池左侧烧杯中
的浓度不变
C. 若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量会减小
D. 若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液可能是AgNO3溶液
难度: 困难查看答案及解析
-
短周期主族元素W、X、Y、Z原子序数依次增大,其中W元素原子的最外层电子数是内层电子数的两倍。X与Z同主族,两原子的核外电子数之和为24。Y的原子半径是所有短周期主族元素中最大的。下列说法正确的是( )
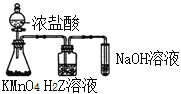
A. 简单离子半径:Z>Y>X
B. 如图所示实验可证明非金属性:Cl>Z
C. W、Y、Z的单质分别与X2反应时,X2用量不同产物均不同
D. Y分别与X、Z形成二元化合物中不可能存在共价键
难度: 中等查看答案及解析
-
下列图示与对应的叙述相符的是( )
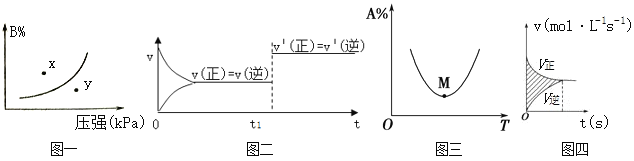
A. 图一表示反应:mA(s)+nB(g)⇌pC(g) △H>O,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的慢.
B. 图二是可逆反应:A(g)+B(s)⇌C(s)+D(g) △H>O的速率时间图像,在t1时刻改变条件一定是加入催化剂。
C. 图三表示对于化学反应mA(g)+nB(g) ⇌ pC(g)+qD(g),A的百分含量与温度(T)的变化情况,则该反应的ΔH>0。
D. 图四所示图中的阴影部分面积的含义是(v正-v逆)
难度: 困难查看答案及解析
-
NaClO2( 亚氯酸纳)是常用的消毒剂和漂白剂,工业上可采用电解法制备,工作原理如图所示。下列叙述正确的是
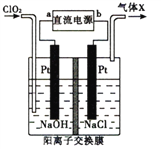
A. 若直流电源为铅蓄电池,则b极为Pb
B. 阳极反应式为ClO2+e-=ClO2-
C. 交换膜左测NaOH 的物质的量不变,气体X 为Cl2
D. 制备18.1g NaClO2时理论上有0.2molNa+由交换膜左侧向右侧迁移
难度: 中等查看答案及解析