-
Ⅰ.已知:2CO(g)+O2(g)=2CO2 (g) ΔH=-566.0 kJ·mol-1;键能EO=O=499.0 kJ·mol-1则CO(g)+O2(g)⇌CO2 (g)+O(g)的ΔH=______kJ·mol-1。
Ⅱ.汽车尾气净化的主要反应原理为2NO(g)+2CO(g)⇌2CO2(g)+N2(g)。将1.0 mol NO、0.8 mol CO充入2 L恒容密闭容器,分别在T1℃和T2℃下测得n(CO2)随时间(t)的变化曲线如下图所示。

(1)T2℃时,0~2s内的平均反应速率v(N2)= ________。
(2)该反应自发进行的条件(假设ΔH,ΔS不随温度变化而变化)___(高温自发,低温自发,任何温度均不自发,任何温度均自发)。
(3)为使该反应的反应速度增大,且平衡向正反方向移动的是________。
A.及时分离除CO2气体 B.适当升高温度
C.增大CO的浓度 D.选择高效催化剂
Ⅲ .工业可以采用下列反应合成甲醇:CO(g)+2H2(g) ⇌CH3OH(g),在一体积可变的密闭容器中(如图),将2 mol CO和3 mol H2放入容器中,移动活塞至体积为V L,用铆钉固定在A、B点,发生反应,测得在不同条件,不同时段内CO的转化率,得出下列数据。
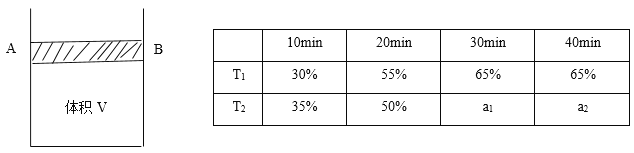
(1)根据上表数据,比较T1_______T2(选填“>、=、<”);T2温度下,第20 min时,反应达到平衡,该温度下的平衡常数为__________。
(2)T2温度下,第40 min时,拔出铆钉后,活塞没有发生移动,再向容器中通入6 mol的CO,此时V(正)________V(逆) (选填“>、=、<”),判断理由是:___________________。
-
处理燃烧产生的烟道气CO和SO2,方法之一是在一定条件下将其催化转化为CO2和S。
已知:①2CO(g)+O2(g) 2CO2(g) ∆H=-566.0kJ/mol
2CO2(g) ∆H=-566.0kJ/mol
②S(g)+O2(g) SO2(g) ∆H=-296.0kJ/mol
SO2(g) ∆H=-296.0kJ/mol
下列说法中正确的是
A. 转化①有利于碳参与自然界的元素循环
B. 转化②中S和O2属于不同的核素
C. 可用澄清的石灰水鉴别CO2与SO2
D. 转化的热化学方程式是:2CO(g)+ SO2(g)  S(s)+ 2CO2 (g) ∆H =+270kJ/mol
S(s)+ 2CO2 (g) ∆H =+270kJ/mol
-
处理燃烧产生的烟道气CO和SO2,方法之一在一定条件下将其催化转化为CO2和S。己知:①2CO(g)+O2(g)= 2CO2(g) △H =-566.0 kJ/mol ②S(s)+O2(g)=SO2(g) △H=-296.0 kJ/mol 下列说法中正确的是( )
A. 可用澄清的石灰水鉴别CO2与SO2
B. 转化②中S和O2属于不同的核素
C. 转化①有利于碳参与自然界的元素循环
D. 转化的热化学方程式是:2CO(g)+SO2(g)=S(s)+2CO2(g) △H=+270kJ/mol
-
下列关于热化学反应的描述中正确的是
A.CO(g)的燃烧热是283.0 kJ/mol,则表示CO燃烧热的热化学方程式为2CO(g)+O2(g)===2CO2 (g);△H=-566.0 kJ/mol
B.由石墨比金刚石稳定可知:C(金刚石,s)= C( 石墨,s);△H<0
石墨,s);△H<0
C.需要加热才能发生的反应一定是吸热反应
D.已知:2SO2 (g) + O2 (g) 2SO3 (g);△H =-98.3 kJ/mol。将1 m
2SO3 (g);△H =-98.3 kJ/mol。将1 m ol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ的热量
ol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ的热量
-
已知下列两个热化学方程式:2CO(g)+O2(g)=2CO2(g) △= - 586.7kJ·mol-1;
2H2(g)+O2(g)=2H2O(l) △= -571.6kJ·mol-1,实验测得:CO与H2的混合气体5.8g,完全燃烧时,放出的热量为87.25kJ,则混合气体中CO和H2的体积比为
A.1:1 B.2:1 C.2:3 D.1:3
-
已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)===Na2CO3(s)+ O2(g) ΔH=-226 kJ·mol-1
O2(g) ΔH=-226 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是( )
A. CO的燃烧热为283 kJ
B. 下图可表示由CO生成CO2的反应过程和能量关系
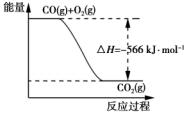
C. 2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-452 kJ·mol-1
D. CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
-
已知:
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)===Na2CO3(s)+ O2(g) ΔH=-266 kJ·mol-1
O2(g) ΔH=-266 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是
A.CO的燃烧热为283 kJ
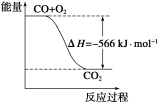
B.下图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-532kJ·mol-1
D.CO(g)与Na2O2(s)反应放出549 kJ热量时,电子转移数为6.02×1023
-
下列说法正确的是
A. 1mol H2与0.5 mol O2反应放出的热就是H2的燃烧热
B. 已知2CO2(g)=2CO(g)+O2(g)△H=+566 kJ/mol ,则CO的燃烧热ΔH =-283.0kJ/mol
C. H2SO4与Ba(OH)2反应生成1molH2O时放出的热叫做中和热
D. 已知H+(aq)+OH–(aq)=H2O(1) △H = -57.3kJ·mol-1,则任何酸碱中和的反应热均为57.3kJ
-
已知:
2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=-266 kJ·mol-1
O2(g) ΔH=-266 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的标准燃烧热为283 kJ
B.下图可表示由CO生成CO2的反应过程和能量关系
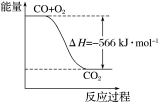
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-532 kJ·mol-1
D.CO(g)与Na2O2(s)反应放出549 kJ热量时,电子转移数为6.02×1023
-
已知:2CO(g)+O2(g)=2CO2(g) △H=-566kJ/mol Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) △H=-226kJ/mol。根据以上热化学方程式判断,下列说法正确的是( )
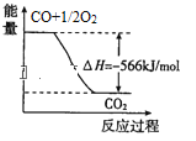
A. CO的燃烧热为566kJ/mol
B. 上图可表示由CO生成CO2的反应过程和能量关系
C. 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) △H>-452kJ/mol
D. CO2 (g)与Na2O2(s)反应放出452kJ热量时,转移电子个数为6.02×1023





