-
造成大气污染的SO2主要来源于
A.自然界硫化物分解 B.火山喷发
C.汽车排出的废气 D.大量含硫燃料燃烧
难度: 简单查看答案及解析
-
在空气中不易变质的是
A.Na2SO3 B.NaHSO4 C.亚硫酸 D.氢硫酸
难度: 简单查看答案及解析
-
不能由单质直接化合而得到的化合物是
A.FeCl3 B.SO2 C. CuS D.FeS
难度: 简单查看答案及解析
-
下列气体中最易液化,适宜做致冷剂的是
A.N2 B.NH3 C.SO2 D.HCl
难度: 简单查看答案及解析
-
硒(Se)位于周期表中第4周期、第ⅥA族,根据它在周期表中的位置推测,硒不可能具有的性质是
A.硒元素有+6、+4、-2等常见化合价 B.SeO3的水化合物是一种含氧酸
C.H2Se的热稳定性比 H2S的稳定性强 D.Se的单质在常温下呈固态
难度: 简单查看答案及解析
-
硫的非金属性比氧弱,但从以下的事实不能做出判断的是
A.硫化氢不如水稳定
B.硫化氢的水溶液露置在空气中变浑浊
C.硫跟氢气反应需要加热,而氧气跟氢气反应只需点燃
D.硫是固体,氧气在常温下是气体
难度: 简单查看答案及解析
-
下列对SO2和SO3的叙述正确的是
A.通常条件下都是无色气体,都易溶于水
B.都是酸性氧化物,其水溶液都是强酸
C.都可使品红溶液褪色
D.都能与碱溶液反应
难度: 简单查看答案及解析
-
质量百分含量为25%的氨水用等体积的水稀释后,所得溶液的溶质质量分数
A.等于12.5% B.大于12.5% C.小于12.5% D.无法确定
难度: 简单查看答案及解析
-
下列关于磷的叙述正确的是
A.红磷没有毒性而白磷有剧毒 B.白磷在空气中加热到260 ℃转为红磷
C.白磷可用于制安全火柴 D.白磷不能保存在水中
难度: 简单查看答案及解析
-
下列关于浓HNO3与浓H2SO4的叙述正确的是
A.常温下都可用锌制容器贮存 B.常温下都能与铜较快反应
C.都易挥发 D.露置于空气中,溶液浓度均降低
难度: 简单查看答案及解析
-
下列变化中,属于物理变化的是:①红磷加热升华变成白磷 ②氯化铵晶体受热后由试管底部移到试管上部 ③固体碘受热变成碘蒸气 ④干冰汽化 ⑤浓硝酸从无色液体变成黄色液体
A.①② B.③④ C.④⑤ D.③④⑤
难度: 简单查看答案及解析
-
Cu粉放入稀硫酸中,加热后无明显现象,当加入一种盐后,Cu粉质量减少,而溶液变蓝,同时有气体生成,此盐是
A.氯化物 B.硫酸盐 C.硝酸盐 D.磷酸盐
难度: 简单查看答案及解析
-
右图装置可用于
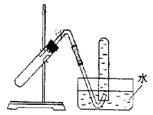
A.加热NaHCO3制CO2
B.用Cu与稀HNO3反应制NO
C.用NH4Cl与浓NaOH溶液反应制NH3
D.用NaCl与浓H2SO4反应制HCl
难度: 简单查看答案及解析
-
用下列气体和溶液进行喷泉实验,最终液体不能充满烧瓶的是
A.CO2和NaOH溶液 B.NH3和水 C.Cl2和NaOH溶液 D.NO2和水
难度: 简单查看答案及解析
-
下列物质中,只能跟NaOH溶液作用,不能跟盐酸作用的是
A.NaHSO4 B.Na2SO3 C.Al(OH)3 D.NH4HCO3
难度: 简单查看答案及解析
-
下列排列顺序正确的是:
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O
③酸性:H3PO4>H2AsO4>H2SO4 ④离子半径:O2->F->Mg2+
A.①③ B.②④ C.①④ D.②③
难度: 简单查看答案及解析
-
下列各组分子中,都属于含有极性键的非极性分子的一组是
A.CO2,H2O B.CO2、CH4 C.Cl2、CS2 D.NH3、HCl
难度: 简单查看答案及解析
-
下列叙述不正确的是
A.阳离子N5+中的氮原子间以共价键结合
B.O2-半径比F-的小
C.1 1H、2 1H、13H是氢的三种同位素
D.氯化氢溶于水需要破坏化学键
难度: 简单查看答案及解析
-
下列叙述中错误的是
A.将SO2气体通入足量的Ba(OH)2溶液中有白色沉淀生成
B.将SO2气体通入BaCl2溶液中有白色沉淀生成
C.将SO2气体通入用硝酸酸化的BaCl2溶液中有白色沉淀生成
D.将HNO3酸化后的BaCl2溶液加入含某种离子的溶液中有白色沉淀生成,不能判断该溶液中一定存在SO42-
难度: 简单查看答案及解析
-
13克锌与足量的稀硫酸反应后,得到的氢气若在空气中完全燃烧,能生成水的质量为
A.14.4克 B.9克 C.7.2克 D.3.6克
难度: 简单查看答案及解析
-
24 mL 0.05 mol/L的Na2SO3溶液,恰好与20mL 0.02 mol/L的K2Cr2O7溶液完全反应,则Cr在还原产物中的化合价是
A.+6 B.+3 C.+2 D.0
难度: 简单查看答案及解析
-
盛满等体积的NO和NO2的混合气体的试管,倒置在水槽中,反应完毕后,液面上升的高度是试管高度的
A.1/2 B.1/3 C.2/3 D.5/6
难度: 简单查看答案及解析
-
26gZn和63gHNO3的稀溶液恰好完全反应,得到的还原产物的相对分子质量可能为:
A.30 B.28 C.46 D.80
难度: 简单查看答案及解析
-
将3. 84克铜粉与一定质量浓硝酸反应,当铜完全作用时,收集到气体2.24L(标况下),则所消耗硝酸的物质的量是
A.0.11mol B.0.22mol C.0.16mol D.0.1mol
难度: 简单查看答案及解析
-
把含有(NH4)2SO4、NH4NO3的混合溶液a L分为两等份,一份中加入b mol KOH刚好把NH+4全部转化为NH3,另一份中加入c mol BaCl2恰好使沉淀完全,则原混合溶液中NO-3浓度是
A.
mol·L-1 B.
mol·L-1
C.
mol·L-1 D.
mol·L-1
难度: 简单查看答案及解析