-
下列属于化学变化的是( )
A.蔗糖溶解
B.滴水成冰
C.花香四溢
D.铁器生锈难度: 中等查看答案及解析
-
下列属于纯净物的是( )
A.液态氧
B.加碘盐
C.酸牛奶
D.不锈钢难度: 中等查看答案及解析
-
下列属于化学能转化为其它能量的是( )
A.
水力发电
B.
电解水
C.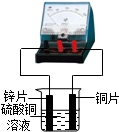
化学电池
D.
太阳能供热难度: 中等查看答案及解析
-
下列做法与社会可持续发展理念相违背的是( )
A.将工业废水注入地下,治理水污染
B.研发可降解的塑料,减少“白色污染”
C.开发新能源,代替化石燃料
D.推行自行车、公交车等出行方式,减少“碳”排放难度: 中等查看答案及解析
-
下列归类错误的是( )
选项 归类 物质 A 化石燃料 煤、石油、天然气 B 同一物质 烧碱、火碱、纯碱 C 营养物质 淀粉、蛋白质、油脂 D 复合材料 汽车轮胎、玻璃钢、钢筋混凝土
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
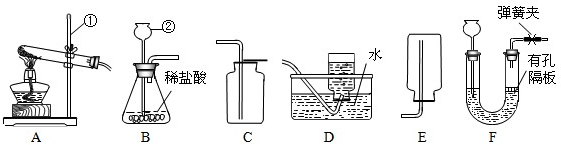
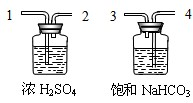
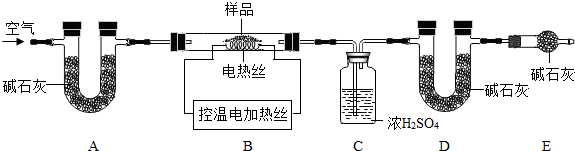
按下列装置实验,不能达到对应目的是( )
A.收集H2
B.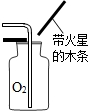
O2验满
C.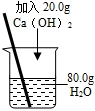
配制20%的Ca(OH)2溶液
D.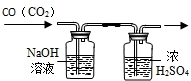
除去CO中的CO2难度: 中等查看答案及解析
-
下列做法正确的是( )
A.用聚氯乙烯包装食品
B.常用钢丝球洗刷铝锅,使之光亮、耐用
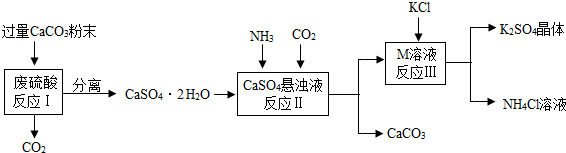
C.将草木灰(含K2CO3)与氯化铵混合施用,增进肥效
D.利用石灰乳和硫酸铜溶液配制波尔多液难度: 中等查看答案及解析
-
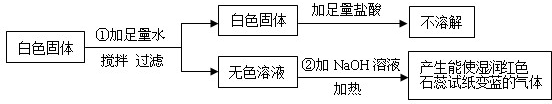
下列做法错误的是( )
A.用灼烧的方法区别棉花和羊毛
B.用润湿的pH试纸测白醋的pH
C.用水鉴别NH4NO3、NaOH、NaCl三种固体
D.按溶解、过滤、蒸发的主要操作顺序分离CaCl2、CaCO3的固体混合物难度: 中等查看答案及解析
-
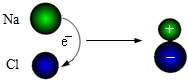
甲和乙反应可制备燃料丙,其微观示意图如下.下列说法错误的是( )
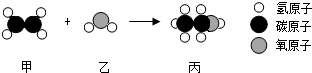
A.该反应属于化合反应
B.该反应中分子和原子的种类都发生了改变
C.甲、丙是有机物,乙是氧化物
D.甲、丙分别在氧气中完全燃烧,产物相同难度: 中等查看答案及解析
-
下列实验操作或现象的描述正确的是( )
A.将50.0mL酒精与50.0mL蒸馏水混合,所得溶液体积小于100.0mL
B.向加碘食盐溶液中滴加淀粉,溶液变蓝
C.“粗盐提纯”实验中,过滤时将悬浊液直接倒入漏斗
D.硫在空气中燃烧发出明亮蓝紫色火焰,生成无色无味气体点燃难度: 中等查看答案及解析
-
下列化学方程式能正确表示所述内容的是( )
A.铁丝在氧气中燃烧:4Fe+3O22Fe2O3
B.实验室制备CO2:CaCO3CaO+CO2↑
C.盐酸除铁锈:Fe2O3+6HCl═2FeCl3+3H2O
D.CO2通入CaCl2溶液中:CO2+CaCl2+H2O═CaCO3↓+2HCl难度: 中等查看答案及解析
-
下列推理正确的是( )
A.向某无色溶液中滴加酚酞无现象,则溶液一定呈中性
B.酸雨的pH小于7,pH小于7的雨水不一定是酸雨
C.在同一化合物中,金属元素显正价,则非金属元素一定显负价
D.酸碱中和反应生成盐和水,则生成盐和水的反应一定是中和反应难度: 中等查看答案及解析
-
下列除杂设计(括号内为杂质)所选用试剂和操作都正确的是( )
序号 物 质 选用试剂 操作 A CO2(CO) O2 点燃 B NaOH溶液(Na2CO3) 稀盐酸 加入试剂至不再产生气泡 C KNO3溶液(KOH) Cu(NO3)2溶液 加入适量的试剂,直接蒸发 D 蛋白质固体(蔗糖) H2O、
饱和(NH4)2SO4溶液溶解、盐析、过滤、
洗涤、低温干燥
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
下列各组转化中,一定条件下均能一步实现的组合是( )
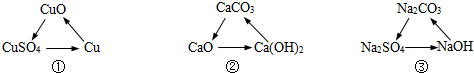
A.①②
B.②③
C.①③
D.①②③难度: 中等查看答案及解析
-
工业上以CaO和HNO3为原料制备Ca(NO3)2•6H2O晶体.为确保制备过程中既不补充水,也无多余的水,所用硝酸的溶质质量分数约为( )
A.41.2%
B.53.8%
C.58.3%
D.70.0%难度: 中等查看答案及解析
-
下列说法正确的是( )
A.氯化钠溶液会加快钢铁的锈蚀
B.洗洁精和汽油都能清洗油污,且原理相同
C.高炉炼铁中所需的高温和CO的生成都与焦炭有关
D.为了加强食品的色、香、味,可以大量使用添加剂难度: 中等查看答案及解析
-
20℃时,将等质量的甲、乙固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3.
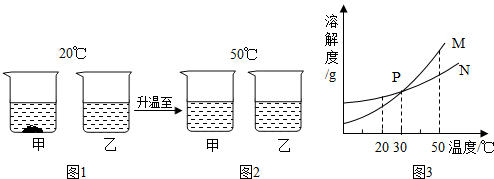
下列说法正确的是( )
A.图1中乙溶液一定不饱和
B.图2中两溶液中溶质质量分数一定相等
C.图3中N表示甲的溶解度曲线
D.图2中两溶液降温至30℃一定都不会析出晶体难度: 中等查看答案及解析
-
下列各组溶液,不用其他试剂不能鉴别出来的是( )
A.Na2CO3、稀H2SO4、稀HCl、KNO3
B.稀HCl、Na2CO3、BaCl2、Na2SO4
C.NaOH、Na2CO3、酚酞、CaCl2
D.CuSO4、NaOH、BaCl2、NaCl难度: 中等查看答案及解析
-
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是( )
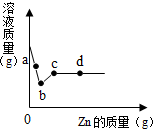
A.a点溶液中的溶质有2种
B.c点溶液中溶质为Zn(NO3)2
C.若取b~c段溶液,滴加稀盐酸,有白色沉淀
D.取d点的固体,加入稀盐酸,无气泡产生难度: 中等查看答案及解析
-
已知:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O.有关CuSO4制备途径及性质如图所示.
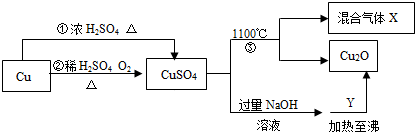
下列说法正确的是( )
A.途径①比途径②更好地体现绿色化学思想
B.反应③分解所得混合气体X是SO2和SO3
C.反应③中有三种元素化合价发生变化
D.Y可以是葡萄糖,利用此反应可以检验病人是否患有糖尿病难度: 中等查看答案及解析