-
有x、y、z三种金属,如果把x和y分别放入稀硫酸中,x溶解并产生氢气,而y不反应;如果把y和z分别放入硝酸银溶液中,过一会儿,在y表面有银析出,而z没有变化.根据以上实验事实,判断x、y和z的金属活动顺序正确的是( )
A.x>y>z B.x>z>y C.z>y>x D.z>x>y
难度: 简单查看答案及解析
-
市售的某种含氟(F)牙膏中有一种化学药物的化学式为Na2FPO3,已知F为﹣1价,则P元素的化合价为( )
A.+5 B.+3 C.+1 D.﹣3
难度: 困难查看答案及解析
-
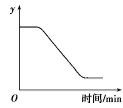
已知:2KClO3
2KCl+3O 2↑,下图表示一定质量的KClO3和MnO 2固体混合物受热过程中,某变量y随时间的变化趋势。纵坐标表示的是
A.固体中氧元素的质量
B.生成O 2的质量
C.固体中MnO 2的质量
D.固体中钾元素的质量分数
难度: 中等查看答案及解析
-
实验室常用如图所示装置探究可燃物的燃烧条件.下列说法错误的是
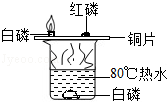
A.烧杯中的热水只起到加热作用
B.水中的白磷不能燃烧,是因为白磷没有与空气接触
C.对准烧杯中的白磷通入氧气,热水中的白磷能燃烧
D.铜片上的红磷不能燃烧,是因为温度没有达到着火点
难度: 简单查看答案及解析
 B. 加热液体
B. 加热液体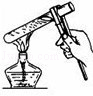
 D. 检查装置气密性
D. 检查装置气密性