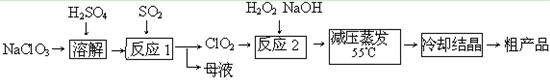
-
“化学,我们的生活,我们的未来”是2011年“国际化学年”的主题。你认
为下列行为中,不符合这一主题的是
A.控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源
B.研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展
C.开发太阳能、水能、风能等新能源、减少使用煤、石油等化石燃料
D.实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使
用(Reuse)、提高资源的循环利用(Recycle)
难度: 中等查看答案及解析
-
六氟化硫分子呈正八面体,常温下难以水解,在高电压下仍有良好的绝缘性,在电器工业有着广泛用途,但逸散到空气中会引起强温室效应。下列有关SF6的推测正确的是
A.SF6易燃烧生成二氧化硫
B.SF6中各原子均达到8电子稳定结构
C.高温条件下,SF6微弱水解生成H2SO4和HF
D.SF6是极性分子
难度: 中等查看答案及解析
-
下列叙述不正确的是
A.有化学键断裂的变化不一定是化学变化
B.水受热不易分解,与水分子之间存在的氢键无关
C.熔化状态下能导电的物质不一定是离子晶体
D.易溶于水的物质一定是电解质
难度: 中等查看答案及解析
-
从下列事实所得出的相应结论正确的是
实 验 事 实
结 论
①
Cl2的水溶液可以导电
Cl2是电解质
②
将燃烧的镁条放入CO2中能继续燃烧
还原性:Mg>C
③
NaHCO3溶液与NaAlO2溶液混合产生白色沉淀
酸性:HCO3->Al(OH)3
④
常温下白磷可自燃而氮气须在放电时才与氧气反应
非金属性:P>N
⑤
某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝
该溶液一定有NH4+
A.③④⑤ B.②③⑤ C. ①②③ D. 全部
难度: 中等查看答案及解析
-
2010年诺贝尔化学奖授予美日科学家,他们由于研究“有机物合成过程中
钯催化交叉偶联”而获奖。钯的化合物氯化钯可用来检测有毒气体CO,发生反
应的化学方程式为:CO+PdCl2 +H2O =CO2 +Pd↓ +2HC1。
下列说法正确的是
A.题述反应条件下还原性:CO> Pd
B.题述反应中PdCl2被氧化
C.生成22.4 LCO2时,转移的电子为2 mo1
D.CO气体只有在高温下才能表现还原性
难度: 中等查看答案及解析
-
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的几种。现取该溶液进行实验,得到如下实验现象:①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。据此可以推断,该溶液中肯定不存在的离子是
A.Al3+、CO32-、Br-、SO32- B.Mg2+、Na+、CO32-、I-
C.Al3+、Na+、SO32-、I- D. Al3+、Mg2+、I-、SO32-
难度: 中等查看答案及解析
-
关于下列图示的说法中,正确的是
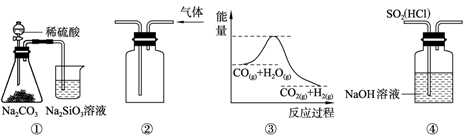
A.图①所示实验可比较硫、碳、硅三种元素的非金属性强弱
B.用图②所示实验装置排空气法收集CO2气体
C.图③表示可逆反应CO(g)+H2O(g)
CO2(g)+H2(g)的ΔH大于0
D.图④ 装置可以用来除去SO2中的HCl
难度: 中等查看答案及解析
-
A、B、C为三种短周期元素,A、B在同周期,A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构。下列说法中正确的是
A.原子序数: B>A>C B.原子半径:A>B>C
C.离子半径:A2->C->B2+ D.原子核外最外层电子数:A>C>B
难度: 中等查看答案及解析