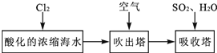
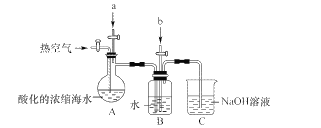
-
a、b、c、d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c。下列叙述错误的是( )
A. d元素的非金属性最强
B. 它们均存在两种或两种以上的氧化物
C. 只有a与其他元素生成的化合物都是离子化合物
D. b、c、d与氢形成的化合物中化学键均为极性共价键
难度: 中等查看答案及解析
-
某元素最高价氧化物对应水化物的化学式是H2XO3,则其气态氢化物的化学式为( )
A. HX B. H2X C. XH3 D. XH4
难度: 简单查看答案及解析
-
糖类、油脂、蛋白质是人类生活的基本营养物质,下列叙述正确的是
A. 豆油长期放置变质是因为发生了加成反应
B. 食物中含有的纤维素,可在人体内直接水解成葡萄糖
C. 糖类、油脂、蛋白质都是天然有机高分子化合物
D. 棉麻、蚕丝织品可通过灼烧时产生的气味来进行鉴别
难度: 简单查看答案及解析
-
下列物质中,既含有离子键又含有共价键的是
A. NaCl B. C2H4 C. NaOH D. CaCl2
难度: 简单查看答案及解析
-
下列有关化学用语使用正确的是
A. HC1的电子式:
B. CO2的比例模型:
C. 乙酸的分子式:CH3COOH D. 甲烷的实验式为CH4
难度: 简单查看答案及解析
-
下列分子式表示的不一定是纯净物的是
A. C3H7Cl B. CH2Cl2 C. CHCl3 D. C3H8
难度: 简单查看答案及解析
-
下列有关烷烃的叙述中,错误的是
A. 烷烃分子中,所有的化学键都是单键
B. 分子通式为CnH2n+2的烃一定是烷烃
C. 正丁烷和异丁烷分子中共价键数目相同
D. 烷烃中除甲烷外,很多都能使酸性KMn04溶液的紫色褪去
难度: 简单查看答案及解析
-
下列结论错误的是
A. 氢化物稳定性:HF>H2S>PH3
B. 离子还原性:S2- >Cl- >Br->I-
C. 酸性:H2SO4>HClO
D. 碱性强弱:KOH>NaOH>Mg(OH)2
难度: 简单查看答案及解析
-
16O和18O是不同的核素,下列说法正确的是
A. 16O2和18O2的物理性质、化学性质均相同
B. 4. 48L18O2含有4NA个中子(NA表示阿伏伽德罗常数的值)
C. 16O2和18O2互为同位素
D. 36 g18O2含有16 mol电子
难度: 简单查看答案及解析
-
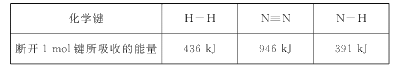
下列说法正确的是
A. 化学反应发生过程中一定伴随着能量变化
B. 吸热反应一定需要加热才能进行
C. 化学反应释放的能量一定是热能
D. 有化学键断裂的变化一定是化学变化
难度: 简单查看答案及解析
-
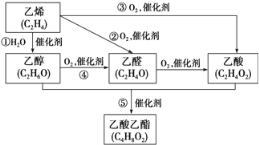
“绿色化学”要求原料物质中所有的原子完全被利用,全部转入到期望的产品中,工业上由C2H4(乙烯)合成C4H802(乙酸乙酯)的过程中,为使原子利用率达到100%,在催化剂作用下还需加入的反应物是
A. CH3COOH B. H2O和CO C. O2和H2 D. CO2
难度: 简单查看答案及解析
-
N2+3H2
2NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
A. 达到平衡时,反应速率:v(正)=v(逆)=0
B. 恒温恒压下,充入少量He,反应速率减慢
C. 升温正反应速率加快,逆反应速率减慢
D. 若在反应的密闭容器加入1 mol N2和过量的H2,最后能生成2 mol NH3
难度: 简单查看答案及解析
-
下列实验能获得成功的是
A. 苯和浓溴水混合,加入铁作催化剂制溴苯
B. 除去乙烷中的乙烯,将混合气体通过盛有酸性KMnO4溶液的洗气瓶
C. 向蔗糖水解后的液体中加入新制的Cu(OH)2悬浊液,加热至沸腾,验证水解产物为葡萄糖
D. 用NaHCO3溶液鉴别乙醇和乙酸
难度: 简单查看答案及解析
-
下列叙述正确的是
A. 活泼金属钠用电解法冶炼 B. 铜只能用电解法冶炼得到
C. 汞的冶炼只能用热还原法 D. 用铝热法冶炼铝
难度: 简单查看答案及解析
-
下列各组变化类型相同的是
A. 干馏和分馏 B. 裂化和裂解
C. 煤的气化和海水的蒸馏 D. 蛋白质的变性和盐析
难度: 简单查看答案及解析
-
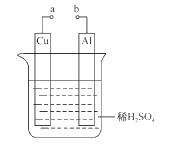
铜 - 锌原电池如图所示,电解质溶液为硫酸铜溶液,电池工作一段时间后,下列说法错误的是
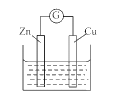
A. 锌电极上的反应为Zn- 2e-=Zn2+
B. 溶液中的SO42-向锌电极移动
C. 电子从锌电极经过硫酸铜溶液流向铜电极
D. 铜电极质量增加
难度: 简单查看答案及解析
-
下列关于共价化合物和离子化合物说法正确的是
A. 只含共价键的物质一定是共价化合物
B. 离子化合物都能溶于水,且熔点一般都较高
C. 全由非金属元素组成的化合物中可能含有离子键
D. 气态单质分子中一定含有非极性共价键
难度: 简单查看答案及解析
-
在铁片与100 mL0.1 mol/L的稀盐酸反应中,为了减慢此反应速率而不改变H2的产量,下列方法错误的是
①加KN03溶液 ②加入少量醋酸钠固体
③加NaCl溶液 ④滴入几滴硫酸铜溶液
A. ①② B. ②③ C. ③④ D. ①④
难度: 简单查看答案及解析
-
把a、b、c三块金属片浸在稀硫酸中,用导线两两连接可以组成原电池,若a、b相连时b为负极;a、c相连时a极上产生大量气泡;b、c相连时,电流由b到c。则这三种金属的活动性顺序由大到小为
A. a>c>b B. c>b>a C. a>b>c D. b>c>a
难度: 简单查看答案及解析
-
下列叙述正确的是
A. 等质量的甲烷和乙烯完全燃烧,甲烷消耗的O2多
B. C5H11Cl有6种同分异构体
C. 聚乙烯与乙烯性质相似,可使溴水褪色
D. 正丁烷和异丁烷互为同系物
难度: 简单查看答案及解析
-
下列由实验得出的结论正确的是( )
实验
结论
A.
某有机物完全燃烧,只生成CO2和H2O
该有机物属于烃类物质
B.
乙醇和水都可与金属钠反应产生可燃性气体
乙醇分子中的氢与水分子中的氢具有相同的活性
C.
用乙酸浸泡水壶中的水垢,可将其清除
乙酸的酸性强于于碳酸的酸性
D.
甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红
生产的氯甲烷具有酸性
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(g)+xB(g)=2C(g),2 min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果正确的是
A. 平衡时,容器内的压强是起始时的
B. x值等于3
C. A的转化率为20%
D. B的平均反应速率为0.4 mol·L-1·min-l
难度: 简单查看答案及解析
-
中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。C02可转化成有机物实现碳循环。恒温恒容下反应:C02(g)+3H2(g)=CH3OH(g)+H2O(g),能说明上述反应达到平衡状态的是
A. 反应中C02与CH3OH的物质的量浓度之比为1:1
B. 混合气体的密度不随时间的变化而变化
C. 单位时间内消耗3 molH2,同时生成1 molH2O
D. C02的体积分数在混合气体中保持不变
难度: 简单查看答案及解析
-
阿波罗宇宙飞船上使用的是氢氧燃料电池,其电极总反应式为:2H2+O2=2H2O;电解质溶液为KOH溶液,反应保持在较高温度,使水蒸发,下列叙述正确的是
A. 电池工作时K+向负极移动
B. 工作时电解质溶液中的OH-的物质的量不断增加
C. 正极电极反应式为:2O2+4e-+4H+=4OH-
D. 工作时负极有水产生
难度: 简单查看答案及解析