-
“纳米材料”是当今材料科学研究的前沿,1纳米(nm)=10-9 m,其研究成果广泛应用于催化及军事科学中。“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料。如将“纳米材料”分散到蒸馏水中,所得混合物可能具有的性质是
A.有丁达尔效应
B.该分散系放置一段时间可能很快出现分层现象
C.不能透过滤纸
D.所得分散系一定是浊液
难度: 简单查看答案及解析
-
下列现象与胶体知识无关的是
A.夏日的傍晚常常看到万丈霞光穿云而过美不胜收
B.向碳酸氢钠溶液中加入氯化钙溶液时溶液没有浑浊
C.食品加工厂利用豆浆中加入盐卤做豆腐
D.某化工厂利用静电除尘技术去除废气中的固体悬浮物
难度: 中等查看答案及解析
-
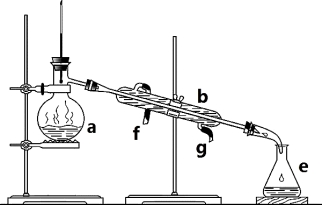
下列实验操作中错误的是
A.蒸发操作时,不能使混合物中的水分完全蒸干后才停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
难度: 中等查看答案及解析
-
下列常用实验仪器中,不能直接用于混合物的分离或提纯的是
A.分液漏斗 B.漏斗 C.蒸馏烧瓶 D.容量瓶
难度: 简单查看答案及解析
-
容量瓶上标有①压强 ②刻度线 ③浓度 ④容量 ⑤温度等项中的
A.①③⑤ B.②④⑤ C.①②③ D.③④⑤
难度: 简单查看答案及解析
-
胶体区别于其它分散系的本质特征是
A.胶体的分散质粒子能透过滤纸
B.胶体能产生丁达尔现象
C.胶体的分散质粒子直径在1~100 nm之间
D.胶体是纯净物,其它分散系是混合物
难度: 中等查看答案及解析
-
质量相同的N2和CO,下列物理量不一定相同的是
A.物质的量 B.分子个数 C.原子个数 D.气体体积
难度: 中等查看答案及解析
-
已知气体的密度与它的摩尔质量成正比。一只气球若放在空气(空气的平均摩尔质量是29 g·mol-1)中可静止不动,那么在相同条件下该气球放在下列气体中会下沉的是
A.O2 B.Cl2 C.CO2 D.CH4
难度: 困难查看答案及解析
-
下列物质属于电解质且能够导电的是
A.固体NaCl B.熔融的NaOH C.NaCl溶液 D.液态氯化氢
难度: 中等查看答案及解析
-
能正确表示下列化学反应的离子方程式的是
A.氢氧化钠溶液与盐酸的反应 : OH—+H+ = H2O
B.澄清的石灰水与稀盐酸反应: Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C.铜片插入硝酸银溶液中: Cu + Ag+ = Cu2+ + Ag
D.碳酸钙溶于稀盐酸中: CaCO3+2H+=Ca2++H2CO3
难度: 中等查看答案及解析
-
下列说法正确的是
A. 在标准状况下,1mol水的体积是22.4L
B. 1molH2所占的体积一定是22.4L
C. 在标准状况下,NA个任何分子所占的体积约为22.4L
D. 在标准状况下,总质量为28g的N2和CO的混合气体,其体积约为22.4L
难度: 中等查看答案及解析
-
实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是
A.950 mL 111.2 g B.500 mL 117 g
C.1000 mL 117 g D.任意规格 111.2 g
难度: 中等查看答案及解析
-
下列说法正确的是
A.氢气的摩尔质量是2g B.摩尔是物质的质量单位
C.1molOH—的质量是17g D.1mol气体所占的体积约为22.4L
难度: 简单查看答案及解析
-
在下列反应中, HCl 作氧化剂的是
A.NaOH + HCl = NaCl + H2O
B.Zn + 2HCl = ZnCl2 + H2↑
C.MnO2 +4HCl(浓)
MnCl2+2H2O+Cl2↑
D.CuO + 2HCl = CuCl2 + H2O
难度: 简单查看答案及解析
-
下列溶液中,与100 ml 0.5 mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是
A.100 ml 0.5 mol/L MgCl2 溶液 B.200 ml 0.25 mol/L HCl溶液
C.50 ml 1 mol/L NaCl溶液 D.200 ml 0.25 mol/L CaCl2溶液
难度: 中等查看答案及解析
-
下列离子可以大量共存且溶液是无色的离子组是
A.H+、Na+、NO3-、Cu2+ B.Ba2+、Mg2+、Cl-、SO42-
C.NO3-、SO42-、K+、Mg2+ D.Mg2+、K+、OH-、NO3-
难度: 中等查看答案及解析
-
某元素在化学反应中由化合态变为游离态,则该元素
A.一定被氧化 B.一定被还原
C.既可能被氧化,也可能被还原 D.以上都不是
难度: 中等查看答案及解析
-
下列四种基本类型的反应中,一定不是氧化还原反应的是
A.复分解反应 B.分解反应 C.化合反应 D.置换反应
难度: 中等查看答案及解析
-
将5 mol·L-1的盐酸10 mL稀释到200 mL,再取出5 mL溶液的物质的量浓度是
A.0.05 mol·L-1 B.0.25 mol·L-1 C.0.10 mol·L-1 D.0.50 mol·L-1
难度: 简单查看答案及解析
-
下列化学方程式中,不能用离子方程式H++OH-=H2O表示的是
A.2NaOH + H2SO4 = Na2SO4 + 2H2O
B. Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
C.Ba(OH)2 + 2HCl = BaCl2 + 2H2O
D.KOH + HCl = KCL + H2O
难度: 中等查看答案及解析