-
下列设备工作时,将化学能转化为热能的是
A.硅太阳能电池

B.锂离子电池

C.太阳能集热器

D.燃气灶

难度: 简单查看答案及解析
-
某学生的实验报告所列出的下列数据中合理的是
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL
难度: 简单查看答案及解析
-
把A、B、C、D四块金属泡在稀硫酸中,用导线两两相连可以组成各种原电池,若A、B相连时,A为负极;C、D相连时,D上有气泡逸出;A、C相连时,A极减轻;B、D相连时,B为正极。则四种金属的活泼性顺序由大到小排列为
A.A>B>C>D B.A>C>B>D
C.A>C>D>B D.B>D>C>A
难度: 中等查看答案及解析
-
下列溶液一定是碱性的是
A.pH=8的某电解质的溶液 B.c(OH-)>1×10-7mol/L
C.溶液中含有OH- D.溶液中c(OH-)>c(H+)
难度: 简单查看答案及解析
-
0.1mol/L的K2S溶液中,有关粒子的浓度大小关系正确的是
A.c(K+)+c(H+)=c(S2—)+c(HS—)+c(OH—) B.c(H+)= c(OH—)
C.c(K+)=c(S2—)+c(HS—)+c(H2S) D.c(OH-)=c(H+)+c(HS—)+2c(H2S)
难度: 中等查看答案及解析
-
将等质量的两份锌粉a、b分别加入过量的稀硫酸。同时向a中加入少量CuSO4溶液。图中产生H2的体积V L与时间t min的关系正确的是
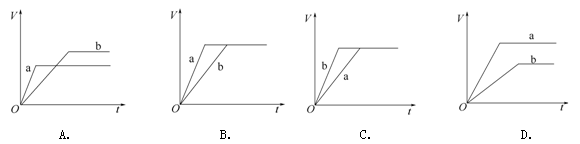
难度: 中等查看答案及解析
-
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH
CH3COO-+H+ 对于该平衡,下列叙述正确的是
A.加入少量NaOH固体,平衡向逆反应方向移动
B.升高温度,平衡向正反应方向移动
C.加入水稀释,溶液中c(H+)一定增大
D.加入少量CH3COONa固体,平衡向正反应方向移动
难度: 简单查看答案及解析
-
在298K、100kPa时,已知:
2H2O(g)=O2(g)+2H2(g) ΔH1
Cl2(g)+H2 (g)=2HCl(g) ΔH2
2Cl2(g)+2 H2O (g)=4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是
A.ΔH3=ΔH1+2ΔH2 B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2 D.ΔH3=ΔH1-ΔH2
难度: 中等查看答案及解析
-
某原电池的电池反应为:Fe+2Fe3+===3Fe2+,与此电池反应不符的原电池是
A.铜片、铁片、FeCl3溶液组成的原电池
B.石墨、铁片、Fe(NO3)3溶液组成的原电池
C.铁片、锌片、Fe2(SO4)3溶液组成的原电池
D.铜片、铁片、Fe(NO3)3溶液组成的原电池
难度: 简单查看答案及解析
-
常温下,把pH=2的H2SO4和pH=11的NaOH溶液混和,若使混和液pH=7,则酸与碱溶液的体积比是
A.10:1 B.1:10 C.1:2 D.2:1
难度: 中等查看答案及解析
-
Ksp(AgCl)=1.56×10-10 ,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12 ,已知,某溶液中含有C1-, Br- 和CrO42-,浓度均为0.010mo1·L-,向该溶液中逐滴加入0.010mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
A.C1- 、Br-、CrO42- B.CrO42-、Br-、C1-
C.Br-、C1-、CrO42- D.Br- 、CrO42-、C1-
难度: 中等查看答案及解析
-
对于密闭容器中进行的反应CO(g) + H2O(g)
CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
A.正反应速率增大
B.逆反应速率减小
C.达到平衡时,逆反应速率比原平衡要大
D.化学平衡常数不变
难度: 简单查看答案及解析
-
在蒸发皿中加热蒸干下列物质的溶液,再灼烧(溶液低于400℃)可以得到原溶质固体的是
A.AlCl3 B.NaHCO3 C.MgSO4 D.KMnO4
难度: 中等查看答案及解析
-
某小组为研究电化学原理,设计如图装置。下列叙述错误的是
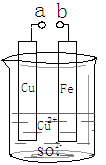
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu
C.a和b分别连接足够电压的直流电源正、负极时,Cu2+向铜电极移动
D.无论a和b是否用导线连接,铁片均溶解,溶液从蓝色逐渐变成浅绿色
难度: 中等查看答案及解析
-
下列有关电池的说法不正确的是
A.手机上用的锂离子电池属于二次电池
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
C.氢氧燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
难度: 简单查看答案及解析
-
一定条件下,可逆反应:X(g) + 3Y(g)
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),反应达到平衡时, X、Y、Z的浓度分别为0.1mol/L、0.3 mol/L、0.08 mol/L,下列判断不正确的是
A.c1∶c2 =1∶3
B.平衡时,Y和Z生成速率之比为3∶2
C.X、Y的转化率不相等
D.c1的取值范围为0< c1< 0.14 mol/L
难度: 中等查看答案及解析
-
在一密闭容器中,反应aA(g)
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
A.平衡向逆反应方向移动了 B.物质A的转化率减小了
C.物质B的质量分数增加了 D.a>b
难度: 中等查看答案及解析
-
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是
A.由Al、Cu、稀H2SO4组成原电池,放电时SO42-向Al电极移动
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O
C.由Fe、Cu、NaCl溶液组成原电池,其负极反应式为:Cu - 2e-= Cu2+
D.由Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出1 mol Ag时,消耗Cu电极32g
难度: 困难查看答案及解析
-
关于下列各装置图的叙述中,不正确的是
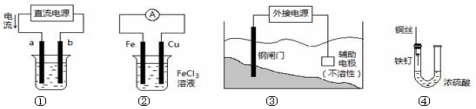
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+
C.装置③中钢闸门应与外接电源的负极相连
D.装置④中的铁钉几乎没被腐蚀
难度: 中等查看答案及解析
-
实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙(其pH变色范围为3.1~4.4)作指示剂,下列操作中可能使测定结果偏低的是
A.酸式滴定管在装酸液前未用标准盐酸润洗2~3次
B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
C.锥形瓶溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
难度: 简单查看答案及解析
-
下列说法中不正确的是
A.体系有序性越高,熵值就越低 B.自发过程将导致体系的熵增大
C.吸热反应不可以自发进行 D.同种物质气态时熵值最大
难度: 简单查看答案及解析