-
下列关于有机化合物的说法正确的是
A.2-甲基丁烷也称异丁烷
B.由乙烯生成乙醇属于加成反应
C.C4H9Cl有3种同分异构体
D.油脂和蛋白质都属于高分子化合物
难度: 简单查看答案及解析
-
化学与生活密切相关,下列有关说法错误的是
A.用灼烧的方法可以区分蚕丝和人造纤维
B.食用油反复加热会产生稠环芳香烃等有害物质
C.加热能杀死流感病毒是因为蛋白质受热变性
D.医用消毒酒精中乙醇的浓度为95%
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数值。下列有关叙述正确的是
A.14 g乙烯和丙烯混合气体中的氢原子数为2NA
B.1 molN2与4 mol H2反应生成的NH3分子数为2NA
C.1 molFe溶于过量硝酸,电子转移数为2NA
D.标准状况下,2.24 LCCl4含有的共价键数为0.4NA
难度: 中等查看答案及解析
-
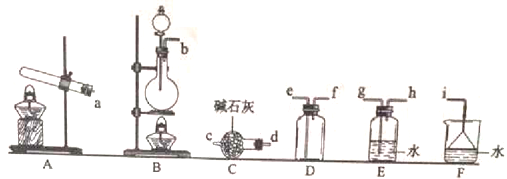
下列实验操作能达到实验目的的是
A.用长颈漏斗分离出乙酸与乙醇反应的产物
B.用向上排空气法收集铜粉与稀硝酸反应产生的NO
C.配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释
D.将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2
难度: 简单查看答案及解析
-
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
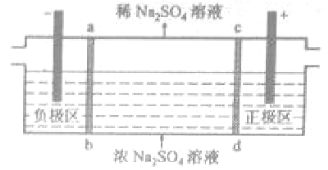
下列叙述正确的是
A.通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2 H2O–4e–=O2+4H+,负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
难度: 困难查看答案及解析
-
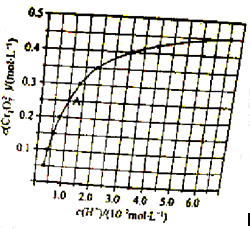
298K时,在20.0mL 0.10mol
氨水中滴入0.10 mol
的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol
氨水的电离度为1.32%,下列有关叙述正确的是
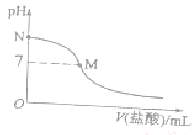
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D.N点处的溶液中pH<12
难度: 困难查看答案及解析
-
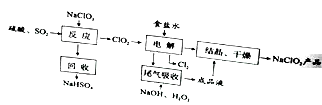
短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L–1 r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是

A.原子半径的大小W<X<Y
B.元素的非金属性Z>X>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
难度: 困难查看答案及解析