-
[化学——选修2:化学与技术]
高锰酸钾( )是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:
)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:
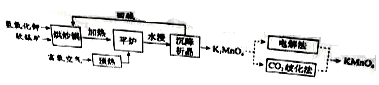
回答下列问题:
(1)原料软锰矿与氢氧化钾按1∶1的比例在“烘炒锅”中混配,混配前应将软锰矿粉碎,其作用是 。
(2)“平炉”中发生的化学方程式为 。
(3)“平炉”中需要加压,其目的是 。
(4)将K2MnO4转化为KMnO4的生产有两种工艺。
①“ 歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成K2MnO4,MnO2和 (写化学式)。
歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成K2MnO4,MnO2和 (写化学式)。
②“电解法”为现代工艺,即电解K2MnO4水溶液,电解槽中阳极发生的电极反应为
,阴极逸出的气体是 。
③“电解法”和“ 歧化法”中,K2MnO4的理论利用率之比为 。
歧化法”中,K2MnO4的理论利用率之比为 。
(5)高锰酸钾纯度的测定:称取1.0800 g样品,溶解后定容于100 mL容量瓶中,摇匀。取浓度为0.2000 mol·L−1的H2C2O4标准溶液20.00 mL,加入稀硫酸酸化,用KMnO4溶液平行滴定三次,平均消耗的体积为24.48 mL,该样品的纯度为
(列出计算式即可,已知2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O)。
-
[化学——选修2:化学与技术]高锰酸钾(KMnO4)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:

回答下列问题:
(1)原料软锰矿与氢氧化钾按1∶1的比例在“烘炒锅”中混配,混配前应将软锰矿粉碎,其作用是 。
(2)“平炉”中发生的化学方程式为 。
(3)“平炉”中需要加压,其目的是 。
(4)将K2MnO4转化为KMnO4的生产有两种工艺。
①“ 歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱酸性,K2MnO4发生歧化反应,反应中生成K2MnO4、MnO2和 (写化学式)。
歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱酸性,K2MnO4发生歧化反应,反应中生成K2MnO4、MnO2和 (写化学式)。
②“电解法”为现代工艺,即电解K2MnO4水溶液,电解槽中阳极发生的电极反应为 ,阴极逸出的气体是 。
③“电解法”和“ 歧化法”中,K2MnO4的理论利用率之比为 。
歧化法”中,K2MnO4的理论利用率之比为 。
(5)高锰酸钾纯度的测定:称取1.0800 g样品,溶解后定容于100 mL容量瓶中,摇匀。取浓度为0.2000 mol·L−1的H2C2O4标准溶液20.00 mL,加入稀硫酸酸化,用KMnO4溶液平行滴定三次,平均消耗的体积为24.48 mL,该样品的纯度为 (列出计算式即可,已知2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O)。
-
高锰酸钾(KMnO4)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:
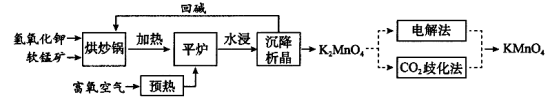
回答下列问题:
(1)“平炉”中发生的化学方程式为 。
(2)“平炉”中需要加压,其目的是 。
(3)将K2MnO4转化为KMnO4的生产有两种工艺。
①“CO2歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成KMnO4,MnO2和 (写化学式)。
②“电解法”为现代工艺,即电解K2MnO4水溶液,电解槽中阳极发生的电极反应为 ,阴极逸出的气体是 。
③CO2的等电子体COS,分子 COS电子式为_____________。
(4)高锰酸钾纯度的测定:称取1.0800 g样品,溶解后定容于100 mL容量瓶中,摇匀。取浓度为0.2000 mol·L−1的H2C2O4标准溶液20.00 mL,加入稀硫酸酸化,用KMnO4溶液滴定,滴定终点现象 ,该反应中,氧化剂与还原剂的物质的量之比 。
-
高锰酸钾(KMnO4)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:
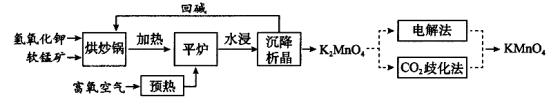
回答下列问题:
(1)“平炉”中发生的化学方程式为 。
(2)“平炉”中需要加压,其目的是 。
(3)将K2MnO4转化为KMnO4的生产有两种工艺。
①“CO2歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成KMnO4,MnO2和 (写化学式)。
②“电解法”为现代工艺,即电解K2MnO4水溶液,电解槽中阳极发生的电极反应为 ,阴极逸出的气体是 。
③CO2的等电子体COS,分子 COS电子式为_______________。
(4)高锰酸钾纯度的测定:称取1.0800 g样品,溶解后定容于100 mL容量瓶中,摇匀。取浓度为0.2000 mol·L−1的H2C2O4标准溶液20.00 mL,加入稀硫酸酸化,用KMnO4溶液滴定,滴定终点现象 ,该反应中,氧化剂与还原剂的物质的量之比为________________。
-
高锰酸钾(KMnO4)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:
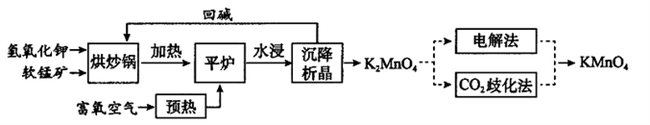
回答下列问题:
(1)原料软锰矿与氢氧化钾按1∶1的比例在“烘炒锅”中混配,混配前应将软锰矿粉碎,其作用是_________________。
(2)“平炉”中发生的化学方程式为_________________,该条件下此反应的△S____0(填大于、小于或等于)。
(3)将K2MnO4转化为KMnO4的生产有两种工艺。
①“CO2歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应生成的含锰物质有KMnO4和MnO2,该反应的化学方程式为__________________。
②“电解法”为现代工艺,即电解K2MnO4水溶液,若用惰性电极,阳离子交换膜电解槽电解时产品纯度高,阴极室中加入电解质溶液溶质的化学式为_______,电解时阳极发生的电极反应为____________,从阳极室的溶液得到产品的实验操作是___________________。与传统工艺比较,现代工艺的优点除产品纯度高外还有_______________。
-
高锰酸钾 是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿
是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿 主要成分为
主要成分为 为原料生产高锰酸钾的工艺路线如下:
为原料生产高锰酸钾的工艺路线如下:
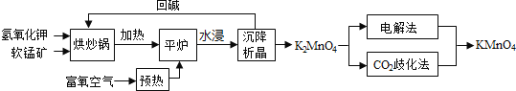
回答下列问题:
 原料软锰矿与氢氧化钾按1:1的比例在“烘炒锅”中混配,混配前应将软锰矿粉碎,其作用是 __________________________________________;
原料软锰矿与氢氧化钾按1:1的比例在“烘炒锅”中混配,混配前应将软锰矿粉碎,其作用是 __________________________________________;
 “平炉”中发生的化学方程式为 _______________________________;
“平炉”中发生的化学方程式为 _______________________________;
 “平炉”中需要加压,其目的是 _______________________________;
“平炉”中需要加压,其目的是 _______________________________;
 将
将 转化为
转化为 的生产有两种工艺:
的生产有两种工艺:
 “
“ 歧化法”是传统工艺,即在
歧化法”是传统工艺,即在 溶液中通入
溶液中通入 气体,使体系呈中性或弱酸性,
气体,使体系呈中性或弱酸性, 发生歧化反应,反应中生成
发生歧化反应,反应中生成 ,
, 和 __________________
和 __________________ 写化学式
写化学式 ;
;
 “电解法”为现代工艺,即电解
“电解法”为现代工艺,即电解 水溶液,电解槽中阳极发生的电极反应为______________________________________________;
水溶液,电解槽中阳极发生的电极反应为______________________________________________;
 “电解法”和“
“电解法”和“ 歧化法”中,
歧化法”中, 的理论利用率之比为______;
的理论利用率之比为______;
 高锰酸钾纯度的测定:称取
高锰酸钾纯度的测定:称取 样品,溶解后定容于100mL容量瓶中,摇匀。取浓度为
样品,溶解后定容于100mL容量瓶中,摇匀。取浓度为 的
的 标准溶液
标准溶液 ,加入稀硫酸酸化,用
,加入稀硫酸酸化,用 溶液平行滴定三次,平均消耗的体积为
溶液平行滴定三次,平均消耗的体积为 ,该样品的纯度为_____________
,该样品的纯度为_____________ 列出计算式即可,已知
列出计算式即可,已知 。
。
-
高锰酸钾是中学化学常用的试剂。主要用于防腐、化工、制药等。实验室模拟工业上用软锰矿制备高锰酸钾的流程如下:
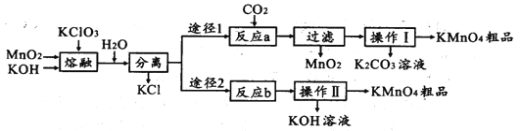
(1)实验室熔融二氧化锰、氧氧化钾、氯酸钾时应选择哪一种仪器________________
a.普通玻璃坩埚 b.石英坩埚 c.陶瓷坩埚 d.铁坩埚
(2)第一步熔融时生成K2MnO4的化学方程式:_________
(3)操作Ⅰ中根据KMnO4和K2CO3两物质在____________ (填性质)上的差异,采用浓缩结晶、趁热过滤得到KMnO4。趁热过滤的原因是_______________
(4)反应b是电解法制备KMnO4,其装置如图所示,a作____________极(填“阳”或“阴”),中间的离子交换膜是_____ (填“阳”或“阴”)离子交换膜。阳极的电极反应式为____________
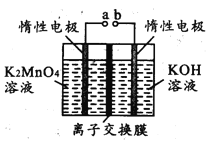
(5)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的________(填标号)。
a.双氧水 b.84消液(NaClO溶液) c.75%酒精
-
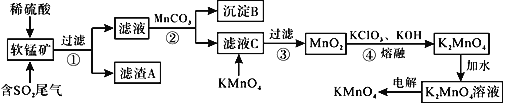
KMnO4是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿(主要成分MnO2,还有Fe2O3、Al2O3、SiO2等)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得KMnO4(反应条件已经省略)。
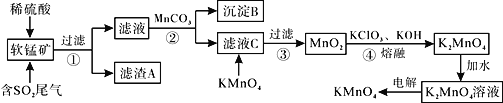
已知:Ksp[Fe(OH)3]=4×10-38,Ksp[Al(OH)3]=1×10-33。回答下列问题:
(1)K2MnO4中Mn的化合价为___________。
(2)滤渣A的成分是_________,析出沉淀B时,首先析出的物质是_________。
(3)步骤2中加入MnCO3的作用为_______________。
(4)滤液C中加入KMnO4时发生反应的离子方程式是_________________。
(5)步骤4中反应的化学方程式是_______________。
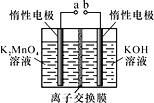
(6)电解制备KMnO4的装置如图所示。b与电源的______极相连,电解液中最好选择_______离子交换膜(填“阳”或“阴”)。电解时,阳极的电极反应式为_________。
-
 是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿
是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿 主要成分
主要成分 ,还有
,还有 、
、 、
、 等
等 作脱硫剂,通过如下简化流程既脱除燃煤尾气中的
作脱硫剂,通过如下简化流程既脱除燃煤尾气中的 ,又制得
,又制得 反应条件已经省略
反应条件已经省略 。
。
已知: ,
, 回答下列问题:
回答下列问题:
 滤渣A的成分是
滤渣A的成分是 写化学式
写化学式  ______。
______。
 析出沉淀B时,首先析出的物质是
析出沉淀B时,首先析出的物质是 写化学式
写化学式  ______。
______。
 步骤2中加入
步骤2中加入 的作用为______。
的作用为______。
 滤液C中加入
滤液C中加入 时发生反应的离子方程式是______。
时发生反应的离子方程式是______。
 完成步骤4中反应的化学方程式______
完成步骤4中反应的化学方程式______ ______
______ ______
______ ______
______
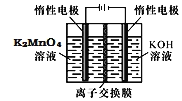
 电解制备
电解制备 的装置如图所示。电解液中最好选择______离子交换膜
的装置如图所示。电解液中最好选择______离子交换膜 填“阳”或“阴”
填“阳”或“阴” 。电解时,阳极的电极反应式为______。
。电解时,阳极的电极反应式为______。
-
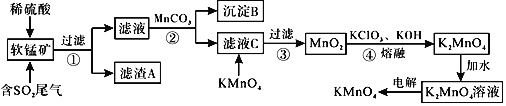
 是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿
是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿 主要成分
主要成分 ,还有
,还有 、
、 、
、 等
等 作脱硫剂,通过如下简化流程既脱除燃煤尾气中的
作脱硫剂,通过如下简化流程既脱除燃煤尾气中的 ,又制得
,又制得 反应条件已经省略
反应条件已经省略 。
。
已知: ,
, 回答下列问题:
回答下列问题:
 滤渣A的成分是
滤渣A的成分是 写化学式
写化学式  ______。
______。
 析出沉淀B时,首先析出的物质是
析出沉淀B时,首先析出的物质是 写化学式
写化学式  ______。
______。
 步骤2中加入
步骤2中加入 的作用为______。
的作用为______。
 滤液C中加入
滤液C中加入 时发生反应的离子方程式是______。
时发生反应的离子方程式是______。
 完成步骤4中反应的化学方程式______
完成步骤4中反应的化学方程式______ ______
______ ______
______ ______
______
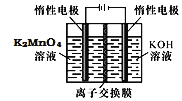
 电解制备
电解制备 的装置如图所示。电解液中最好选择______离子交换膜
的装置如图所示。电解液中最好选择______离子交换膜 填“阳”或“阴”
填“阳”或“阴” 。电解时,阳极的电极反应式为______。
。电解时,阳极的电极反应式为______。
)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:

歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成K2MnO4,MnO2和 (写化学式)。
歧化法”中,K2MnO4的理论利用率之比为 。












