-
简要回答实验室进行下列实验时,是由于什么不当操作引起了题中说明的不良后果:
(1)点燃酒精灯时,灯内有足量酒精,但不着火______;
(2)熄灭酒精灯时,灯内、外酒精一起燃烧______;
(3)H2验纯后的试管再次收集H2时,H2发生器突然发生爆炸______;
(4)用蒸发皿加热食盐水时,食盐水飞溅______.难度: 中等查看答案及解析
-
烟道废气的主要成分是:①CO2②CO③N2④O2.为了测定废气中各组分的体积分数.现提供下列吸收试剂及其性质:
a.KOH溶液:可吸收O2或CO2;
b.Cu2Cl2的氨溶液:可吸收CO,但Cu2Cl2易O2被氧化成CuCl2;
c.KOH溶液:可吸收CO2.
(1)请指明下列被吸收气体应选择的吸收试剂(用吸收试剂的序号填写):CO2______、CO______、O2______.
(2)各气体吸收与测定的先后顺序为______(用气体的序号填写)难度: 中等查看答案及解析
-
已知某工业纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用如图中的装置进行实验.实验前后的测量数据如下
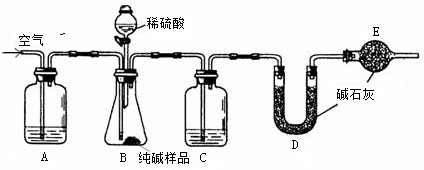
①实验前称量盛有碱石灰的U形管的质量为m1 g.
②实验前称量一定量的工业纯碱n1 g,并将其放入锥形瓶中;
③从分液漏斗中缓缓滴入一定量的稀硫酸,并从导管A处缓缓鼓入一定量的空气,直到不再产生气体时为止;
④实验后称量盛有碱石灰的U型管的质量为m2 g.
根据上述实验操作和测定数据,回答下列问题:(1)C中所盛试剂为______.如果撤去装置C,则会导致实验结果______(填“偏大”、“偏小”或“不变”).
(2)实验进行操作③时,要缓缓鼓入空气,其作用是______,装置A中盛放的液体应选用______,其作用是______.
(3)装置E的作用是______.
(4)根据此实验,写出计算纯碱中Na2CO3的质量分数的表达式:______.难度: 中等查看答案及解析
-
KClO3和MnO2的混合物a g充分加热后,剩余固体物质的质量为b g求原混合物中MnO2的质量分数.
难度: 中等查看答案及解析
-
现有由MgO和MgCl2组成的混合物,测得其中镁元素的质量分数为35.56%,求其中氯元素、氧元素、镁元素的原子个数比.
难度: 中等查看答案及解析
-
将一定量CO和H2的混合气体通过盛有足量灼热CuO的硬质玻璃管后,再通过装有碱石灰(吸收CO2和H2O)的干燥管,假设反应和吸收均完全.现有下列实验数据:盛有CuO的硬质玻璃管的质量在反应前为42.0g,反应后为41.4g;装有碱石灰干燥管的质量在反应前为72.0g,反应后为72.74g.请计算原混合气体中CO和H2的质量各是多少克?
难度: 中等查看答案及解析