-
我国稀土资源丰富,下列关于稀土元素14462Sm与15062Sm的有关说法中,正确的是( )
A.14462Sm与15062Sm互为同位素
B.14462Sm与15062Sm的质量数相同
C.14462Sm与15062Sm是同一种核素
D.14462Sm与15062Sm核外电子数和中子数均为62难度: 中等查看答案及解析
-
在相同条件下,等质量的H3和H2相同的是( )
A.原子数
B.分子数
C.体积
D.物质的量难度: 中等查看答案及解析
-
2008年北京“奥运标准线”中重要组成部分--运通104路是北京首条“无菌”公交路线.公交车上采用了一种纳米材料清洁技术,这种纳米材料的粒子直径是5nm-30nm,若将这种纳米材料分散到液体分散剂中,下列各组混合物和该分散系具有相同数量级的是( )
A.溶液
B.胶体
C.悬浊液
D.乳浊液难度: 中等查看答案及解析
-
下列类型的反应,一定没有发生电子转移的是( )
A.化合反应
B.分解反应
C.置换反应
D.复分解反应难度: 中等查看答案及解析
-
关于氧化还原反应,下列叙述正确的是( )
A.氧化还原反应的本质是化合价发生变化
B.有单质产生的分解反应一定是氧化还原反应
C.氧化剂在同一反应中既可以是反应物,也可以是生成物
D.还原剂在反应中发生还原反应难度: 中等查看答案及解析
-
随着人们生活节奏的加快,方便的小包装食品已被广泛接受.为了延长食品的保质日期,防止富脂食品氧化变质,常在包装袋中放入硫酸亚铁,原因是硫酸亚铁具有( )
A.吸水性
B.氧化性
C.还原性
D.挥发性难度: 中等查看答案及解析
-
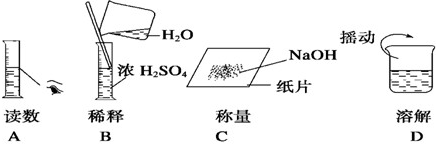
以下实验装置一般不用于分离物质的是( )
A.
B.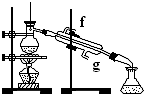
C.
D.难度: 中等查看答案及解析
-
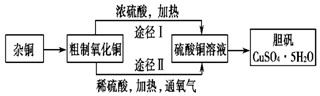
不能实现下列物质间直接转化的元素是( )

A.碳
B.硫
C.钠
D.铜难度: 中等查看答案及解析
-
设NA为阿伏伽德罗常数,下列物质所含的分子数最多的是( )
A.0.8mol二氧化碳
B.含NA个氢原子的氢气
C.3.6g水
D.标准状况下,2.24L氨气难度: 中等查看答案及解析
-
1molO2与1molCO2相比较,下列叙述中正确的是( )
A.在同温同压下,体积相等
B.在同温同压下,密度相等
C.在标准状况下,质量相等
D.所含原子数相等难度: 中等查看答案及解析
-
右图是某燃煤发电厂处理废气的装置示意图.装置内发生的主要反应中不含( )

A.化合反应
B.分解反应
C.置换反应
D.氧化还原反应难度: 中等查看答案及解析
-
相同体积的NaCl溶液(浓度为C1)和Na2SO4溶液(浓度为C2),若其中的Na+ 物质的量浓度相同,则它们的物质的量浓度C1和C2的关系是( )
A.C1=C2
B.C1>2C2
C.C1<2C2
D.C1=2C2难度: 中等查看答案及解析
-
下列出去杂质的方法正确的是( )
A.除去CO2中混有的CO:用澄清的石灰水洗气
B.除去NaHCO3溶液中混有的Na2CO3:通入足量的二氧化碳
C.除去FeCl3溶液中混有的CuCl2:加入过量的铁粉过滤
D.除去BaCO3固体中混有的BaSO4:加入过量的盐酸、过滤、洗涤难度: 中等查看答案及解析
-
设NA为阿伏伽德罗常数,下列叙述正确的是( )
A.24g镁的原子最外层电子数为NA
B.1L0.1mol•L-1乙酸溶液中H+数为0.1NA
C.1mol甲烷分子所含质子数为10NA
D.标准状况下,22.4L乙醇的分子数为NA难度: 中等查看答案及解析
-
从石英砂制取并获得高纯硅的主要化学反应如下:
①SiO2+2CSi(粗)+2CO
②Si(粗)+2Cl2SiCl4
③SiCl4+2H2Si(纯)+4HCl
关于上述反应的分析不正确的是( )
A.①、③是置换反应,②是化合反应
B.高温下,焦炭与氢气的还原性均强于硅
C.任一反应中,每消耗或生成28g硅,均转移4mol电子
D.高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅难度: 中等查看答案及解析
-
300mLAl 2(SO4)3溶液中,含Al3+为1.62g,在该溶液中加入0.1mol/LBa(OH)2溶液300mL,反应后溶液中SO42-的物质的量的浓度为( )(混合体积看成两液体体积之和)
A.0.4mol/L
B.0.3mol/L
C.0.2mol/L
D.0.1mol/L难度: 中等查看答案及解析