①SiO2+2C
②Si(粗)+2Cl2
③SiCl4+2H2
关于上述反应的分析不正确的是( )
A.①、③是置换反应,②是化合反应
B.高温下,焦炭与氢气的还原性均强于硅
C.任一反应中,每消耗或生成28g硅,均转移4mol电子
D.高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅
高三化学选择题中等难度题
高三化学选择题中等难度题
从石英砂制取并获得高纯硅的主要化学反应如下:
①SiO2+2CSi(粗)+2CO↑
②Si(粗)+2Cl2SiCl4
③SiCl4+2H2Si(纯)+4HCl
关于上述反应的分析不正确的是( )
A. ①、③是置换反应,②是化合反应
B. 任一反应中,每消耗或生成28 g硅,均转移4 mol电子
C. 高温下,焦炭与氢气的还原性均强于硅
D. 高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅
高三化学单选题困难题查看答案及解析
高三化学选择题中等难度题查看答案及解析
硅是无机非金属材料的主角,工业上可用多种方法制取硅单质。
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:SiO2(s)+2C(s)=Si(s)+2CO △H = akJ/mol
该反应可分两步进行,其中一步反应为:
SiO2(s)+C(s)=SiO(g)+CO(g)△H=bkJ/mol
则另一步反应的热化学方程式为_________(△H用含a、b的代数式表示)
SiO是反应过程中的中间产物。隔绝空气时,SiO与过量KOH溶液反应的(产物之一是硅酸钾,Si+2KOH+H2O=K2SiO3+2H2↑)的化学反应方程式:______________。
(2)粗硅提纯常用方法之一是先将粗硅与HCl反应制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)Si(s)+3HCl(s),不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图所示:
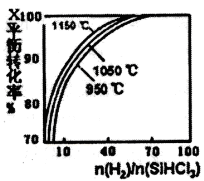
①X是________(填“H2”或“SiHCl3”)
②上述反应的平衡常数K (1150℃)__________K(950℃)(填“>”、“<”或“=”)
③下列叙述不能证明该反应处于平衡状态的是__________。
A.H2的消耗速率等于HCl生成速率的3倍;
B.恒温恒容条件下体系压强不随时间而变化;
C.绝热恒容条件下体系的温度不随时间而变化;
D.某温度下浓度商Qc不随时间而变化;
E.c(SiHCl3):c(H2): c(HCl)=l:l:3
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。
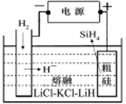
① 用粗硅做原料,熔融盐电解法制取硅烷原理如图所示,电解时阳极的电极反应式:___________。
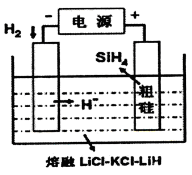
② 硅基太阳能电池需要N、Si两种元素组成的化合物Y 做钝化材料,它可由SiH4与NH3混合反应得到。已知Y 中Si的质量分数为60%,Y的化学式为:______________。
高三化学填空题困难题查看答案及解析
多晶硅是太阳能光伏产业的重要原料。
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
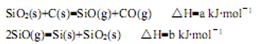
①反应SiO2(s)+2C(s)=Si(s)+2CO(g)的△H=________kJ·mol-1(用含a、b的代数式表示)。
②SiO是反应过程中的中间产物。隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式是________。
(2)粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图;

①X是________(填“H2”、“SiHCl3”)。
②上述反应的平衡常数K(1150℃)________K(950℃)(选填“>”、“<”、“=”)
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。
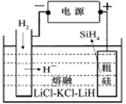
①用粗硅作原料,熔盐电解法制取硅烷原理如图10,电解时阳极的电极反应式为________。
②硅基太阳电池需用N、Si两种元素组成的化合物Y作钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到,已知Y中Si的质量分数为60%,Y的化学式为________。
高三化学计算题极难题查看答案及解析
多晶硅是太阳能光伏产业的重要原料。
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
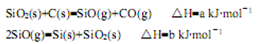
①反应SiO2(s)+2C(s)=Si(s)+2CO(g)的△H=________kJ·mol-1(用含a、b的代数式表示)。
②SiO是反应过程中的中间产物。隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式是________。
(2)粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图;

①X是________(填“H2”、“SiHCl3”)。
②上述反应的平衡常数K(1150℃)________K(950℃)(选填“>”、“<”、“=”)
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。
①用粗硅作原料,熔盐电解法制取硅烷原理如图10,电解时阳极的电极反应式为________。
②硅基太阳电池需用N、Si两种元素组成的化合物Y作钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到,已知Y中Si的质量分数为60%,Y的化学式为________。
高三化学填空题极难题查看答案及解析
半导体工业中,有一句行话:“从沙滩到用户”,即由SiO2制Si。制取过程中不涉及到的化学反应是( )
A. SiO2+2CSi+2CO↑
B. SiO2+2NaOH=Na2SiO3+H2O
C. Si+2Cl2SiCl4
D. SiCl4+2H2Si+4HCl
高三化学单选题中等难度题查看答案及解析
工业上通过反应“SiO2+2CSi+2CO↑”制取单质硅,下列说法正确的是
A. 自然界中硅元素均以SiO2形式存在
B. 高纯度晶体Si可用于制造光导纤维
C. 该反应条件下C的还原性比Si强
D. 标准状况下生成4.48 L CO时转移电子数为0.4×6.02×1023
高三化学选择题困难题查看答案及解析
工业上通过反应“SiO2+2CSi+2CO↑”制取单质硅,下列说法正确的是
A.自然界中硅元素均以SiO2形式存在
B.高纯度晶体Si可用于制造光导纤维
C.该反应条件下C的还原性比Si强
D.生成4.48L CO时转移电子数为0.4×6.03×1023
高三化学选择题中等难度题查看答案及解析
(1)工业上制取纯硅涉及以下三个反应:
①SiO2+2CSi(粗)+2CO↑ ②Si(粗)+2Cl2
SiCl4
③SiCl4+2H2Si(纯)+4HCl
其中属于置换反应的有____________;反应①、②、③的反应物中有C、H2、Cl2、SiO2,按照某种物质分类标准,它们中有一种物质与其他三种物质明显不同,该物质为________,写出分类的依据________ (只需写出一种分类方法)。
(2)碳、铝均能还原铁的氧化物。为确定混合物(含FeO、Fe2O3)的组成,现进行如下实验:
①取一定质量混合物与足量炭粉共热,只收集到CO气体m mol;
②取与①相同质量的混合物与足量铝进行铝热法炼铁,得到单质铁n mol则混合物中FeO的物质的量分数是________(用m、n表示)。
③经测定,消耗1mol碳粉还原固体Fe2O3生成固体铁和CO气体,放出akJ热量,请写出该反应的热化学方程式________。
高三化学填空题中等难度题查看答案及解析
硅及其化合物广泛应用于太阳能的利用、光导纤维及硅橡胶的制备等.
纯净的硅是从自然界中的石英矿石(主要成分为SiO2)中提取.高温下制取纯硅有如下反应(方法Ⅰ):
①SiO2(s)+2C(s)⇌Si(s)+2CO(g)
②Si(s)+2Cl2(g)⇌SiCl4(g)
③SiCl4(g)+2H2(g)→Si(s)+4HCl(g)
完成下列填空:
(1)硅原子核外有______ 种不同能级的电子,最外层p电子有______种自旋方向;SiO2晶体中每个硅原子与______个氧原子直接相连.
(2)单质的还原性:碳______硅(填写“同于”、“强于”或“弱于”).从平衡的视角而言,反应①能进行的原因是______.
(3)反应②生成的化合物分子空间构型为;该分子为______分子(填写“极性”或“非极性”).
(4)某温度下,反应②在容积为V升的密闭容器中进行,达到平衡时Cl2的浓度为a mol/L.然后迅速缩小容器容积到0.5V升,t秒后重新达到平衡,Cl2的浓度为b mol/L.则:a______b(填写“大于”、“等于”或“小于”).
(5)在t秒内,反应②中反应速率v(SiCl4)=______(用含a、b的代数式表示).
(6)工业上还可以通过如下反应制取纯硅(方法Ⅱ):
④Si(粗)+3HCl(g) SiHCl3(l)+H2(g)+Q(Q>0)
⑤SiHCl3(g)+H2(g)Si(纯)+3HCl(g)
提高反应⑤中Si(纯)的产率,可采取的措施有:______、______.
高三化学综合题中等难度题查看答案及解析