-
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A. 四氯化碳的比例模型:
B. 丙烷分子的球棍模型:
C. CO2的电子式:
D. 质量数为37的氯原子: 17 37Cl
难度: 简单查看答案及解析
-
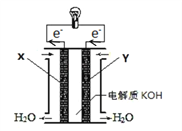
我国科学家报道了如图所示的水溶液锂离子电池体系,下列叙述错误的是( )
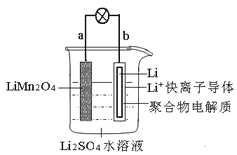
A. 放电时,a极锂的化合价发生变化
B. 电流的方向为a到b
C. a为电池的正极
D. 放电时,溶液中Li+从b向a迁移
难度: 中等查看答案及解析
-
下列说法中,正确的是( )
A. 苯分子中所有原子共面,含3个碳碳双键,能使酸性高锰酸钾溶液褪色
B. 乙烯能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色,反应原理相同
C. 相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同
D. C4H10有4种一氯代物
难度: 简单查看答案及解析
-
下列反应中既是氧化还原反应,能量变化情况又符合下图的是
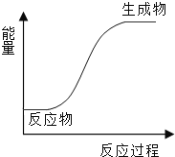
A. 铝片与稀盐酸的反应 B. NH4Cl和Ba(OH)2·8H 2 O的反应
C. 碳和水蒸气反应 D. 甲烷的燃烧反应
难度: 中等查看答案及解析
-
根据元素周期表和元素周期律,判断下列叙述不正确的是 ( )

A. 气态氢化物的稳定性:H2O>NH3
B. 氢元素与其他元素可形成共价化合物或离子化合物
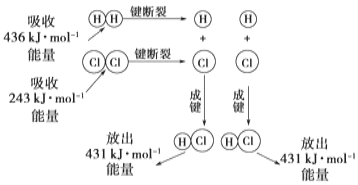
C. 如图所示实验可证明元素的非金属性:Cl>C>Si
D. 人工合成的第118号元素在周期表中位于第七周期0族
难度: 中等查看答案及解析
-
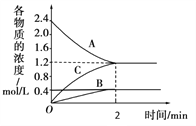
四位同学同时进行反应:A(g)+3B(g)=2C(g)+2D(g)的速率测定实验,分别测得反应速率如下:
①v(A)= 0.15mol/(L·s) ②v(B)= 0.6mol/(L·s)
③v(C)= 0.4mol/(L·s) ④v(D)= 0.45mol/(L·s)
其中,反应进行得最快的是( )
A. ④ B. ③ C. ② D. ①
难度: 简单查看答案及解析
-
下列叙述I和II均正确并且有因果关系的是 ( )
选项
陈述I
陈述II
A
SiO2硬度大
SiO2用于制造光导纤维
B
Fe3+具有氧化性
用KSCN溶液可以鉴别Fe3+
C
相同条件下,溶解度:CaCO3<Ca(HCO3)2
相同条件下,溶解度:Na2CO3<NaHCO3
D
Na2O2吸收CO2产生O2
用作呼吸面具供氧剂
A. A B. B C. C D. D
难度: 中等查看答案及解析
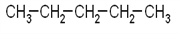 ②
②  ⑤
⑤ 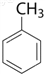 ⑥
⑥ 