-
下列各组物质混合后,不能生成NaOH的是
A. Na和H2O B. Na2O2和H2O
C. Ca(OH)2溶液和Na2CO3溶液 D. Ca(OH)2溶液和NaCl溶液
难度: 中等查看答案及解析
-
氨气(NH3)是一种十分重要的化学物质,下列反应中,氨气做氧化剂的是
A. 8NH3+3Cl2 = 6NH4Cl+N2 B. 2NH3+2Na = 2NaNH2+H2↑
C. HCl + NH3 = NH4Cl D. 2NH3+3CuO = N2↑+3Cu+3H2O
难度: 简单查看答案及解析
-
把铁片放入下列溶液中,铁片溶解,溶液质量增加,但没有气体放出的是
A. 稀硫酸 B. CuSO4溶液 C. Fe2(SO4)3溶液 D. AgNO3溶液
难度: 中等查看答案及解析
-
下列气体中,对人体无毒害作用的是
A. NH3 B. NO2 C. N2 D. Cl2
难度: 简单查看答案及解析
-
人们庆祝节日时燃放的焰火与金属的焰色反应直接相关。下列说法中正确的是
A. 焰色反应实验时,应将铂丝用硫酸洗净并灼烧到无特殊焰色
B. 焰色反应实验时一定有氧化还原反应发生
C. 焰色反应实验时可用洁净的铁丝代替铂丝
D. 某样品的焰色反应呈黄色,则其中一定含钠元素而不含钾元素
难度: 中等查看答案及解析
-
下列成分组成的物质一定不是合金的是
A. Fe、C B. C、Si C. Cu、Zn D. Al、Cu
难度: 中等查看答案及解析
-
下列贮存试剂的方法错误的是
A. FeCl3溶液加入少量铁粉保存 B. 常温下,浓硝酸保存在铁器皿中
C. 烧碱溶液保存在带橡胶塞的试剂瓶中 D. 小块钠保存在煤油中
难度: 中等查看答案及解析
-
下列除杂试剂和操作方法的选择正确的是
物质(括号内为杂质)
除杂试剂
操作
A
CO2(SO2)
Na2CO3溶液
洗气
B
SiO2(CaO)
稀硫酸
充分反应后过滤
C
NaHCO3(Na2CO3)
无
充分加热
D
MgO(Al2O3)
NaOH溶液
充分反应后过滤
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
在实验室里,要想使AlCl3中的A1全部沉淀出来,应选用下列试剂中的
A. 氨水 B. 氢氧化钠溶液 C. 硫酸 D. 石灰水
难度: 中等查看答案及解析
-
关于硅及其化合物的叙述中,错误的是
A. 水玻璃可做粘合剂及耐火材料 B. 硅可做半导体材料
C. 普通玻璃以黏士和石灰石为原料 D. 二氧化硅是制作光导纤维的原料
难度: 中等查看答案及解析
-
下列有关实验安全问题的叙述中确的是
A. 实验室制取氯气时,多余的氯气应通入水中
B. 蒸发食盐溶液时,发生液滴飞溅现象,立即加水冷却
C. 酒精不小心酒在实验泉上,并燃烧起来,应立即用水扑灭
D. 在盛放浓硫酸的试剂瓶的标签上应印有右图所示的警示标识
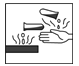
难度: 中等查看答案及解析
-
丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,其密度小于lg/ml,沸点约55℃,分离水和丙酮最合理的方法是
A. 蒸发 B. 分液 C. 蒸馏 D. 过滤
难度: 中等查看答案及解析
-
若NA表示阿伏加德罗常数的值,则下列叙述中正确的是
A. 1molFe与足量稀硝酸完全反应,转移电子数目为2NA
B. 标准状况下,11.2LH2O中含有的原子数为1.5NA
C. 0.5mol/LFe2(SO4)3溶液中,SO42-的数目为1.5NA
D. 1molN2所含的原子个数为2NA
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是
A. 铜片加入稀硫酸中:Cu+2H+=Cu2++H2↑
B. 铁与稀硝酸反应:Fe+2H+=Fe2++H2↑
C. 二氧化碳通入氢氧化钠溶液中:CO2+2OH-=CO32-+H2O
D. 稀硫酸与氢氧化钡溶液反应:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓
难度: 中等查看答案及解析
-
下列离子在容液中能大量共存的是
A. K+、CO32-、Ba2+、Cl- B. NH4+、NO3-、Na+、HCO3-
C. Fe2+、Cl-、H+、NO3- D. H+、SiO32-、K+、NO3-
难度: 简单查看答案及解析
-
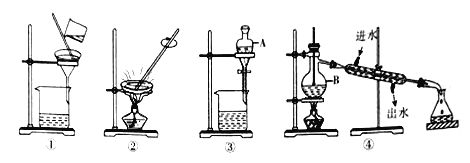
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作下列图示对应的操作规范的是( )
A. 称量
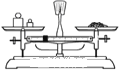 B. 溶解
B. 溶解C. 转移
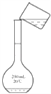 D. 定容
D. 定容
难度: 简单查看答案及解析
-
下对有关电解质的说法正确的是
A. 熔融的A12O3能导电,所以它属于电解质
B. NH3的水溶液可以导电,所以它属于电解质
C. BaSO4为难溶物,所以它不属于电解质
D. 纯硫酸不导电,所以它不属于电解质
难度: 中等查看答案及解析
-
向未知水溶液中加入AgNO3溶液有白色沉淀生成,再加入稀硝酸后,沉淀部分溶解,且有无色无味的气体生成,将此气体通入澄清石灰水石灰水变浑浊,由此判断未知水溶液中可能含有
A. CO32-、 NO3- B. Cl-、NO3- C. Cl-、CO32- D. Cl-、OH-
难度: 中等查看答案及解析
-
下列关于浓硫酸和浓硝酸的叙述中错误的是
A. 加热时两者都能与铜发生反应
B. 两者都具有较强的氧化性
C. 浓硫酸能使蔗糖等有机物炭化,浓硝酸不能
D. 浓硝酸与浓盐酸按质量比为1:3混合可得王水
难度: 中等查看答案及解析
-
只用一种试剂可将NH4Cl、(NH4)2SO4、NaCl、Na2SO4 四种溶液区分开,这种试剂是
A. Ba(OH)2溶液 B. AgNO3溶液 C. BaCl2溶液 D. NaOH 溶液
难度: 中等查看答案及解析