-
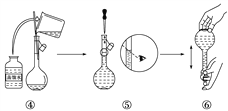
对于危险化学品在包装标签上印有警示性标志。在运输乙醇的包装标签上应选用的标志是

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
具备基本的化学实验技能使进行科学探究的基础和保证。下列有关实验操作正确的是
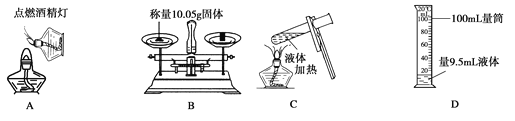
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
进行化学实验时必须注意安全,下列说法不正确的是
①不慎将酸溅到眼中,应立即用大量水冲洗,边洗边眨眼睛 ②不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 ③不慎将浓盐酸洒在桌面上,应立即用浓氢氧化钠溶液冲洗 ④配制稀硫酸时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 ⑤酒精灯着火时可用水扑灭
A. ①②③ B. ②③④ C. ③④⑤ D. 全部
难度: 中等查看答案及解析
-
下列叙述正确的是
A. 1 mol H2O的质量为18 g/mol
B. 3.01×1023个SO2分子的质量为32 g
C. 4 g NaOH溶于1L水中,所得溶液的物质的量浓度为0.1 mol/L
D. 标准状况下,1 mol任何物质体积均为22.4 L
难度: 简单查看答案及解析
-
下列确定某溶液中一定有SO
的方法中,正确的是
A. 先加BaCl2溶液有白色沉淀,再加稀盐酸沉淀不消失
B. 先加BaCl2溶液有白色沉淀,再加稀硝酸沉淀不消失
C. 先加Ba(NO3)2溶液有白色沉淀,再加稀硫酸沉淀不消失
D. 先加稀盐酸无明显现象,再加BaCl2溶液有白色沉淀
难度: 简单查看答案及解析
-
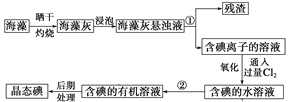
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A. 分液、蒸馏、萃取 B. 萃取、蒸发、分液
C. 分液、萃取、蒸馏 D. 蒸馏、萃取、分液
难度: 中等查看答案及解析
-
为了除去粗盐中的Ca2+、Mg2+、SO
和泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液,正确的操作顺序是
A. ①④②⑤③ B. ④①②⑤③
C. ②⑤④①③ D. ④⑤②①③
难度: 中等查看答案及解析
-
下列各组物质中,可按溶解、过滤、蒸发的操作顺序分离的是
A. 氧化铜和炭粉 B. 硝酸钾和氯化钠
C. 水和酒精 D. 碳酸钠和硫酸钡
难度: 中等查看答案及解析
-
下列实验操作中正确的是
A. 蒸发操作时,应使混合物中的水分完全蒸干后才能停止加热
B. 过滤操作时,玻璃棒紧靠三层滤纸处
C. 分液操作时,分液漏斗中下层液体从下口放出后,再将上层液体从下口放出到另一个烧杯
D. 萃取操作时,萃取剂的密度必须比水大
难度: 简单查看答案及解析
-
下列两种气体的分子数一定相等的是
A. 质量相等的N2O和CO2 B. 体积相等的CO和C2H4
C. 等温、等体积的O2和N2 D. 等压、等体积的N2和CO2
难度: 中等查看答案及解析
-
在体积为V L的密闭容器中,通入气体CO a mol和O2 b mol,点燃充分反应后,容器中碳原子数和氧原子数之比为
A.
B.
C.
D. a/(2a+b)
难度: 中等查看答案及解析
-
下列说法正确的是
A. 在常温、常压下,11.2 L N2含有的分子数为0.5 NA
B. 标准状况下,22.4 L H2和O2的混合物所含分子数为NA
C. 标准状况下,18 g H2O的体积是22.4 L
D. 1 mol SO2的体积是22.4 L
难度: 简单查看答案及解析
-
下列溶液中溶质的物质的量浓度为1 mol/L的是
A. 将40 g NaOH溶解在1 L水中
B. 将22.4 L HCl气体溶于水配成1 L溶液
C. 将1 L 10 mol/L浓盐酸加入9 L水中
D. 将10 g NaOH溶解在水中配成250 mL溶液
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,以任意比例混合的氧气和二氧化碳混合物22.4 L,所含的分子数为NA
B. 标准状况下,1 L汽油(分子式为C8H18)完全燃烧后,所生成气体产物的分子数为8NA/22.4
C. 标准状况下,1 L四氯化碳所含分子数为NA/22.4
D. 标准状况下,以任意比混合的氢气和一氧化碳气体共8.96 L,所含分子数为0.8 NA
难度: 简单查看答案及解析
-
下列有关物质的分类正确的是
A. 混合物:空气、矿泉水、水银 B. 酸性氧化物:CO2 、SO2、 CO
C. 盐:醋酸钠、氯化铵、纯碱 D. 纯净物:CH3COOH、H2O、盐酸
难度: 简单查看答案及解析
-
用10 mL的0.1 mol·L-1 BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌
和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是
A. 3∶2∶2 B. 1∶3∶3 C. 1∶2∶3 D. 3∶1∶1
难度: 中等查看答案及解析
-
下列描述正确的是
A. 胶体粒子大小介于1纳米至100纳米之间,所以纳米材料全部属于胶体
B. 两种物质的物质的量相同,则它们在标况下的体积也相同
C. 可使用丁达尔效应来区分FeCl3溶液和Fe(OH)3胶体
D. 1 mol 任何物质均含有约6.02×1023个原子
难度: 简单查看答案及解析