-
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O 下列说法不正确的是( )
A.KClO3在反应中得到电子
B.ClO2是还原产物
C.H2C2O4在反应中被氧化
D.1molKClO3参加反应有2mol电子转移难度: 中等查看答案及解析
-
下列关于胶体的叙述不正确的是( )
A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9~10-7m之间
B.光线透过胶体时,胶体中可发生丁达尔效应
C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
D.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的难度: 中等查看答案及解析
-
已知短周期元素的离子.aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A.原子半径A>B>D>C
B.a-c=1
C.离子半径C>D>B>A
D.单质的还原性A>B>D>C难度: 中等查看答案及解析
-
经分析,某物质只含有一种元素,则该物质( )
A.一定是纯净物
B.可能是化合物
C.一定是混合物
D.可能是纯净物,也可能是混合物难度: 中等查看答案及解析
-
下列电离方程式的书写正确的是( )
A.CuCl2=Cu+Cl2↑
B.Na2CO3=2Na++CO32-
C.KClO3═K++Cl-+3O2-
D.Ba(OH)2=Ba2++(OH)-2难度: 中等查看答案及解析
-
0.5L 1mol/L FeCl3溶液与0.2L 1mol/L KCl溶液中的Cl-的物质的量浓度之比( )
A.5:2
B.3:1
C.15:2
D.1:3难度: 中等查看答案及解析
-
分离下列各组固体混合物时,可按溶解、过滤、蒸发的操作顺序进行的是( )
A.氯化钠和硝酸钾
B.铁粉和锌粉
C.氯化钾和二氧化锰
D.碳酸铵和氯化铵难度: 中等查看答案及解析
-
不另用任何试剂就能将下列五种溶液:①CuCl2、②Na2SO4、③KCl、④K2CO3、⑤BaCl2鉴别出来,其正确的鉴别顺序是( )
A.①②④③⑤
B.④⑤③②①
C.①④⑤②③
D.①②④⑤③难度: 中等查看答案及解析
-
下列叙述中正确的是( )
A.摩尔是表示物质所含微粒数量以及物质质量的具有双重意义的单位
B.摩尔是国际单位制中7个基本物理量
C.含有6.02×1023个氧原子的H3PO4的物质的量是0.25mol
D.2H既可以表示2个氢原子又可以表示2mol氢原子难度: 中等查看答案及解析
-
下列反应中既是化合反应又是氧化还原反应的是( )
A.CaO+H2O=Ca(OH)2
B.Ca+Cl2CaCl2
C.Fe+CuSO4=FeSO4+Cu
D.H2SO4+BaCl2=BaSO4↓+2HCl难度: 中等查看答案及解析
-
下列物质属于电解质的是( )
A.铜
B.AgNO3
C.蔗糖
D.盐酸难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数,下列说法中正确的是( )
A.1molNa2SO4溶于水中,所得溶液中Na+个数为NA
B.18g水含有电子数为8NA
C.标准状况下,22.4L氢气含有氢原子个数约为2NA
D.11.2L氢气一定含有NA个氢原子难度: 中等查看答案及解析
-
有下列物质:
①0.5mol NH3 ②标准状况下22.4L He ③4℃时9ml H2O ④0.2mol H3PO4
按所含的原子数由多到少的顺序排列正确的是( )
A.①④③②
B.④③②①
C.②③④①
D.①②③④难度: 中等查看答案及解析
-
标准状况下,相同物质的量的SO2和SO3,下列有关说法正确的是( )
A.具有相同数目的原子数
B.具有相同的氧原子数
C.具有相同的质量
D.质量比为4:5难度: 中等查看答案及解析
-
某金属氯化物MCl2 40.5g,含有0.6mol Cl-,则金属M的摩尔质量为( )
A.135
B.135g•mol-1
C.64
D.64g•mol-1难度: 中等查看答案及解析
-
2mol Cl2与足量的元素A单质完全反应生成1mol AClX,则x值为( )
A.1
B.2
C.3
D.4难度: 中等查看答案及解析
-
相同物质的量的各种固体或液体的体积并不相同,其主要原因是( )
A.粒子大小不同
B.粒子质量不同
C.粒子间距离不同
D.粒子间作用力不同难度: 中等查看答案及解析
-
实验室用浓硫酸配制1mol•L-1的稀硫酸溶液250mL,下列不需要的仪器是( )
A.烧杯
B.漏斗
C.玻璃棒
D.容量瓶难度: 中等查看答案及解析
-
要将溴水中的溴提取出来,需要用到的一组仪器是( )
A.普通漏斗、玻璃棒、烧杯
B.分液漏斗、玻璃棒、烧杯
C.大试管、试管夹、容量瓶
D.分液漏斗、烧杯、铁架台难度: 中等查看答案及解析
-
检验NH3的方法或现象的描述中,正确的是( )
A.干燥的红色石蕊试纸变红
B.使湿润的红色石蕊试纸变蓝
C.闻溶液的气味
D.尝溶液的味道难度: 中等查看答案及解析
-
“1mol/L的Na2SO4溶液”的含义是( )
A.1L水中有1molNa2SO4
B.1L溶液中含有142gNa2SO4
C.SO42-的物质的量浓度为2mol/L
D.1LNa2SO4溶液中含有Na+1mol难度: 中等查看答案及解析
-
用括号中注明的方法分离下列各组混合物,其中不正确的是( )
A.氮气和氧气(液化蒸馏)
B.食盐中的沙砾(溶解过滤)
C.氢氧化铁胶体和水(过滤)
D.花生油和水(分液)难度: 中等查看答案及解析
-
下述实验现象能确定试样中一定有Cl-的是( )
A.滴加AgNO3溶液有白色沉淀
B.滴加硝酸酸化的Ba(NO3)2有白色沉淀
C.滴加硝酸酸化的AgNO3溶液有白色沉淀
D.滴加硫酸酸化的AgNO3溶液有白色沉淀难度: 中等查看答案及解析
-
检验试样中有无SO42-的操作及结论正确的是( )
A.先加HCl无明显现象,再加BaCl2有白色沉淀,一定有SO42-
B.加HCl酸化的BaCl2有白色沉淀,一定有SO42-
C.滴加硝酸酸化的Ba(NO3)溶液有白色沉淀,一定有SO42-
D.滴加BaCl2有白色沉淀,一定有SO42-难度: 中等查看答案及解析
-
关于配制NaCl溶液的叙述不正确的是( )
A.托盘天平称取58.5g食盐,加1升水配制成溶液,NaCl溶液浓度为1mol•L-1
B.转移时,要用玻璃棒引流
C.溶解食盐的烧杯要洗涤2~3次并将洗涤液转移到容量瓶中
D.搅拌可加速溶解难度: 中等查看答案及解析
-
配制100mL1.0mol•L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是( )
A.容量瓶使用前有少量蒸馏水
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.在转移过程中有溶液撒在外面
D.定容时俯视确定凹液面与刻度线相切难度: 中等查看答案及解析
-
元素R的质量数为A,Rn-的核外电子数为x,则WgRn-所含中子的物质的量为( )
A.(A-x+n)mol
B.(A-x-n)mol
C.mol
D.mol
难度: 中等查看答案及解析
-
如图是一种试验某气体化学性质的实验装置,图中B为开关.若先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )
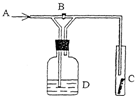
A.浓H2SO4
B.饱和NaCl溶液
C.浓NaOH溶液
D.浓NaBr溶液难度: 中等查看答案及解析