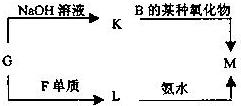
-
已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列判断中正确的是( )
A.元素非金属性按X、Y、Z的顺序减弱
B.阴离子的还原性按X、Y、Z的顺序减弱
C.气态氢化物的稳定性按X、Y、Z的顺序增强
D.单质的氧化性按X、Y、Z的顺序增强难度: 中等查看答案及解析
-
元素A的阳离子与元素B的阴离子具有相同的电子层结构.以下关于A、B元素性质的比较中,正确的是( )
①原子半径:A<B ②原子序数:A>B ③原子最外层电子数:B>A
④元素所在的周期数:A>B ⑤A的最高正价与B的最低负价的绝对值相等.
A.、①②
B.、②③④
C.、④⑤
D.、②⑤难度: 中等查看答案及解析
-
(东城一模)应用元素周期律分析下列推断,其中正确的组合是( )
①碱金属单质的熔点随原子序数的增大而降低
②砹(At)是第VIIA族,其氢化物的稳定性大于HCl
③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱.
A.①③④
B.①③⑥
C.③④⑤
D.②④⑥难度: 中等查看答案及解析
-
元素性质呈周期性变化的决定因素是( )
A.元素原子半径呈周期性变化
B.元素的相对原子质量依次递增
C.元素原子的核外电子排布呈周期性变化
D.元素的化合价呈周期性的变化难度: 中等查看答案及解析
-
某阳离子Mn+ 的核外共有x个电子,核内有a个中子,则M的质量数为( )
A.a+x-n
B.a+x+n
C.a-x-n
D.a-x+n难度: 中等查看答案及解析
-
含硒(Se)的保健品已开始进入市场.已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中,正确的是( )
A.非金属性比硫强
B.氢化物比HBr稳定
C.原子序数为34
D.最高价氧化物的水化物显碱性难度: 中等查看答案及解析
-
2005年,我国考古工作取得了七项重大成果,13C、15N应用于考古研究名列第七.下列对13C、15N的有关叙述中正确的是( )
A.13C与15N互为同位素
B.13C、15N原子中质子数不等,中子数相等
C.13C与15N的质量比约为13:15
D.13C与12C、14N与15N的化学性质不同,因而才有用于考古研究的特殊用途难度: 中等查看答案及解析
-
下列叙述中错误的是( )
A.原子半径:Cl>S>O
B.还原性:Na>Mg>Al
C.稳定性:HF>CH4>SiH4
D.酸性:HClO4>H2SO4>H3PO4难度: 中等查看答案及解析
-
与氢氧根具有相同的质子数和电子数的微粒是( )
A.CH4
B.NH4+
C.NH2-
D.Cl-难度: 中等查看答案及解析
-
下列有关原子结构和元素周期律的表述正确的是( )
①ⅦA族元素是同周期中非金属性最强的元素
②原子序数为15的元素的最高化合价为+3
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素的单质常温与水缓慢反应.
A.①②
B.①④
C.②③
D.③④难度: 中等查看答案及解析
-
AB是A离子和B离子构成的化合物,其中A离子和B离子的电子层结构相同,A、B原子核外最外层电子数A比B少4个,而次外层电子数则A是比B多6个,则该化合物可以是( )
A.MgO
B.CaO
C.KF
D.MgS难度: 中等查看答案及解析
-
下列粒子的结构示意图正确的是( )
A.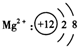
B.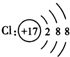
C.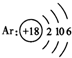
D.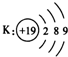
难度: 中等查看答案及解析
-
根据下列原子结构示意图的共同特征,可把
 三种微粒归为一类.下面的微粒可以归入此类的是( )
三种微粒归为一类.下面的微粒可以归入此类的是( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
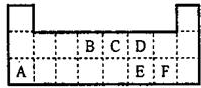
右图是元素周期表的一部分,下列有关A、B、C、D四种元素的叙述正确的是( )
A.原子半径由大到小排列顺序A>B>C>D
B.生成的气态氢化物稳定性为A>B>C>D
C.A元素形成化合物种类最多
D.A、B、C、D的单质在常温下均不导电难度: 中等查看答案及解析
-
X,Y,Z,W四种短周期元素,若①X的阳离子与Y阴离子具有相同的电子层结构.②W的阳离子的氧化性强于同主族带等电荷数的X的阳离子的氧化性.③Z的阴离子半径大于同主族带等电荷的Y的离子半径.则这四种元素的原子序由大到小的顺序为( )
A.W>Y>X>Z
B.Z>Y>W>X
C.X>Y>Z>W
D.Z>X>Y>W难度: 中等查看答案及解析
-
甲和乙都属于非金属元素,下列叙述中,不能说明甲原子得电子能力比乙强的是( )
A.甲比乙容易与氢气化合
B.甲单质能与乙的阴离子在水溶液中发生氧化还原反应
C.最高价氧化物对应的水化物的酸性甲强于乙
D.与某金属反应时,甲原子得电子数目比乙原子多难度: 中等查看答案及解析
-
根据表1信息,
表1 部分短周期元素的原子半径及主要化合价
判断以下叙述正确的是( )元素代号 L M Q R T 原子半径/nm 0.160 0.143 0.092 0.104 0.066 主要化合价 +2 +3 +2 +6、-2 -2
A.氢化物的沸点为H2T<H2R
B.与稀盐酸反应单质L比单质Q慢
C.L2+与R2-的核外电子数相等
D.M与T形成的化合物具有两性难度: 中等查看答案及解析
-
某元素的最外层有 2 个电子,则 该元素( )
A.一定是金属元素
B.最高化合价一定为+2价
C.一定是ⅡA族元素
D.无法确定属于哪类元素难度: 中等查看答案及解析