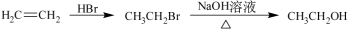-
我国新修订的《环境保护法》已于2015年1月1日起施行。下列做法不应该提倡的是
A.用CO2合成聚碳酸酯等可降解塑料,减少白色污染
B.推广燃煤发电,停建核电站,避免核泄漏事故的危害
C.加强生活污水的脱氮除磷处理,遏制水体的富营养化
D.实施化石燃料脱硫脱硝技术,减少大气污染物的排放
难度: 简单查看答案及解析
-
下列有关氧元素及其化合物的表示正确的是
A.质子数为8、中子数为10的氧原子:
B.氧原子的结构示意图:
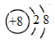
C.水分子的电子式:
D.乙酸甲酯的结构简式:HCOOC2H5
难度: 简单查看答案及解析
-
下列说法正确的是
A.在化学反应中,原子重新组合时伴随着能量的变化
B.淀粉和纤维素的化学式均为(C6H10O5)n,故互为同分异构体
C.通过化学变化可以“点石成金”,即可将黏土转化成金单质
D.等质量的铝粉按a、b两种途径完全转化,途径a比途径b消耗更多的NaOH
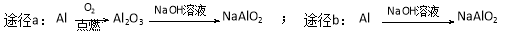
难度: 中等查看答案及解析
-
Mg和SiO2在高温下反应生成MgO和Mg2Si。下列说法正确的是
A.微粒的半径:Si > Mg B.氧元素不存在同素异形体
C.Mg的还原性强于Si D.该反应是置换反应,镁元素被氧化
难度: 中等查看答案及解析
-
原子序数依次增大的短周期主族元素X、Y、Z、W,X是最外层只有一个电子的非金属元素,Y是地壳中含量最高的元素,W的原子序数是Y的2倍,X、Y、Z、W最外层电子数之和为15。下列说法正确的是
A.X和Y只能形成一种化合物 B.简单离子半径:W2->Y2->Z2+
C.简单气态氢化物的热稳定性:W>Y D.WY2、ZY中化学键类型相同
难度: 中等查看答案及解析
-
常温下,下列各组离子一定能在指定溶液中大量共存的是
A.使甲基橙呈红色的溶液:Na+、NH4+、AlO2-、CO32-
B.8% H2O2溶液:H+、Fe2+、SO42-、Cl-
C.含有Fe3+的溶液:Na+、Al3+、Cl-、SCN-
D.Kw/c(H+)=0.1 mol·L-1的溶液:Na+、K+、CO32-、ClO-
难度: 中等查看答案及解析
-
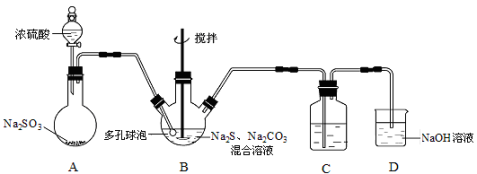
下列有关实验原理或实验操作正确的是
A.将氯化铁固体溶于稀盐酸配制FeCl3溶液
B.称取4.0gNaOH,放入100mL容量瓶中,加水稀释,配制1.0mol·L-1的NaOH溶液
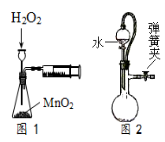
C.利用图1装置定量测定H2O2的分解速率
D.如图2所示,关闭弹簧夹检查装置的气密性
难度: 中等查看答案及解析
-
在给定条件下,下列选项中所示的物质间转化均能一步实现的是
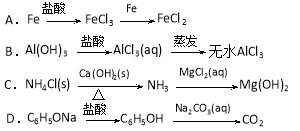
难度: 中等查看答案及解析
-
下列指定反应的离子方程式正确的是
A.氨水吸收少量的CO2气体:NH3·H2O+ CO2 = NH4++HCO3-
B.Na2SO3溶液中SO32-的水解:SO32-+ 2H2O=H2SO3 + 2OH-
C.KClO3溶液与浓盐酸反应: ClO3-+5Cl-+6H+=3Cl2↑+3H2O
D.(NH4)2Fe(SO4)2溶液与过量NaOH反应:Fe2++2OH-=Fe(OH)2↓
难度: 困难查看答案及解析
-
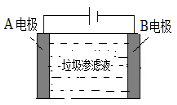
一种石墨烯锂硫电池(2Li+S8=Li2S8)工作原理示意如图。下列有关该电池说法正确的是
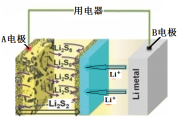
A.B电极发生还原反应
B.A电极上发生的一个电极反应为:2Li++S8+2e-=Li2S8
C.每生成1mol Li2S8转移0.25mol电子
D.电子从B电极经过外电路流向A电极,再经过电解质流回B电极
难度: 困难查看答案及解析
-
下列有关说法正确的是
A.普通锌锰干电池中的MnO2在工作时起催化作用
B.若1mol Na2O2与足量水反应产生O2,理论上转移的电子数约为2×6.02×1023
C.室温下,体积、pH均相同的HA和HB两种酸分别与足量的锌反应,HA放出氢气多,说明酸性:HB>HA
D.恒温恒压密闭容器中进行的反应N2(g)+3H2(g)
2NH3(g) △H=-a kJ·mol-1,平衡时向容器中再充入一定量NH3,重新达平衡时a值不变
难度: 中等查看答案及解析
-
分枝酸在微生物、植物的芳香族氨基酸的生物合成系统中作为中间体,其结构简式如图。下列关于分枝酸的叙述不正确的是
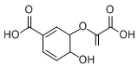
A.分枝酸的分子式为C10H10O6
B.1mol分枝酸最多消耗3molNaOH
C.分枝酸分子中含2个手性碳原子
D.一定条件下,分枝酸可发生取代、加成、氧化和聚合反应
难度: 中等查看答案及解析
-
下列设计的实验方案能达到实验目的的是
A.工业上制取漂白粉:向澄清石灰水中通入足量的Cl2
B.验证醋酸是弱电解质:常温下测定0.1 mol·L-1醋酸或醋酸钠溶液的pH
C.探究FeCl3和KI溶液反应限度:向5mL0.1 mol·L-1KI溶液中加入0.1 mol·L-1FeCl3溶液1mL,振荡,加苯萃取后,向水层中加入5滴KSCN溶液,观察实验现象
D.检验蔗糖水解生成的葡萄糖:蔗糖溶液在稀硫酸存在下水浴加热一段时间后,再与银氨溶液混合加热,观察实验现象
难度: 中等查看答案及解析
-
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.在0.1mol·L-1 NH4Cl溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.在0.1mol·L-1 CH3COOH中: c(CH3COOH)>c(H+)>c(CH3COO-)>c(OH-)
C.0.2mol·L-1NaHCO3溶液与0.1mol·L-1KOH溶液等体积混合:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3)
D.0.2mol·L-1氨水与0.1mol·L-1HCl溶液等体积混合:c(Cl-)+c(H+)=c(NH3·H2O)+c(OH-)
难度: 困难查看答案及解析
-
臭氧的脱硝反应为:2NO2(g)+O3(g)
N2O5(g)+O2(g),一定条件下,向2.0 L恒容密闭容器中充入2.0 mol NO2和1.0 mol O3,一段时间后达到平衡。下图曲线a表示该反应在温度T下O3的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时O3的浓度随时间的变化。下列叙述正确的是

A.反应2NO2(g)+O3(g)
N2O5(g)+O2(g) △S<0
B.曲线b对应的条件改变可能是加入了催化剂,平衡常数Ka=Kb
C.曲线b对应的条件改变可能是密闭容器的体积变为4.0 L
D.若c1=0.3mol·L-1,从反应开始到平衡时该反应的速率v(NO2)=0.005 mol·L-1·s-1
难度: 困难查看答案及解析


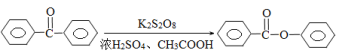

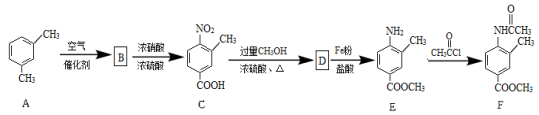
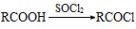 。请写出以
。请写出以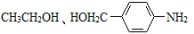 为原料,制备化合物
为原料,制备化合物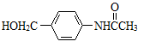 的合成路线流程图(无机试剂可任选)。
的合成路线流程图(无机试剂可任选)。