-
下列物质的类别与所含官能团都正确的是
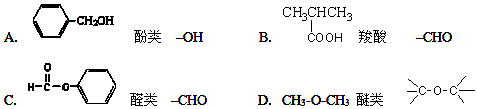
难度: 简单查看答案及解析
-
物质的量浓度相同的三种正盐NaX、NaY、NaZ的水溶液,其pH分别为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
A、HX>HZ>HY B、HZ>HY>HZ C、HX>HY>HZ D、HY>HZ>HX
难度: 简单查看答案及解析
-
物质的量浓度都是0.1mol/L的CH3COOH和CH3COONa混合溶液,已知其中c(CH3COO-)>c(Na+),对该溶液的下列判断正确的是
A.c(H+)<c(OH-)
B.c(CH3COOH)+c(CH3COO-)=0.2mol/L
C.c(CH3COOH) >c(CH3COO-)
D.c(CH3COO-)+ c(OH-)=0.1mol/L
难度: 中等查看答案及解析
-
pH=3的盐酸和pH=11的氨水等体积混合,溶液中离子浓度关系正确的是
A.c(NH4+)>c(Cl-)>c(H+)>c(OH-) B.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C.c(Cl-)>c(NH4+)>c(H+)>c(OH-) D.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
难度: 中等查看答案及解析
-
某有机物分子结构如下:
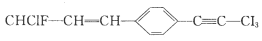
关于该分子结构的说法正确的是
A.除苯环外的其余碳原子有可能都在一条直线上
B.除苯环外的其余碳原子不可能都在一条直线上
C.12个碳原子不可能都在同一平面上
D.12个碳原子一定都在同一平面上
难度: 中等查看答案及解析
-
已知有机物A的红外光谱和核磁共振氢谱如下图,下列说法错误的是
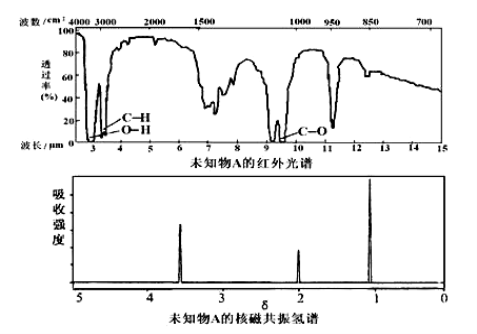
A.由红外光谱可知,该有机物中至少有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子
C.仅由其核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的化学式为C2H6O,则其结构简式为CH3OCH3
难度: 困难查看答案及解析
-
用惰性电极电解下列溶液一段时间后,再加入一定量的某种物质(括号内物质),能够使溶液恢复到原来的成分和浓度的是
A.AgNO3(AgNO3) B.NaOH(NaOH) C.KCl(KCl) D.CuSO4(CuO)
难度: 困难查看答案及解析
-
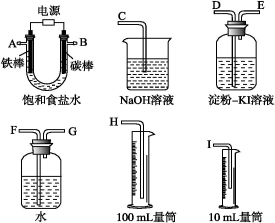
下图各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是
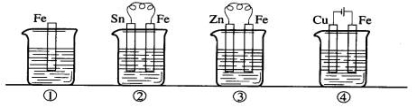
A.④>②>①>③ B.②>①>③>④ C.④>②>③>① D.③>②>④>①
难度: 中等查看答案及解析
-
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
A.氯碱工业中电解饱和食盐水时,阳极的电极反应为:2Cl--2e-=Cl2↑
B.氢氧燃料电池的负极反应:O2+2H2O+4e-=4OH-
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应为:Cu-2e-=Cu2+
D.钢铁发生电化学腐蚀的正极反应:Fe-2e-=Fe2+
难度: 中等查看答案及解析
-
观察下列几个装置示意图,有关叙述正确的是

A.装置①中阳极上析出红色固体
B.装置②的待镀铁制品应与电源正极相连
C.装置③闭合电键后,外电路电子由a极流向b极
D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过
难度: 极难查看答案及解析
-
某小组为研究电化学原理,设计如图装置,下列叙述不正确的是
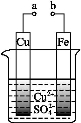
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
难度: 中等查看答案及解析
-
金属镍有广泛的用途。粗镍中含有少量杂质Fe、Zn、Cu、Pt,可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是
A.阳极发生还原反应,其电极反应:Ni2++2e-=Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
难度: 困难查看答案及解析
-
有一支50mL酸式滴定管其中盛有溶液,液面恰好在10mL刻度处,现把管内溶液全部流下排出,用量筒承接,该溶液的体积应为
A.10mL B.40mL C.大于40mL D.小于40ml
难度: 简单查看答案及解析
-
常温下,下列说法正确的是
A.往CH3COOH溶液中加水,c(OHˉ)和c(H+)均增大
B.物质的量浓度均为0.1mol•Lˉ1的CH3COOH溶液和NaOH溶液等体积混合,c(Na+)<c(CH3COOˉ)
C.某浓度的氯化铵溶液中存在c(NH4+)>c(Clˉ)>c(H+)> c(OHˉ)
D.在pH=4的氯化铵溶液中c(H+)+ c(NH4+)= c(Clˉ)+ c(OHˉ)
难度: 中等查看答案及解析
-
常温时,将pH=13的强碱溶液和pH=2的强酸溶液混合,所得溶液的pH=11,则强碱溶液和强酸溶液的体积之比为
A.1:9 B.9:1 C.10:1 D.1:10
难度: 中等查看答案及解析
-
实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙(其pH变色范围为3.1~4.4)作指示剂,下列操作中可能使测定结果偏低的是
A.酸式滴定管在装酸液前未用标准盐酸润洗2~3次
B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
C.锥形瓶溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
难度: 困难查看答案及解析
-
对于常温下0.0lmol/L的氨水,下列叙述正确的是
A.c(H+)+c(NH4+)=c(OH-)
B.与等体积等浓度的氯化铵溶液混合c(NH4+)+c(NH3·H2O)=0.02 mol·L-1
C.与等体积等浓度的盐酸混合后所得溶液显碱性
D.由H2O电离出的c(H+)=1.0×10-12 mol·L-1
难度: 中等查看答案及解析
-
25℃时下列叙述正确的是
A.0.10mol·L-1的三种溶液:①NaCl、②NaOH、③CH3COONa,其pH大小顺序为:③>②>①
B.0.10mol·L-1NaHCO3溶液中:c(CO32-)+c(HCO3-)+c(H2CO3)=0.10mol·L-1
C.pH=2的盐酸和pH=12的NaOH溶液中,水的离子积Kw不同
D.与体积相同、pH=2的盐酸和醋酸完全反应,需要0.010mol·L-1 NaOH的体积相同
难度: 困难查看答案及解析
-
下列溶液中各微粒的浓度关系不正确的是
A.0.1 mol/LCH3COOH溶液中:c(CH3COO-)+ c(CH3COOH)=0.1mol/L
B.NaHCO3溶液中: c(OH-) = c(H+) + c(H2CO3)-c(CO32-)
C.CH3COONa溶液中:c(Na+)> c(CH3COO-)> c(OH-)> c(H+)
D.Na2S溶液中:2 c(Na+)= c(S2-) + c(HS-)+ c(H2S)
难度: 困难查看答案及解析
-
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列说法正确的是
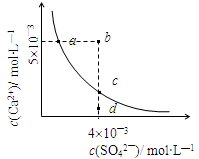
A.常温下CaSO4饱和溶液中,c(Ca2+)、c(SO42—)对应于曲线上任意一点
B.b点将有沉淀生成,平衡后溶液中c(SO42—)等于3×10-3 mol·L—1
C.d点溶液通过蒸发可以变到c点
D.a点对应的Ksp等于c点对应的Ksp
难度: 困难查看答案及解析
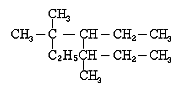 是某有机物结构简式,按系统命名法,该有机物的名称是
是某有机物结构简式,按系统命名法,该有机物的名称是