-
能表明氨水是弱电解质的叙述是
A. NH3·H2O 的导电性比NaOH溶液弱得多
B. 0.1mol/L 的NH3·H2O 的pH值大于7
C. NH4Cl 的水溶液的pH值小于7
D. 5mL 1mol/L的NH3·H2O跟10mL 0.5mol/L的HCl恰好完全反应
难度: 简单查看答案及解析
-
一定量的稀盐酸跟过量锌粉反应时,为了加快反应速率又不影响生成H2的总量,可采取的措施是
A.加入少量稀NaOH溶液 B.加入少量CH3COONa固体
C.加入少量NH4HSO4固体 D.加入少量CuSO4溶液
难度: 简单查看答案及解析
-
下列叙述正确的是
A.常温下pH=12的烧碱和pH=2的盐酸溶液等体积混合,混合液的pH =7
B.pH相同氨水和烧碱溶液稀释相同倍数时,它们的pH仍相同
C.同浓度盐酸中和pH相同的氨水和烧碱溶液,
D.向一定量纯水中通入少量HCl气体后,Kw值增大
难度: 简单查看答案及解析
-
常温、常压下饱和CO2溶液的pH为3.9,用已知浓度的盐酸滴定未知浓度的NaHCO3溶液时,应选用的指示剂及滴定终点的颜色变化是
A.石蕊、由蓝变红 B.酚酞、红色褪去
C.甲基橙、由橙变黄 D.甲基橙、由黄变橙
难度: 简单查看答案及解析
-
下列有关pH变化的判断中,正确的是
A.加热盐酸溶液,溶液的pH减小 B.随温度的升高,纯水的pH增大
C.新制氯水经光照一段时间后,pH减小 D.NaOH溶液久置于空气中,pH增大
难度: 简单查看答案及解析
-
25℃,向1LpH = a的NaOH溶液中滴加pH = b的盐酸10L时,刚好完全中和,则(a+b)的值为
A.13 B.14 C.15 D.12
难度: 简单查看答案及解析
-
下列反应的离子方程式正确的是
A.向KAl(SO4)2溶液中加入Ba(OH)2至SO完全沉淀:
2Ba2++4OH-+Al3++2SO=2BaSO4↓+AlO+2H2O
B.偏铝酸钠溶液中加过量HCl:AlO+4H+=Al3++H2O
C.向NH4HSO3溶液中滴入适量NaOH溶液:HSO+OH-=SO+ H2O [
D.电镀铜时阳极反应为:Cu2+ + 2e-= Cu
难度: 简单查看答案及解析
-
下列是关于盐酸滴定氢氧化钠溶液的实验叙述:①取一锥形瓶用待测NaOH溶液润洗两次;②在锥形瓶中放入25.00mL待测液;③加入几滴石蕊试剂滴至刚变紫色立即停止;④取一只酸式滴定管,洗涤干净;⑤不润洗滴定管,直接往其中注入标准酸溶液,进行滴定;⑥左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶;⑦两眼注视滴定管内盐酸溶液液面下降,直至滴定终点。其中操作错误是
A. ④⑥⑦ B. ①⑤⑥⑦ C. ③⑤⑦ D. ①③⑤⑦
难度: 简单查看答案及解析
-
下列各组离子能大量共存于同一溶液中,且加入过量NaOH溶液或少许稀硫酸时,都能产生白色沉淀的是
A.Ba2+、Mg2+、NO、CO B.Na+、Al3+、Cl-、AlO2-
C.Ba2+、K+、Cl-、HCO D.NH、Fe3+、Ba2+、Cl-
难度: 简单查看答案及解析
-
下列说法不正确的是
A.同温下,0.1 mol•L-1NH4Cl溶液中NH4+的浓度比0.1 mol•L-1氨水中NH4+的浓度大
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl多
C.电解饱和食盐水时,阴极得到氢氧化钠溶液和氢气
D.除去溶液中的Mg2+,用OH-比CO效果好,说明Mg(OH)2的溶解度比MgCO3的小
难度: 简单查看答案及解析
-
一氯代物的同分异构体有2种,二氯代物的同分异构体有4种的烷烃是
A.乙烷 B.丙烷 C.正丁烷 D.新戊烷
难度: 简单查看答案及解析
-
物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合,下列关系式中正确的是
A.c (Na+)=2c(CH3COO-)+2c(CH3COOH)
B.c(H+)=c(CH3COO-)+c(OH-)
C.c (Na+) > c (CH3COO-)>c(OH-)>c(H+)
D.c(CH3COO-) +2c(OH-) = 2c(H+) + c(CH3COOH)
难度: 简单查看答案及解析
-
下列叙述正确的是
A.电解饱和食盐水制烧碱时,Fe作阳极,石墨作阴极
B.电解氯化铜时,阳极上产生的气体质量和阴极上析出的铜的质量相等
C.钢铁在空气中发生电化腐蚀时,铁作负极
D.原电池工作时,阳离子移向电池的负极
难度: 简单查看答案及解析
-
称取三份锌粉,分别盛于甲、乙、丙三支试管中 。甲加入50mLpH=3的盐酸,乙加入50mLpH=3的醋酸,丙加入50mLpH=3的醋酸及少量的胆矾粉末。若反应终了,生成氢气的体积一样多,且没有剩余的锌,则下列说法错误的是
A.开始时反应速率的大小:甲=乙=丙
B.反应过程中,甲、乙速率相同
C.反应终了时,所需时间的大小:甲>乙>丙
D.三支试管中参加反应的锌的质量:甲=乙<丙
难度: 简单查看答案及解析
-
利用电解法可将含有Fe、Zn、Ag、Au等杂质的粗铜提纯,下列叙述正确的是
A. 电解时以纯铜作阳极
B.电解时阴极发生氧化反应
C.粗铜连接电源负极,电极反应是Cu -2e-=Cu2+
D.电解结束,电解槽底部会形成含少量Ag、Au等阳极泥
难度: 简单查看答案及解析
-
用石墨作电极,电解CuSO4溶液,一段时间后,阴极上只析出铜,要恢复到原浓度,应向溶液中加入
A.Cu(OH) 2 B. Cu C.CuSO4 D. CuO
难度: 简单查看答案及解析
-
把物质的量均为0.1mol的AlCl3、CuCl2和H2SO4溶于水制成100 mL的混合溶液,用石墨做电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下体积相同。则下列描述正确的是
A.阳极得到的气体中有O2且为0.35mol B.电路中共转移0.9mol电子
C.阴极质量增加3.2g D.铝元素仅以Al(OH)3的形式存在
难度: 简单查看答案及解析
-
当CH3COOH
CH3COO-+H+已达平衡,若要使醋酸的电离平衡向左移动和溶液的pH值都减小,应加入的试剂是
A.CH3COONa B.NH3·H2O C.HCl D.H2O
难度: 简单查看答案及解析
-
pH=2的A、B两种酸溶液各lmL,分别加水稀释到1000 mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是

A.A、B溶液浓度一定相等
B.稀释后A溶液酸性比B溶液强
C.a=5时,A是强酸,B是弱酸
D.若A、B都是弱酸,则2<a=5
难度: 简单查看答案及解析
-
下列物质的溶液在蒸发皿加热蒸干、灼烧,可以得到该物质固体的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
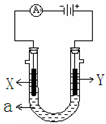
如图a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色。下列说法中不正确的是

A.U形管中溶液碱性增强 B.c上析出红色物质
C.a极和Pt都有气泡产生 D.x是正极,y是负极
难度: 简单查看答案及解析
-
有机物
的正确命名为
A.2 – 乙基– 3,3 – 二甲基戊烷 B.3,3 – 二甲基 – 4–乙基戊烷
C.3,3,4 – 三甲基己烷 D.3,4,4 – 三甲基己烷
难度: 简单查看答案及解析
-
下列有机物互为同分异构体的是
①CH2=CHCH3 ②
③CH3CH2CH3 ④HC
CCH3 ⑤CH3CH=CHCH2CH3
A.①和② B.①和③ C.③和④ D.⑤和③
难度: 简单查看答案及解析
-
下图所示的实验,能达到实验目的的是
A
B
C
D
验证化学能
转化为电能
验证铅蓄电池
放电时Pb为负极
验证铁
发生析氢腐蚀
验证AgCl
溶解度小于Ag2S
难度: 简单查看答案及解析
-
一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,其电池反应为:
2CH3OH + 3O2 + 4OH-
22CO + 6H2O,则下列说法错误的是
A.放电时CH3OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:CH3OH-6e- +8OH- =CO + 6H2O
D.充电时每生成1 mol CH3OH转移6 mol电子
难度: 简单查看答案及解析