-
下列关于物质分类的说法正确的是
A.金刚石、白磷都属于单质
B.漂白粉、石英都属于纯净物
C.氯化铵、次氯酸都属于强电解质
D.葡萄糖、蛋白质都属于高分子化合物
难度: 简单查看答案及解析
-
如下图所示装置是化学实验室中的常用装置,它有多种用途,以下各项用途和操作都正确的是 ( )
A. 洗气或干燥装置:瓶内放一定体积溶液,由a管口进气
B. 用于收集不溶于水的气体:瓶内充满水,由b管口进气
C. 提供少量
:瓶内充满
,b管口接自来水龙头
D.
和
反应的装置:由a管口通入
,b管口通入
难度: 中等查看答案及解析
-
在含有
、
、
和
各0.1
的混合溶液中加入0.1
铁粉,充分搅拌后铁完全反应,且溶液中不存在
,同时又析出0.1
.则下列结论中不正确的是( )
A. 反应后溶液中
与
的物质的量之比为1:2
B. 氧化性:
C. 含
的溶液可腐蚀铜板
D. 1
可还原2
难度: 困难查看答案及解析
-
将标准状况下的
(
)溶于1000
水中,得到的盐酸密度为
则该盐酸的物质的量浓度是( )
A.
B.
C.
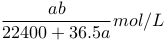
D.

难度: 困难查看答案及解析
-
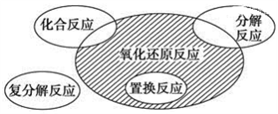
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是( )
A.
B.
C.
D.
(提示:
中的氧为-1价)
难度: 中等查看答案及解析
-
赤铜矿的主要成分是
,辉铜矿的主要成分是
,将赤铜矿与辉铜矿混合加热发生以下反应:
,关于该反应的说法中,正确的是( )
A. 该反应的氧化剂只有
B.
在反应中既是氧化剂,又是还原剂
C.
既是氧化产物又是还原产物
D. 每生成19.2
,反应中转移1.8
电子
难度: 中等查看答案及解析
-
下列关于电解质说法正确的是( )
A. 能导电的物质叫电解质
B.
晶体不导电,所以
不是电解质
C. 电解质在通电时发生电离
D. 熔融的
导电,所以
是电解质
难度: 简单查看答案及解析
-
表中关于物质分类的正确组合是( )
类别
组合
酸性氧化物
碱性氧化物
酸
碱
盐
A
B
C
D
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作方法均正确的一组是( )
选项
待提纯的物质
选用的试剂
操作的方法
A
CaO(CaCO3)
水
溶解、过滤、结晶
B
Cu(CuO)
稀盐酸
溶解、过滤、洗涤、干燥
C
CuSO4(H2SO4)
氢氧化钠溶液
过滤
D
CO(H2)
氧气
点燃
难度: 中等查看答案及解析
-
中含有
个氢原子,则阿伏加德罗常数为( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A. 直径介于1~100
之间的微粒称为胶体
B.
胶体是纯净物
C. 利用丁达尔现象可以区别溶液和胶体
D. 胶体粒子很小,可以透过半透膜
难度: 简单查看答案及解析
-
分类是化学学习和研究中的常用手段。下列分类依据和结论都正确的是( )
A.
、
、
均可由活泼金属和活泼非金属作用形成,都是离子化合物
B.
、
、
均具有氧化性,都是氧化性酸
C.
、
、
、
熔融状态或溶于水时能导电,都是电解质
D.
、
、
中均含有氧,都是氧化物
难度: 中等查看答案及解析
-
属于氧化还原反应的离子方程式是( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
、
、
、
、
,可按某种标准划分为同一类物质,下列分类标准中不正确的是( )
A. 电解质 B. 钠的化合物 C. 离子化合物 D. 钠盐
难度: 简单查看答案及解析
-
下列分散系中,分散质微粒半径最小的是( )
A. 石灰乳 B. 蛋白质溶液 C. 雾 D. 硝酸钾溶液
难度: 简单查看答案及解析
-
是常规核裂变产物之一,可以通过测定大气或水中
的含量变化来监测核电站是否发生放射性物质泄漏。下列有关
的叙述中错误的是
A.
的化学性质与
相同 B.
的原子序数为53
C.
的原子核外电子数为78 D.
的原子核内中子数多于质子数
难度: 简单查看答案及解析