-
美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数为118、中子数为175的超重元素,该元素原子核内的中子数和核外电子数之差为
A.57 B.7 C.61 D.293
难度: 简单查看答案及解析
-
N的质量数为14,在微粒NH3中,电子数、质子数、中子数之比为
A.10:7: 11 B.10:11:9
C.10:11:8 D.10:10:7
难度: 简单查看答案及解析
-
下列物质中,属于离子晶体的是
A.铜 B.蒸馏水 C.石墨 D.食盐晶体
难度: 简单查看答案及解析
-
下列化学变化中需加入氧化剂才能实现的是
A.Fe→FeCl2 B.SO3→H2SO4
C.CO2→CO D.KMnO4→MnCl2
难度: 简单查看答案及解析
-
0.012kg14C含有的碳原子数
A.等于NA B.小于NA
C.大于NA D.无法判断
难度: 简单查看答案及解析
-
某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的核电荷数为
A.11 B.15 C.17 D.34
难度: 简单查看答案及解析
-
R2O8n-离子在一定条件下可以把Mn2+离子氧化为MnO4-,若反应后R2O8n-变为RO42离子。又知反应中氧化剂与还原剂的物质的量之比为5:2。则n的值是
A.1 B.2 C.3 D.4
难度: 简单查看答案及解析
-
由极性键形成的非极性分子的是
A.CO2 P4 B.NH3 C.H2O D.KCl
难度: 简单查看答案及解析
-
主族元素在周期表中的位置取决于该元素原子的
A.相对原子质量和核外电子数
B.电子层数和最外层电子数
C.相对原子质量和最外层电子数
D.电子层数和次外层电子数
难度: 简单查看答案及解析
-
根据反应:2H2S+O2==2S↓+2H2O, 4NaI+O2+2H2SO4==2I2+2Na2SO4+2H2O,
Na2S+I2==2NaI+S↓ 判断下列物质的氧化性强弱,正确的是
A.O2>I2>S B.H2S>NaI>H2O
C.S>I2>O2 D.H2O>NaI>H2S
难度: 简单查看答案及解析
-
下列微粒中,跟NH4+的电子总数和质子总数都相同的是
A.Ne B.F- C.CH4 D.H3O+
难度: 简单查看答案及解析
-
下列反应中一定属于氧化还原反应的是
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
难度: 简单查看答案及解析
-
下列说法中,正确的是
A.失去电子是还原剂,具有氧化性
B.氧化还原反应的本质是元素化合价的升降
C.阳离子只有氧化性,阴离子只有还原性
D.氧化还原反应中,某元素由化合态变为游离态,此可能被还原,也可能被氧化
难度: 简单查看答案及解析
-
简单原子的原子结构可用下图形象地表示:其中●表示质子或电子,o表示中子,则下列有关①②③的叙述正确的是
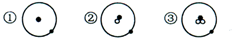
A.①②③具有相同的质量数
B.①②③为三种不同元素的原子
C.①③互为同位素
D.②③是二种化学性质完全不同的粒子
难度: 简单查看答案及解析
-
X元素原子的质量数为m,核内中子数为n,则wgx+含有电子的物质的量是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列试剂的存放正确的是
A.钾、钠在空气中极易氧化,与水发生剧烈反应,应放在盛有煤油的广口瓶中以隔绝空气
B.盛放氢氧化钠溶液的瓶口用玻璃塞塞紧,不能用橡皮塞
C.浓硝酸、硝酸银见光易分解,应存放在棕色细口瓶中,低温避光保存
D.以上方法都不正确
难度: 简单查看答案及解析
-
在含有70克N2,128克O2和44克CO2的混和气体(标准状况)中,氮气所占体积百分比为
A. 29.3% B. 33.3% C. 36% D. 50%
难度: 简单查看答案及解析
-
有
和
两种离子,其电子层结构相同。下列关系式或化学式正确的是
A.a-n=b+m B.氧化物为YOm
C.a+m=b-n D.氢化物为HnX或XHn
难度: 简单查看答案及解析
-
若NA表示阿伏加德罗常数,下列说法正确的是
A.在同温同压时,相同体积的任何气体所含的原子数目相同
B.将49g H2SO4溶于1L水中,所得溶液的物质的量浓度为0. 5mol·L-1
C.标准状况下,11.2L水所含分子数为0.5 NA
D.18g NH4+含有的电子数为10NA
难度: 简单查看答案及解析
-
在标准状况下有①6.72L CH4,②3.01
1023个HCl分子,③13.6gH2S,④0.2mol氨气。下列对这四种气体的关系从大到小描述不正确的是
A.体积:②>③>①>④
B.氢原子数:①>④>③>②
C.质量:②>③>①>④
D.密度:②>③>④>①
难度: 简单查看答案及解析
-
制印刷电路时常用氯化铁作为腐蚀液,发生反应为2FeCl3+Cu=2FeCl2+CuCl2,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
A. 烧杯中有铜无铁 B. 烧杯中有铁无铜
C. 烧杯中铜,铁都有 D. 烧杯中铜铁都无
难度: 简单查看答案及解析