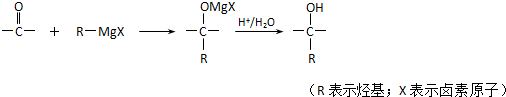
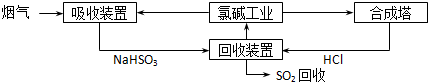
-
根据表中信息判断,下列选项不正确的是( )
序号 反应物 产物 ① KMnO4、H2O2、H2SO4 K2SO4、MnSO4 ② Cl2、FeBr2 FeCl3、FeBr3 ③ MnO4- Cl2、Mn2+
A.第①组反应的其余产物为H2O和O2
B.第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2
C.第③组反应中生成1mo1Cl2,转移电子2mol
D.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2难度: 中等查看答案及解析
-
下列说法正确的是( )
A.碘、铁都是人体必需的微量元素
B.淀粉和纤维素互为同分异构体,均可水解得到葡萄糖
C.碳酸钡、碳酸氢钠、氢氧化镁等均可作为抗酸药物使用
D.聚氯乙烯塑料制品可用于食品包装难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.46g C2H6O中共用电子对数为8×6.02×1023
B.20g重水(D2O)中含有的电子数为10×6.02×1023
C.100mL 2.0 mol•L-1 NH4HCO3溶液中NH4+数为0.2×6.02×1023
D.标准状况下,22.4L NO与CO的混合气体中含有的原子数为2×6.02×1023难度: 中等查看答案及解析
-
下列事实可以用同一原理解释的是( )
A.漂白粉和明矾都常用于自来水的处理
B.乙烯可使溴水或酸性高锰酸钾溶液褪色
C.铁片和铝片置于冷的浓硫酸中均无明显现象
D.苯酚和氢氧化钠溶液在空气中久置均会变质难度: 中等查看答案及解析
-
模拟铁的电化学防护的实验装置如图所示,下列说法错误的是( )

A.若X为碳棒,开关K置于A处可减缓铁的腐蚀
B.若X为锌棒,开关K置于A处或B处均可减缓铁的腐蚀
C.若X为锌棒,开关K置于B处时,铁电极上发生的反应为2H++2e-═H2↑
D.若X为碳棒,开关K置于A处时,铁电极上发生的反应为2H++2e-═H2↑难度: 中等查看答案及解析
-
氢化热是指一定条件下,1mol 不饱和化合物加氢时放出的热量.表中是环己烯(
)、环己二烯(
)和苯的氢化热数据.
下列说法正确的是( )化合物 +H2
+2H2
+3H2
氢化热△H -119.7 -232.7 -208.4
A.环己二烯与H2的反应最剧烈
B.环己烯、环己二烯和苯有相同的官能团
C.三种化合物中环己二烯的稳定性最强
D.上述条件下,1 mol转变为
时放热113 kJ
难度: 中等查看答案及解析
-
T℃时,将6mol CO2和8mol H2充入2L密闭容器中,发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化.下列说法正确的是( )

A.反应开始至a点时v(H2)=1 mol•L-1•min-1
B.若曲线Ⅰ对应的条件改变是升温,则该反应△H>0
C.曲线Ⅱ对应的条件改变是降低压强
D.T℃时,该反应的化学平衡常数为0.125难度: 中等查看答案及解析