-
今年“地球一小时”活动的主题是“开启我的60+生活”,呼吁公众超越“60分钟”的思考和环保行动转变。下列做法不符合这一环保主题的是( )
A. 自带布袋购物
B. 草稿纸尽可能两面使用
C. 提倡使用一次性木筷
D. 选择自行车作为出行工具
难度: 简单查看答案及解析
-
陶瓷是中华民族在人类科技史上的伟大发明下列陶瓷制作工艺中发生化学变化的是( )
A.
 混合 B.
混合 B.  成型
成型C.
 晾干 D.
晾干 D.  烧结
烧结难度: 简单查看答案及解析
-
下列物质中,含有氧分子的是( )
A. 空气 B. MnO2 C. CO2 D. H2O2
难度: 简单查看答案及解析
-
溶液在我们生活中有着广泛的应用,下列物质不属于溶液的是( )
A. 矿泉水 B. 冰水 C. 碘酒 D. 白醋
难度: 简单查看答案及解析
-
下列做法不能有效改善大气质量的是( )
A. 大量生产、使用能过滤PM2.5的口罩
B. 对煤燃烧后形成的烟气进行尾气处理
C. 开发利用太阳能、氢能、风能等清洁能源
D. 研究廉价、高效的催化剂,以降低汽车尾气中有害物质的含量
难度: 简单查看答案及解析
-
中国最新战机歼﹣31使用了高强度、耐高温的钛合金材料。钛元素的信息如图所示,对图中信息解释不正确的是( )

A. 钛是一种金属元素 B. 核内中子数为22
C. 元素符号为Ti D. 相对原子质量为47.87
难度: 中等查看答案及解析
-
下列关于实验现象的描述不正确的是( )
A. 镁条在空气中燃烧,发出耀眼的白光
B. 细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
C. 蜡烛在氧气中燃烧比空气里燃烧得更旺,发出白光
D. 加热试管中的铜绿固体,绿色粉末逐渐变黑
难度: 简单查看答案及解析
-
水果散发出诱人的香味,你能闻到香味的原因是( )

A. 分子在不断运动 B. 分子的质量很小
C. 分子之间有间隔 D. 分子的体积很小
难度: 简单查看答案及解析
-
“毒胶囊”泛指利用由工业皮革废料为原料生产的含重金属铬(Cr)超标的胶囊,其中含有可能引起人体肾伤害的+6价的铬.下列铬的化合物中铬呈+6价的是( )
A. Cr2O3 B. CrCl2 C. Cr2(SO4)3 D. K2CrO4
难度: 中等查看答案及解析
-
豆浆又被称为“植物牛奶”,其营养价值可以与牛奶相媲美,其中含有的异黄酮(C15H10O2)更是具有防癌功能,下列关于异黄酮的说法正确的是( )
A. 异黄酮中共含有17个原子
B. 异黄酮的相对分子质量是222g
C. 异黄酮中氧元素的质量分数最小
D. 异黄酮由三种元素组成
难度: 简单查看答案及解析
-
下列说法不符合化学常识的是( )
A. 可用肥皂水鉴别硬水和软水
B. 生铁的含碳量较钢低,韧性更好
C. 金属铝表面的氧化膜对铝起保护作用
D. 铁锈是铁跟氧气、水共同作用的结果
难度: 简单查看答案及解析
-
若下列实验涉及的化学反应均能完全进行,则有关CO2、CO的实验设计错误的是( )
A.
 鉴别CO2、CO B.
鉴别CO2、CO B.  鉴别CO2、CO
鉴别CO2、COC.
 除去少量CO2 D.
除去少量CO2 D.  除去少量CO
除去少量CO难度: 简单查看答案及解析
-
用溶质质量分数为98%的浓硫酸10mL(密度为1.84g•mL﹣1)配制溶质质量分数为10%的硫酸溶液,下列说法正确的是( )
A. 应量取的水的体积为180mL
B. 量取浓硫酸时仰视读数,则所得溶液的质量分数小于10%
C. 实验中需要仪器有:烧杯、相应规格的量筒、胶头滴管、玻璃棒
D. 装瓶时不小心洒漏一部分溶液,则瓶中硫酸溶液浓度小于10%
难度: 简单查看答案及解析
-
在密闭容器中有甲、乙、丙、丁四种物质、在一定条件下反应,测得反应前及反应过程中的两个时刻各物质的质量分数如下图所示。图中a、b、c、d分别表示相应物质的质量分数。下列数据正确的是
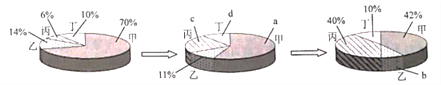
A. a=56% B. b=6% C. c=17% D. d=8%
难度: 中等查看答案及解析
-
在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物X.取一定质量的AgNO3固体充分光照,测得反应后生成Ag、O2、X的质量分别为21.6g、mg、9.2g。下列说法正确的是( )
A. AgNO3固体应密封保存在无色细口瓶中
B. m=3.2
C. X的化学式为NO
D. 该反应方程式中Ag与O2的化学计量数之比为3:2
难度: 困难查看答案及解析
-
两种固体物质(均不含结晶水的溶解度曲线如图所示。下列说法不正确的是( )

A. 40℃时,甲的溶解度大于乙的溶解度
B. 20℃时,等质量的甲、乙溶液中溶质质量一定相等
C. 将40℃时乙的饱和溶液降温至20℃,仍然是饱和溶液
D. 将甲的饱和溶液转化为不饱和,溶质质量分数可能减小
难度: 简单查看答案及解析
-
下列关于溶液的说法不正确的是( )
A. 水是一种最常见的溶剂
B. 溶液都能导电
C. 少量固体溶于水,使稀溶液凝点降低
D. 硝酸铵溶于水,使溶液温度降低
难度: 简单查看答案及解析
-
能反映相关实验过程中量的变化的图象是( )
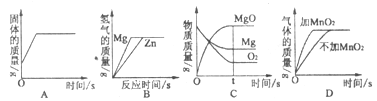
A. 用一氧化碳还原氧化铁
B. 等质量镁、锌分别和足量等质量分数的盐酸反应
C. 镁在氧气中燃烧
D. 等质量、等质量分数的双氧水完全分解
难度: 困难查看答案及解析